Теория:
Гелий (He) в периодической системе: 1‑й период, 18‑я группа (по устаревшей классификации — VIII A), атомная масса 4,0026 а.е.м.
Занимает положение в 1‑м периоде, что определяет наличие всего одного электронного уровня в его атоме.
Гелий — второй по распространенности элемент во Вселенной (после водорода), однако на Земле он встречается гораздо реже и добывается в основном из природного газа.
В чистом виде это инертный одноатомный газ без цвета, вкуса и запаха, который практически не вступает в химические реакции.
Будучи химическим элементом s-блока (несмотря на положение в правой части таблицы), он возглавляет группу благородных газов, находясь над неоном и аргоном.
Нахождение Гелия в 18‑й группе и наличие полностью заполненного внешнего электронного слоя обуславливают его ключевые параметры:
Нулевую валентность (не образует устойчивых химических связей).
А также широчайшее применение в технике (криогеника, охлаждение ядерных реакторов, сварочные работы), медицине (МРТ) и воздухоплавании (наполнение метеозондов и дирижаблей).
Структура атома подтверждается его электронной формулой (конфигурацией):
1s2.
На которой наглядно можно определить его положение как s-блочного элемента с завершенным энергетическим уровнем.
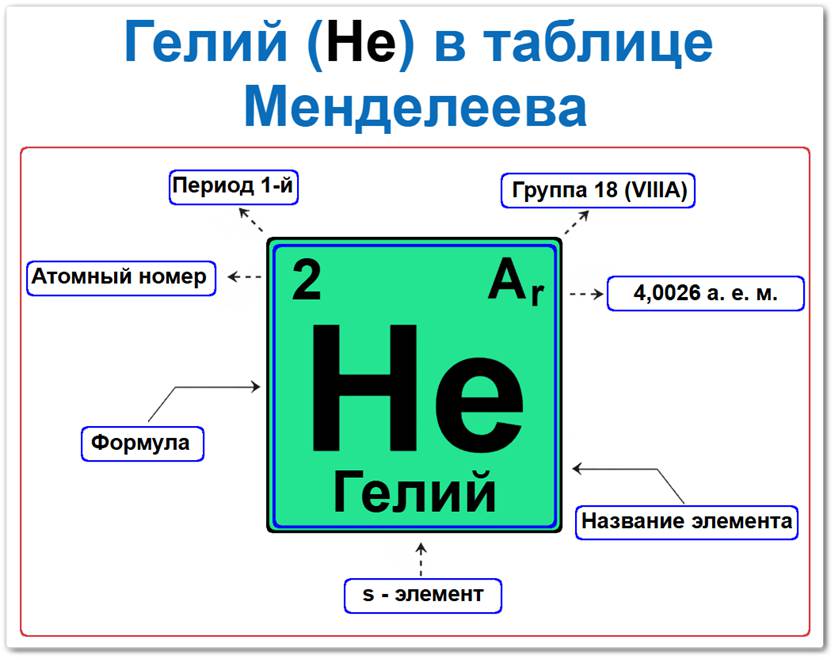
Гелий элемент таблицы Менделеева который можно определить на основании закона периодичности: положение в ряду благородных газов период 1, группа 18, а также по его порядковому номеру (Z = 2).
Содержание страницы
- 1. Как определить положение Гелия в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 2)
- 3. Название и символ
- 4. Группа (18 / VIII A)
- 5. Период (1‑й)
- 6. Относительная атомная масса (Ar)
- 7. s‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Гелия по Таблице Менделеева
- 9. Проверка знаний: Как определить гелий по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Гелия в Таблице Менделеева
Локация гелия в таблице описывается его уникальным статусом самого легкого инертного газа — его «химическим аттестатом»:
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (18-я группа, благородные газы).
- Период (горизонтальный ряд).
- Электронное семейство (гелий — s‑элемент).
Порядковый номер / атомный номер (Z = 2)
- Служит уникальным кодом элемента в системе.
- В ядре самого распространенного изотопа — 2 протона и 2 нейтрона; в оболочке — 2 электрона.
- Электронное строение: 2.
Интересно: Для мастера гелий важен в сварочном деле. Его используют как защитную среду при сварке активных металлов (например, алюминия или магния), чтобы предотвратить их окисление на воздухе. В справочниках по металлообработке гелиевая сварка считается одной из самых чистых.
Название и символ
- Название: «гелий» (от греч. helios — «солнце», так как он был открыт на Солнце раньше, чем на Земле).
- Символ: He (Helium).
- Примечание: Гелий обладает самой низкой температурой кипения среди всех веществ (–268,9 °C), что делает его незаменимым для достижения сверхнизких температур.
Группа (18 / VIII A)
Расположен в 18‑й группе. В периодической системе гелий находится на вершине колонки инертных газов и относится к (подгруппе гелия).
Химический потенциал:
- Валентность гелия: 0.
- Степень окисления: 0. Гелий — самый «необщительный» элемент; он не горит, не поддерживает горение и не вступает в реакции даже при сильном нагреве.
Период (1‑й)
Находится в 1‑м периоде — это самый короткий период, в котором всего два элемента (водород и гелий).
Влияние на свойства:
- Химическая активность: Отсутствует. Из-за близости электронов к ядру их практически невозможно «оторвать» или добавить новые.
- Техническое значение: Благодаря своей легкости и негорючести гелий гораздо безопаснее водорода для наполнения аэростатов.
Все значения элементов в полной сводной таблице параметров химических элементов.
Относительная атомная масса (Ar)
- Ar(He) ≈ 4,0026 а.е.м.
- Определение: среднее значение массы изотопов (в основном Гелий-4). Гелий в 7 раз легче воздуха.
Все значения для всех элементов можно узнать в таблице атомных масс.
s‑Элемент (электронное семейство)
Заполнен внешний (и единственный) 1s‑подуровень (1s2).
Специфика блока: Хотя гелий стоит в 18-й группе с p-элементами, по строению он является s-элементом. Это исключение сделано для того, чтобы подчеркнуть его полную инертность, схожую с другими благородными газами.
Определение энергетических уровней Гелия по Таблице Менделеева
Положение Гелия (He) показывает предельную простоту его атома.
1. 1-й период (Один уровень)
- Итог: У Гелия всего 1 энергетический уровень.
2. Список «жильцов» (Распределение электронов)
Атомный номер Гелия — 2. Распределение:
He ) 2
3. 18-я группа (Инертный характер)
- s-элемент: Полностью закрытая оболочка (дублет).
- Свойства: Газ, не имеющий цвета и запаха, самый химически пассивный элемент во всей таблице.
Проверка знаний: Как определить гелий по таблице Менделеева
Выберите три верных тезиса, характеризующих Гелий (He).
Показать верные ответы
Правильные ответы: 1, 2, 3
Гелий — самый легкий инертный газ, у него всего один уровень и атомный номер 2.
Часто задаваемые вопросы:
Хотя у гелия всего 2 электрона (как у элементов 2-й группы), он стоит в 18-й (VIIIА) группе.
Причина: Его единственный электронный слой полностью заполнен. Это делает гелий химически инертным («благородным»).
По свойствам он — идеальный газ, поэтому он находится в компании неона и аргона, а не активных металлов.
Гелий (He) находится в правом верхнем углу таблицы Менделеева.
Период: 1-йГруппа: 18-я (по старой классификации — VIIIА группа, главная подгруппа 8-й группы).
Порядковый номер: 2.
Относится к главной подгруппе VIII группы (согласно современной классификации — 18-я группа).
Это семейство благородных (инертных) газов.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.