Менделевий это простое вещество, химический элемент 3-й группы (по устаревшей классификации — побочной подгруппы третьей группы, IIIB).
Cедьмого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 101 и символом Md.
Считается трансурановым элементом.
Он был первоначально синтезирован в 1955 году советскими учеными. Менделевий является тяжелым металлом, который обладает высокой радиоактивностью.
Его химические свойства плохо изучены из-за ограниченного количества доступного материала для исследования.
Менделевий получил свое название в честь Дмитрия Ивановича Менделеева, создателя периодической системы химических элементов.
Содержание страницы
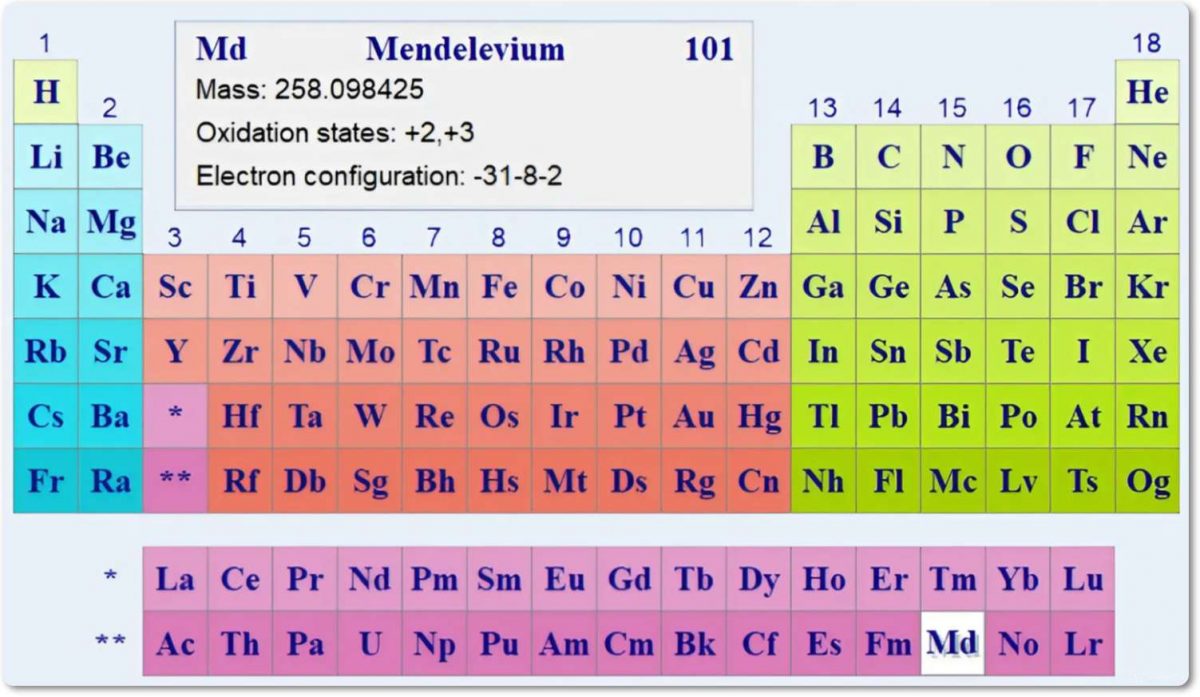
Что такое менделевий
(Mendelevium; по имени русского химика Д. И. Менделеева), Md — искусственно полученный радиоактивный химический элемент.
Атомный номер 101; относится к актиноидам.
Для менделевий характерна степень окисления + 3, может иметь и степени окисления + 2 и + 1.
История
Впервые синтезирован и идентифицирован (1955) американским учеными Г. Сиборгом, А. Гиорсо, Б. Гарвеем, Г. Чоппином и С. Томпсоном в виде изотопа 256Md, считанные атомы которого были получены при облучении мишени из изотопа 253Es альфа-частицами.
Физические химические свойства
Атомная масса (молярная масса) 258,1 а. е. м. (г/моль)
Электронная конфигурация химического элемента Менделевий: [Rn]5f137s2, полная электронная конфигурация 1s22s22p63s23p64s23d104p65s24d105p66s24f145d106p65f137s2.
Электроотрицательность 1,3 (шкала Полинга). Электродный потенциал Md ← Md3+: −1,7 В
Md ← Md2+: −2,4 В.
Степени окисления +1, +2, +3. Энергия ионизации (первый электрон) 635 (6,58) кДж/моль (эВ).
Интересный факт: Менделевий был первым химическим элементом, который был назван в честь Дмитрия Ивановича Менделеева, великого русского химика, создателя периодической системы химических элементов.
Химические свойства
1. Степени окисления:
✅ +3 (наиболее стабильная и распространенная): Как и большинство других актинидов, менделевий в водном растворе стабилен в степени окисления +3.
Это наиболее типичное состояние для тяжелых актинидов. Он образует Md3+ ионы.
✅ +2 (умеренно стабильная): Менделевий также способен проявлять степень окисления +2.
Это отличает его от некоторых других актинидов и сближает его с лантанидами, такими как европий (Eu) и иттербий (Yb), которые тоже могут существовать в состоянии +2. Md3+ относительно легко восстанавливается до Md2+.
✅ +1 (обнаружена, но менее изучена): Есть экспериментальные данные, указывающие на возможность существования степени окисления +1 у менделевия.
Что делает его уникальным среди актинидов и более похожим на щелочные металлы в некоторых условиях (например, в водно-этанольных растворах).
Однако эта степень окисления менее подтверждена и стабильна по сравнению с +2 и +3.
2. Реактивность:
✅ Поскольку менделевий является металлом и актинидом, можно ожидать, что он будет достаточно реактивным, как и другие элементы этой группы.
Однако из-за его радиоактивности и крайне малых количеств, прямые эксперименты по его реактивности с различными веществами затруднены.
✅ В растворах он ведет себя как типичный актинид, образуя нерастворимые фториды и гидроксиды, подобно трехвалентным лантанидам.
✅ +3 (Наиболее стабильная), +2 (Умеренно стабильная) и +1 (Редкая).
Изотопы
Стабильных изотопов не имеет. Известно 10 изотопов менделевий с массовыми числами от 248 до 252 и от 254 до 258.
Наиболее долгоживущий — альфа-радиоактивный изотоп 258Md, время жизни к-рого 55 суток.
Получение
Это сложный процесс, осуществляемый только в специализированных ядерных лабораториях с использованием ускорителей частиц.
Исторический метод получения (первый синтез):
Менделевий был впервые синтезирован в 1955 году группой ученых во главе с Альбертом Гиорсо, Бернардом Харви, Грегори Чоппином, Стенли Томпсоном и Гленном Сиборгом в Радиационной лаборатории имени Лоуренса в Беркли, Калифорния (США).
Заключался в следующем:
Мишень: Использовалась мишень из чрезвычайно редкого и высокорадиоактивного изотопа эйштейния-253 (253Es).
Бомбардировка: Мишень бомбардировали высокоэнергетическими альфа-частицами (ядрами гелия, 4He) в циклотроне (ускорителе частиц).
Ядерная реакция: В результате захвата альфа-частиц ядром эйштейния-253 и последующего испускания нейтронов образовались ядра менделевия-256 (256Md).
Уравнение реакции:
253Es + 4He → 256Md + n
(где n — нейтрон)
Этот эксперимент был примечателен тем, что менделевий был получен буквально поатомно.
За все время эксперимента было синтезировано всего около 17 атомов менделевия-256.
Для идентификации этих атомов использовались сложнейшие химические методы разделения ионов и регистрации актов спонтанного деления.
Современные методы получения:
В настоящее время менделевий получают аналогичными методами:
Использование более тяжелых актинидных изотопов в качестве мишеней (например, другие изотопы эйштейния или фермия).
Бомбардировка различными легкими ионами (например, ядрами углерода, азота, кислорода), а не только альфа-частицами.
Реакции проводятся на мощных ускорителях тяжелых ионов.
Применение
Особого интереса для применения не имеет из за его метода искусственного получения и радиоактивности.
✅Расширения знаний о трансурановых элементах: Изучение его химических, физических и ядерных свойств помогает ученым понять, как ведут себя элементы с очень большими атомными номерами, и проверить предсказания Периодической таблицы.
✅ Ядерные исследования: Его изотопы используются для изучения процессов ядерного деления, стабильности ядер и фундаментальных аспектов ядерной физики.
✅Синтез новых, более тяжелых элементов: Менделевий может быть использован в качестве мишени в ускорителях частиц для создания еще более тяжелых, пока неизвестных или плохо изученных химических элементов.
Литература
Мясоедов Б. Ф.. Аналитическая химия трансплутониевых элементов.
Часто задаваемые вопросы
Нужен исключительно для расширения границ научного познания в области ядерной химии и физики, а не для создания каких-либо продуктов или технологий.
Применяется только в исследовательских целях, для получения других химических элементов.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.