Калифорний — искусственный радиоактивный химический элемент, актиноид, обозначаемый Cf, имеющий атомный номер 98 в периодической системе Менделеева.
Считается трансурановым элементом.
Известны радиоизотопы с массовыми числами 237—256. Стабильных изотопов не имеет.
Калифорний был открыт в 1950 году американскими учёными Альбертом Гиорсо и Гленом Сиборгом в Университете Калифорнии.
Содержание страницы
Что такое калифорний химический элемент
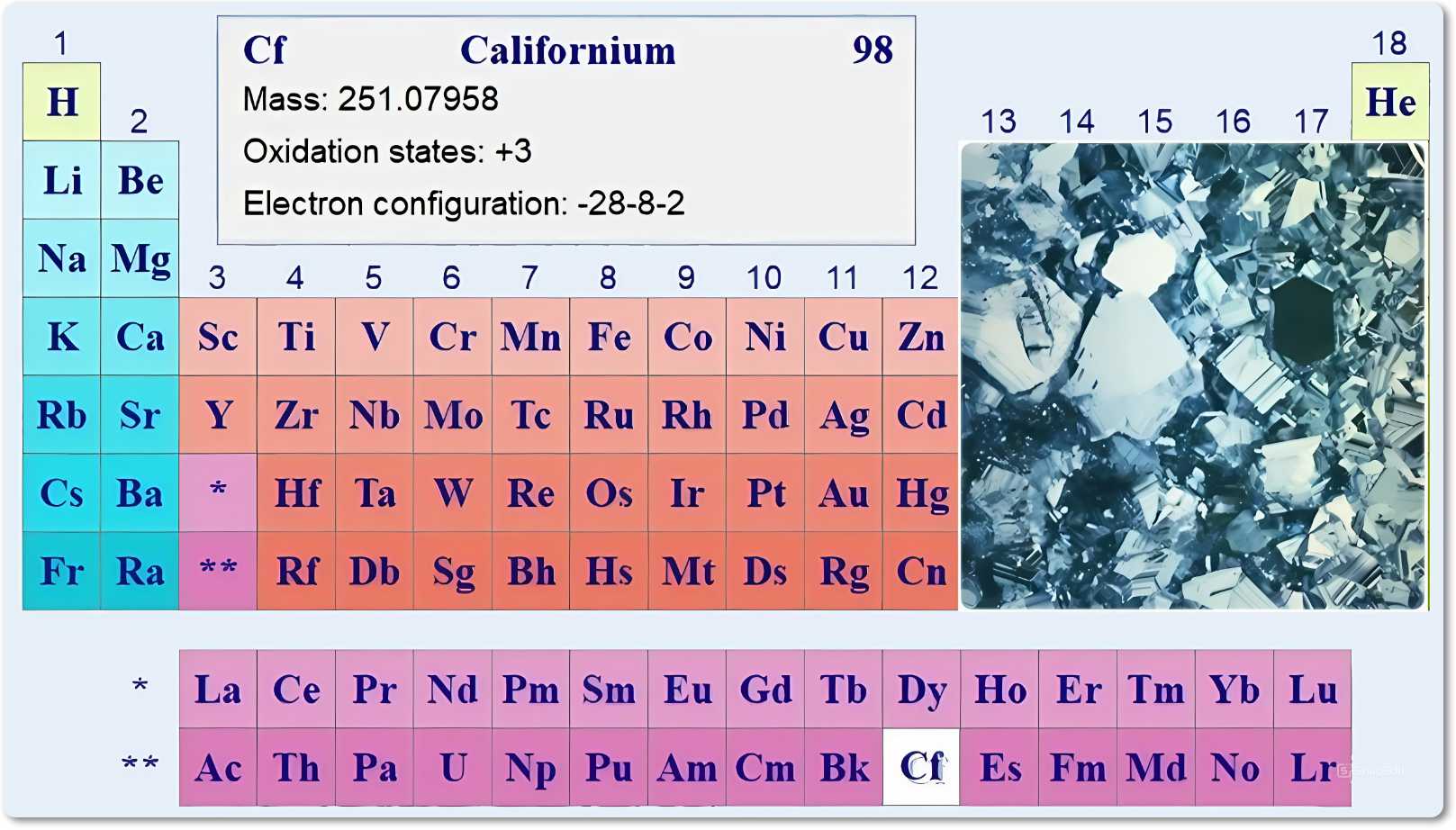
[Californium; от назв. штата Калифорния (California) в США], Cf — это искусственно полученный радиоактивный химический элемент.
Атомный номер. 98;примерная атомная масса [251] а.е.м. относится к актиноидам.
Для калифорний характерна степень окисления +3. Впервые синтезирован и идентифицирован в 1950 амер. учеными С. Томпсоном, А. Гиорсо и Г. Сиборгом в виде изотопа 245Cf, к-рый образовывался в результате облучения мишени из изотопа 242Сf ускоренными альфа-частицами.
Стабильных изотопов не имеет. Известны 16 изотопов калифорний с массовыми числами от 240 до 255.
Свойства
Наиболее долгоживущие — альфа-радиоактивные изотопы 251Cf, 249Cf, 250Cf и 262Cf с периодами полураспада соответственно около 900 лет; 352; 13,1 и 2,63 года.
Электронная конфигурация [Rn] 5f107s2
Их получают в весовых количествах в ядерном реакторе при длительном облучений плутония нейтронами.
Металлический калифорний существует в двух модификациях:
- Гранецентрированной кубической структуре с периодом решетки а0 = 5,743 ± 0,006 А.
- Гексагональной структуре плотной упаковки с периодами решетки а0 = 3,988 1 0,004 А и с0 = 6,887 ± 0,008 А. Т-ра плавления К. 900 ± 30° С.
Интересный факт: 252Cf является одним из самых дорогих веществ на Земле.
Его цена может достигать десятков миллионов долларов за грамм, что делает его в тысячи раз дороже золота или платины.
Степени окисления
Наиболее устойчивой и распространенной степенью окисления для калифорния является +3.
Также известны соединения, где калифорний проявляет степень окисления +2 и +4.
Получение этих состояний обычно требует специфических условий (сильные восстановители или окислители).
Cf(II) получают, например, электрохимическим восстановлением из водных растворов Cf3+.
Cf(IV) образуется при действии сильных окислителей на соединения Cf3+.
Химические свойства
Калифорний образует различные классы соединений, в основном в степени окисления +3:
Оксиды:
Оксид калифорния(III) (Cf2O3): Бесцветные кристаллы. Образуются при сжигании металлического калифорния или его соединений на воздухе.
Диоксид калифорния (CfO2): Может быть получен окислением Cf2O3 кислородом при нагревании под давлением.
Галогениды (CfX3): Образуются при реакции оксида калифорния(III) с галогенводородами при нагревании. Известны трифторид, трихлорид, трибромид и трииодид калифорния.
Также синтезированы оксигалогениды (CfOX), например, CfOCl.
Дииодид калифорния (CfI2) также синтезирован.
Тетрафторид калифорния (CfF4) образуется при окислении фторида калифорния (III) фтором при 450° C и давлении.
Комплексные соединения:
В водных растворах пятивалентный калифорний, как и другие актиноиды, склонен к комплексообразованию, гидролизу и полимеризации.
Известны фторопротактинаты, сульфопротактинаты, оксалаты, а также карбид и нитрид калифорния.
Недавно были получены металлоорганические соединения калифорния со связью калифорний-углерод, что расширяет представления о его химических возможностях.
Растворимость:
Соединения трехвалентного калифорния, такие как нитрат, сульфат, галогениды и перхлорат, растворимы в воде в виде катиона Cf3+.
Изучение химических свойств калифорния затруднено из-за его высокой радиоактивности и явления радиолиза, которое может разрушать молекулы под действием собственного излучения.
Изотопы
Из всех изотопов калифорния наибольшее практическое значение имеет изотоп 262Cf, к-рый в 3% случаев испытывает спонтанное деление, сопровождающееся испусканием нейтронов.
1 мг изотопа 252Cf испускает 2,2 х 109 нейтронов/сек , что позволяет создавать очень компактные и мощные источники нейтронов/
Которые найдут широкое применение в медицине, геологии, геофизике и др.
Литература
Мясоедов Б. Ф. (и др.). Аналитическая химия трансплутониевых элементов. ; Хайд Э., Перлман И., Сиборг Г. Ядерные свойства тяжелых элементов, в. 1. Трансурановые элементы. Пер. с англ.
Часто задаваемые вопросы
Калифорний-252 — мощный источник нейтронов, так что ему нашли применение в атомной энергетике (в качестве «стартёра» для ядерных реакторов)
Не встречается в природе в заметных количествах.
Он является искусственным элементом, который получают в ядерных реакторах или ускорителях частиц.
Чрезвычайно радиоактивен и токсичен. Он является альфа-излучателем, и даже мельчайшие его количества могут быть очень опасны при попадании в организм.
Все работы с калифорнием проводятся в строгих условиях, в герметичных боксах с мощной радиационной защитой.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.