Карбоновые кислоты это органические соединения, которые содержат карбоксильную группу — СООН. Название «карбоксильная» происходит от двух групп: карбонильной — С — О и гидроксильной или оксигруппы — ОН.
Поэтому карбоновые кислоты обладают всеми свойствами альдегидов, кроме способности окисляться, и всеми свойствами спиртов, вернее кислот, так как наличие карбонильной группы делает атом водорода очень подвижным.

Содержание страницы
- 1. Что такое карбоновые кислоты
- 1.1. Карбоновые кислоты
- 1.2. Химические свойства
- 1.3. Муравьиная кислота
- 1.4. Уксусная кислота
- 1.5. Щавелевая кислота
- 1.6. Молочная кислота
- 1.7. Высшие жирные кислоты
- 1.8. Твердые предельные кислоты
- 1.9. Твердые жиры
- 1.10. Сложные эфиры
- 1.11. Быстрые ответы?
Что такое карбоновые кислоты
Карбоновые кислоты могут быть одноосновными (одна карбоксильная группа) и многоосновными (несколько карбоксильных групп).
По рациональной номенклатуре названия кислот связаны с природными объектами, из которых они образовались или выделены (муравьиная, уксусная, пропионовая, масляная и др ).
А по международной номенклатуре название кислоты происходит от названия углеводородов с окончанием — овал (метановая, этановая, пропановая, бутановая и др.).
Простейшие кислоты — жидкости, высокомолекулярные жирные кислоты (стеариновая, пальмитиновая) — твердые вещества, непредельная жирная кислота олеиновая — маслянистая жидкость.
Карбоновые кислоты
Карбоновые кислоты характеризуются присутствием в их молекулах группы атомов
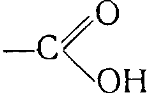
которая является функциональной группой этого класса соединений и носит название карбоксила. Примерами кислот могут служить:
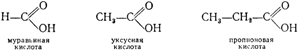
Из приведенных формул видно, что в молекулах карбоновых кислот, как и в молекулах спиртов, содержатся гидроксильные группы, вследствие чего кислоты в некоторых отношениях обнаруживают сходство со спиртами.
Но в кислотах гидроксильная группа находится под влиянием группы атомов:
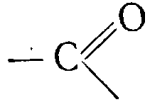
в то время как в спиртах она испытывает влияние углеводородного радикала.
Влияние карбонильной группы на гидроксил сказывается, в частности, в том, что атом водорода гидроксильной группы в кислотах значительно более «кислотен», чем в спиртах.
Легче замещается металлом и может отщепляться в виде катиона, например:
СН3СООН ⇄ СН3СОО’ + Н•
С основаниями эти кислоты образуют соли:
СН3СООН + NaOH =CH3COONa + Н2О
Карбоновые кислоты являются, однако, слабыми кислотами, поэтому их соли подвергаются гидролизу.
В зависимости от числа карбоксильных групп в молекуле, карбоновые кислоты делятся на одноосновные, двухосновные и т. д.
Химические свойства
Карбоновые кислоты реагируют:
2СН3СООН + Са → Са(СН2СОО)2 + Н2,
2СНЗСООН + СаО → Са(СН3СОО)2 + Н2О,
СН3СООН + NaOH → СНзСООNа + Н2О,
2СН3СООН + СаСО3 → Са(СН3СОО)2 + Н2О + СО2.
СН3СООН + НОС2Н5 → СН3СООС2Н5 + Н2О
Муравьиная кислота
Муравьиная кислота НСООН — это бесцветная жидкость с характерным резким запахом. Кипит при 100,5 °С.
Если радикалом общей формулы R—СООН, считать водород, то это кислота, а если радикалом считать оксигруппу, то это альдегид.
В отличие от всех других кислот муравьиная как альдегиде кислота дает реакцию серебряного зеркала:
HСOОН + Ag2O → 2Ag + HOCOOH → 2Ag + CO2 + H2O.
Получают муравьиную кислоту из формиата натрия, который образуется при взаимодействии едкого натра с монооксидом углерода:
СО + NaOH → HCOONa,
HCOONa + H2SO4 → NaHSO4+ НСООН.
В промышленности муравьиную кислоту используют как восстановитель.
Уксусная кислота
Уксусная кислота СН3СООН — это бесцветная жидкость с резким характерным запахом. Она при 118 °C кипит, а при 16,6 °С затвердевает, напоминая лед, поэтому ее называют ледяной.
Была первой кислотой, которая стала известна человеку. Она образуется при брожении вина и при сухой перегонке дерева.
Обладает всеми свойствами кислоты не окислителя.
Уксусная кислоту получают окислением уксусного альдегида и бутана:
2СН3СНО + О2 → 2СН3СООН,
СН3 — СН2 — СН2 — СН3 + 5О2 → 2СН3СООН + 6Н2О.
В промышленности ее получают в больших количествах путем окисления уксусного альдегида, образующегося из ацетилена по реакции Кучерова.
Уксусную кислоту применяют:
1. В производстве пластмасс.
2. Искусственных волокон.
3. Красителей.
4. В пищевой промышленности и т.д.
Щавелевая кислота
НООС—СООН является простейшим представителем двухосновных карбоновых кислот. Это твердое, кристаллическое вещество, легко растворимое в воде.
Содержится во многих растениях (например, в щавеле) в виде кислой калиевой соли. Применяется при крашении тканей.
Двухосновная карбоновая кислота ароматического ряда, имеющая структурную формулу
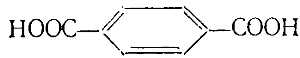
называется терефталевой кислотой.
Из продукта конденсации диметилового эфира этой кислоты с этиленгликолем вырабатывают один из видов синтетического волокна — лавсан.
Молочная кислота
Может служить примером соединения со смешанными функциями, проявляя свойства и кислоты и спирта (спиртокислота).
Она образуется при молочнокислом брожении сахаристых веществ, вызываемом особыми бактериями.
Содержится в кислом молоке, квашеной капусте, силосованных кормах и т. п.
Подобным же соединением в ароматическом ряду является салициловая кислота С6Н4(ОН)СООН.
Уксусный эфир которой — аспирин — широко применяется как жаропонижающее средство.
Высшие жирные кислоты
Высшие жирные кислоты: предельные — стеариновая С17Н35СООН, пальмитиновая С15Н31СООН — и непредельная — олеиновая С17Н33СООН — входят в состав жиров.
Соли этих кислот называются мылами. Твердые мыла — это соли натрия, а жидкие — соли калия. Соли других металлов в воде не растворимы.
При растворении в воде мыла оно практически полностью гидролизует:
С17Н35СООNa + H2O → С17Н35СООН + NaOH.
Образующаяся щелочь создает мылкость раствора, а кислота является хорошим пенообразователем.
Твердые предельные кислоты
Кислоты с большим молекулярным весом, как, например, твердые предельные кислоты:
1. Пальмитиновая С15Н31—СООН.
2. Стеариновая С17Н35 — СООН.
3. Жидкая непредельная олеиновая кислота С17Н33 — СООН.
в виде своих сложных эфиров широко распространены в животных и растительных организмах.
Природные жиры представляют собой смеси сложных эфиров, образованных этими кислотами и глицерином.
Приведем схему образования одного из таких эфиров:
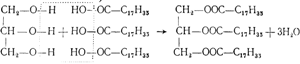
Твердые жиры
В состав твердых жиров входят главным образом эфиры пальмитиновой и стеариновой кислот, а в состав жидких растительных масел — эфиры олеиновой кислоты.
При действии водорода (в присутствии никеля в качестве катализатора) жидкие жиры превращаются в твердые.
В следствие присоединения водорода по месту двойной связи между атомами углерода в этерифицированных молекулах непредельной кислоты.
Как и все сложные эфиры, жиры подвергаются гидролизу (омылению).
Омыление жиров, само по себе медленное, катализируется сильными кислотами, щелочами, окислами металлов или энзимами, образующимися в живых организмах.
При гидролизе жира в нейтральной или кислой среде получаются глицерин и вышеуказанные кислоты, при гидролизе же в щелочной среде вместо свободных кислот получаются их соли, называемые мылами (например, C17H35COONa — натриевое мыло).
В состав некоторых масел, например льняного масла, входят эфиры еще более непредельных кислот, чем олеиновая, в молекулах которых имеется по две и пр три двойных связи.
Такие масла, будучи нанесены на какую-нибудь поверхность, обладают свойством давать на воздухе твердые и прочные пленки.
Они называются высыхающими маслами и применяются для изготовления масляных красок.
Чтобы ускорить процесс высыхания, масла предварительно варят с добавкой окислов металлов-(кобальта, марганца или свинца), являющихся катализаторами в-процессе пленкообразования.
Таким образом получают олифу.
Сложные эфиры
Многие сложные эфиры карбоновых кислот и предельных углеводородов имеют приятный запах и часто встречаются в растениях, придавая аромат цветам, запах плодам и ягодам.
Некоторые из сложных эфиров готовятся искусственно и под названием «фруктовых эссенций» широко применяются в кондитерском деле, производстве фруктовых вод, парфюмерии и т. д.
Уксусно-изоамиловый эфир:
СН3СООС5Н11
(грушевая эссенция) применяется как растворитель целлулоида.
Большое промышленное значение имеют некоторые производные легко полимеризующейся непредельной акриловой кислоты:
СН2 = СН — СООН.
К их числу относится метиловый эфир метакриловой кислоты:
СН2 = С(СН3) —СООСН3.
Полимеры этого эфира тверды, прозрачны, устойчивы по, отношению к нагреванию и действию света.
Из них изготовляют листы прочного и легкого органического стекла, широко применяемого для различных изделий.
Из продукта полимеризации нитрила акриловой кислоты:
СН2 = СН — CN
получают нитрон — синтетическое волокно, заменяющее шерсть.
Быстрые ответы?
Класс органических соединений, молекулы которых содержат одну или несколько функциональных карбоксильных групп COOH.
Кислотные свойства объясняются тем, что данная группа может сравнительно легко отщеплять протоны.
Это производные углеводородов, содержащие в составе молекуле одну или несколько карбоксильных групп.
Существуют также тривиальные названия: метановая – муравьиная, этановая – уксусная, пропановая – пропионовая, бутановая – масляная, пентановая – валериановая и др.
Являются частью природных животных жиров и растительных масел, восков. Карбоновые кислоты используются в пищевой промышленности, в фармации и в органическом синтезе.
Наиболее широко используются уксусная и муравьиная кислота, являющиеся реагентами во многих процессах органического синтеза.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.