Сернистая кислота это сложное неорганическое соединение в состав которого входят: водород Н2, кислород О2 и сера S, ей соответствует химическая формула H2SO3.
Может быть получена из оксида серы (IV) и воды Н2О, это кислота средней силы.
В природе образуется в местах действующих вулканов, производствах связанных с получением серной кислоты, а также на коксохимических предприятиях.
Поэтому участвует в образовании кислотных дождей.
Содержание страницы
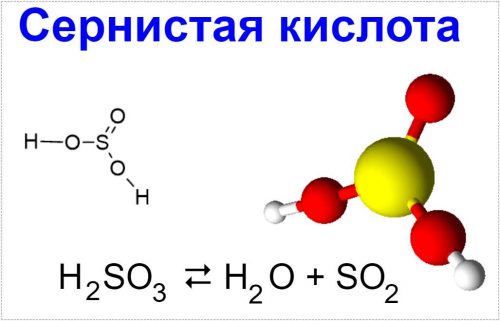
Сернистая кислота: свойства, происхождение и применение
Это двухосная кислота, которая по своим малоустойчивым свойствам практически не существует в чистом виде, а находиться только в водном растворе.
Образуется при взаимодействии диоксида серы SO2 с водой H2O.
Ввиду неустойчивости не может быть выделена в чистом виде из водных растворов.
Химические свойства
Сернистая кислота — весьма малоустойчивое соединение:
H2SO3 ⇄ H2O + SO2.
Она может реагировать:
H2SO3 + СаО = CaSO3 + Н2О,
H2SO3 + 2NaOH = Na2SO3 + 2Н2О,
H2SO3 + I2 + H2O = H2SO4 + 2HI,
H2SO3 + 2H2S = 3S + 3H2O.
Соли сернистой кислоты — сульфиты — широко используются как восстановители в кинофотопромышленности.
AuCl4 + Na2SO3 =
Физиологические свойства
Пары сернистой кислоты обладают аналогичными свойствами воздействия на организм человека, как и ее ангидрид — сернистый газ, за исключением того, что концентрация паров кислоты всегда ниже.
Несмотря на это, она вызывает стойкое раздражение дыхательных путей, не позволяя человеку находиться в атмосфере с высоким содержанием таких пар на протяжении длительного времени.
При постоянном воздействии на человека даже малых концентраций испарений сернистой кислоты, не вызывающих сразу заметного раздражения дыхательных органов.
Могут проявляться катаральные воспаления слизистой оболочки глаз, трудности с дыханием, нарушения пищеварения, что в итоге приводит к общему истощению организма.
Быстрые ответы?
Применяется как восстановитель, для беления шерсти, шелка и других материалов, которые не выдерживают отбеливания с помощью сильных окислителей (хлора).
Легко разлагается на сернистый газ и воду по реакции: H2SO3 ⇄ H2O + SO2.
Её соли и эфиры называются сульфитами и гидросульфитами, которые применяются как восстановители в некоторых реакциях.
Примером может служить восстановление золота сульфитом натрия.
