Хлорид натрия, более известный как поваренная соль, и вода – это два вещества, которые тесно связаны друг с другом.
Заметим, что эта соль хлорид натрия образована сильной кислотой НCl, а вода это растворитель.
Они играют важную роль в жизни человека и окружающей среды.
Реакция хлорид натрия и вода:
NaCl + H2O → раствор где вода растворитель, хлорид натрия растворенная в ней соль.

Содержание страницы
Растворение хлорида натрия в воде
Когда хлорид натрия растворяется в воде, его ионы (Na+ и Cl—) отделяются друг от друга и равномерно распределяются в воде.
Это происходит благодаря полярности молекул воды, которые притягивают ионы соли.
Как написано выше хлорид натрия это соль сильной кислоты (соляная кислота НCl), а соли образованные сильными кислотами или сильными основаниями не подвергаются гидролизу.
Поэтому не происходит не какой либо реакций межу веществами например:
NaCl + H2O ≠ NaOH + HCl
Это происходит потому, что вещество образовано сильной кислотой и в воде этот раствор ведет себя нейтрально.
Но например карбид натрия Na2C2 и оксид натрия Na2О реагируют с водой образуя новые вещества:
Na2C2 + Н2О → 2NaOH + C2H2 гидроксид натрия + ацетилен
Na2О + Н2О → 2NaOH гидроксид натрия
Растворимость
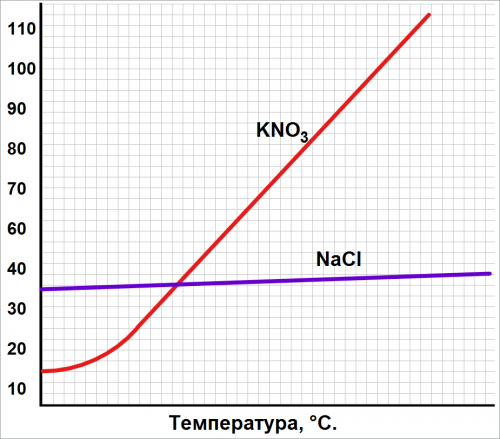
Хлористый натрий (NaCl) легко растворяется в воде, но настает момент когда растворимость прекращается, а нагревание раствора не даёт хороших результатов
Растворимость хлорида натрия в воде при разных температурах:
35,6 г/100 мл (0 °C); 12
35,9 г/100 мл (+25 °C); 12
39,1 г/100 мл (+100 °C).
Упражнение
Рассчитайте какую массу хлорида натрия и какой объем воды надо взять для приготовления 150г 3% раствора.
Для приготовления 150 г 3% раствора хлорида натрия (NaCl) нужно рассчитать массу NaCl и объем воды.
Сначала рассчитаем массу NaCl в растворе. Процентное содержание обозначает, что в 100 г раствора содержится 3 г NaCl.
Для 150 г раствора:
(3 : 100) • 150 = 4.5г
Масса воды в растворе равна общей массе раствора минус масса NaCl:
масса воды = 150г − 4,5г = 145,5г
Поскольку плотность воды примерно равна 1 г/мл, объем воды можно найти следующим образом:
Объем воды = масса воды=145.5мл
Для приготовления 150 г 3% раствора хлорида натрия необходимо взять 4.5 г NaCl и 145.5 мл воды.
Хлорид натрия
Хлорид натрия – это химическое соединение, состоящее из натрия (Na) и хлора (Cl). Это белое кристаллическое вещество, которое легко растворяется в воде.
В природе встречается в виде галита, огромное количество находиться в морской и океанах.
Его присутствие находят в воздухе.
Молярная масса 58,44277 г/моль, Плотность 2,165 г/см3, температура плавления 800,8 °C, кипения 1465 °C.
Вода
Вода – это бесцветная, безвкусная и прозрачная жидкость. Она является универсальным растворителем, что означает, что она может растворять множество веществ, включая хлорид натрия.
Важность
Хлорид натрия и вода играют важную роль в жизни человека и окружающей среды:
Человеческое тело: Хлорид натрия необходим для поддержания водного баланса, регулирования кровяного давления и передачи нервных импульсов.
Вода является основным компонентом человеческого тела, участвуя в различных физиологических процессах.
Растения: Хлорид натрия и вода необходимы для роста и развития растений.
Окружающая среда: Хлорид натрия и вода играют важную роль в гидрологическом цикле и формировании климата.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.