Соли галогеноводородных кислот — это неорганические вещества, которые могут быть получены действием галогеноводородных кислот (HF, НСl, НВr и HI) на соли или щелочи, а также металлы.
Примеры галогеноводородных солей:
- Фториды (NaF).
- Хлориды (NaCl).
- Бромиды (MgBr2).
- Йодиды (AgI).
Некоторые из них встречаются в природе в виде минералов.
Рис. Хлорид бария
Содержание страницы
- 1. Соли соляной кислоты
- 1.1. Хлорид натрия NaCl
- 1.2. Хлорид калия
- 1.3. Хлористый кальций
- 1.4. Хлорид серебра
- 1.5. Хлорид магния
- 1.6. Хлорид кальция
- 1.7. Эксикатор
- 2. Соли фтора
- 3. Соли брома
- 4. Соли йода
Соли соляной кислоты
Хлорид натрия NaCl
Из хлоридов наибольшее значение имеет хлорид натрия, который встречается в природе как в виде каменной соли.
Образовавшейся на месте древних высохших соляных озер, так и в виде самосадочной соли, которая и в настоящее время осаждается в соляных озерах.
Ее образование можно представить формулой:
NaOH + HCl → NaCl + H2O
Поваренная соль кристаллизуется в виде кубических кристаллов, не имеет запаха, обладает соленым вкусом.
Поваренная соль хорошо растворима в воде.
С изменением температуры ее растворимость почти не меняется. Это имеет определенное значение при выделении поваренной соли из растворов других солей методом перекристаллизации.
О применении хлорида натрия можно судить по схеме:
Хлорид натрия → едкий натр → мыло.
Хлорид натрия → едкий натр → шелк.
Хлорид натрия → хлор → хлоруксусная кислота.
Хлорид натрия → хлор → хлорная известь.
Хлорид натрия → хлор → фосген.
Хлорид натрия → соляная кислота.
Хлорид натрия → бисульфат натрия.
Хлорид натрия → сода → бура.
Хлорид натрия → сода → жидкое стекло.
Хлорид натрия → сода → магнезия.
Хлорид натрия → сода → ультрамарин.
▷ Запишите в тетрадь области применения поваренной соли.
Хлорид калия
Хлорид калия КСl. В природе он встречается в виде минерала сильвина КСl или сильвинита KCl-NaCl.
Хлорид калия применяется в сельском хозяйстве в качестве удобрения. До 1930 г. хлорид калия ввозился в нашу страну из-за границы.
Благодаря исследованиям акад. Н. С. Курнакова около Соликамска найдено громадное месторождение хлорида калия.
Хлористый кальций
Хлористый кальций хорошо растворяется в воде. В твердом виде — вещество кристаллическое.
Хлорид бария ВаСl2 ядовит.
Он широко применяется для борьбы с вредителями сельского хозяйства, а также в качестве реактива на серную кислоту и ее соли.
Хлорид серебра
Хлорид серебра AgCl — творожистое белое вещество. Под действием света постепенно темнеет, разлагаясь с выделением металлического серебра.
Хлорид магния
Хлорид магния MgCl2—единственная соль, из которой в промышленности получают металлический магний.
Хлорид кальция
Хлорид кальция СаСl2 — соль, содержащаяся в морской воде, но чаще всего получаемая искусственным путем.
Интересным свойством хлорида кальция является его высокая гигроскопичность. Хлорид кальция энергично поглощает воду, поэтому его применяют в эксикаторах.
Эксикатор
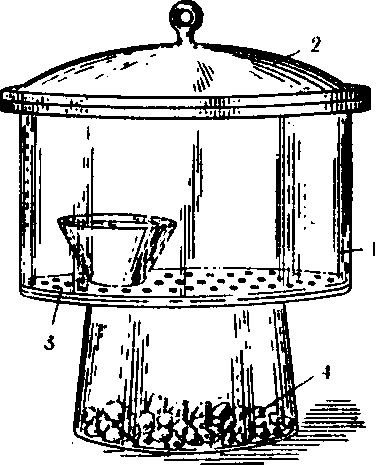
Рис. 2. Эксикатор. 1-резервуар; 2 -притертая крышка; 3- фарфоровая решетка; 4 — хлорид кальция.
Эксикатор служит для хранения веществ, которые необходимо предохранить от увлажнения парами воды, всегда присутствующими в воздухе.
Это стеклянный сосуд, состоящий из двух частей, разделенных фарфоровой решеткой 3.
В нижнюю часть сосуда 4 помещают хлористый кальций, концентрированную серную кислоту или другое вещество, энергично поглощающее воду.
В верхнюю часть сосуда 1 на решетку 3 помещают чашку или тигель с высушиваемым веществом.
Сверху эксикатор закрывают толстой стеклянной крышкой 2 с притертой поверхностью.
Соли фтора
Фторид натрия NaF довольно широко применяется в борьбе с грызунами и с некоторыми насекомыми-вредителями, а также для предохранения древесины от гниения.
Фторидом натрия пропитывают шпалы, телеграфные столбы, строительные деревянные детали для удлинения срока их службы.
Плавиковый шпат, или флюорит, CaF, — наиболее распространенное соединение фтора, из которого получают все фтористые соединения и свободный фтор.
Плавиковый шпат иногда встречается в виде правильных кристаллов с очень ценными оптическими свойствами.
Из них изготовляют линзы, различные оптические приборы. Такие линзы приходится оберегать от толчков, так как они очень хрупкие.
Соли брома
Из солей брома следует прежде всего отметить бромид магния MgBr2, который в природе сопровождает поваренную соль, а также хлорид калия.
После извлечения поваренной соли из воды соляных озер в рассоле остается значительный процент бромида магния.
Бромид магния встречается и в морской воде, но в очень небольших количествах, невыгодных для его промышленного получения.
Большое применение соли брома, главным образом бромиды натрия и калия, находят в медицине.
Бромиды сильно понижают возбудимость нервной системы. Но лечение бромистыми препаратами допустимо только при здоровых почках, иначе вследствие задержки выведения бромидов из организма может наступить отравление.
Продолжительное лечение бромидами также не рекомендуется.
Бромид серебра AgBr обладает способностью легко разлагаться на свету с выделением металлического серебра в виде черной массы
2AgBr = 2Ag + Вr2.
Это свойство AgBr широко используется в фотографии.
Соли йода
Йодид серебра окрашен в желтый цвет, и, так же как хлорид и бромид серебра, он нерастворим в кислотах.
Реактивом на анионы Сl—, Br—, I— в кислотах и солях является катион Ag+, который даете этими анионами нерастворимые в воде и кислотах, по-разному окрашенные осадки:
AgCl — белый, AgBr — желтоватый, быстро темнеющий, AgI — желтый.
Анион F- таким образом открыть нельзя, так как AgF — соль растворимая.
▷Выпишите в тетрадь формулы и названия всех приведенных в тексте солей галогенов, дайте им названия и постарайтесь возможно полнее перечислить, где они применяются.
➡️ 30. Каким образом из раствора иодида натрия можно удалить примесь свободного иода?
31. Йодкрахмальная бумага пропитана растворами крахмала и иодида калия. Почему при попадании в хлорную воду она синеет?
32. В пробирки налили растворы: в одну — хлорид натрия, в другую — бромид калия, в третью — иодид калия, в четвертую — фторид натрия. Как определить, в какой пробирке какая соль?
33. Соль, образовавшуюся при взаимодействии 20 г гидроксида магния и 20 л бромистого водорода, растворили в 40 мл воды. Какой процентной концентрации получился раствор. (См. Ответ)


Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.