Модель электронного облака — это современное представление о распределении электронов вокруг атомного ядра.
В отличие от классической модели, которая описывает электроны как частицы, движущиеся по определённым орбитам, современная модель электронного облака основывается на принципах квантовой механики.
Согласно этой модели, электроны находятся в состоянии вероятности, и их позиция описывается густотой вероятности, что создаёт изображение «облака» вокруг ядра.
Основное преимущество данной модели заключается в её способности объяснять такие феномены, как химическая связь и поведение веществ в различных состояниях.
Электронное облако иллюстрирует, как электроны могут находиться в разных энергетических состояниях и как они взаимодействуют друг с другом и с ядром атома.
Рис. Местонахождения 1 s-электрона в атоме водорода с помощью облака точек.
Модель электронного облака
В 1927 г. немецкий физик Вернер Карл Гейзенберг показал, что вследствие двойственной корпускулярно-волновой природы материи невозможно одновременно с одинаковой точностью определить положение электрона в пространстве и его скорость или количество движения mυ.
Математически этот принцип неопределенности записывается в виде:
∆x • ∆Px≥h,
где:
- ∆х — неопределенность положения электрона в пространстве.
- ∆Рх— неопределенность в определении его импульса.
- h — постоянная Планка.
Из этого соотношения следует, что если достаточно точно определить скорость движения электрона (а значит, и его кинетическую энергию).
То его положение в пространстве останется неопределенным и наоборот.
Поэтому понятие точного местонахождения электрона в атомном пространстве необходимо заменить понятием вероятности его нахождения в элементе объема ∆V.
Мы должны оперировать такими величинами, как среднее и наиболее вероятное расстояние электрона от ядра, средняя скорость его движения в атоме и т. д.
Чтобы показать геометрическое распределение электронов в атомном пространстве, можно воспользоваться моделью (электронного облака).
Представим себе вначале электронное строение простейшего атома — атома водорода.
В поле положительно заряженного ядра с огромной скоростью движется электрон, проявляя одновременно свойства частицы и волны.
Вероятность нахождения электрона в каждом элементе ∆V атомного пространства неодинакова.
Поэтому местонахождение электрона в атоме можно условно изобразить в виде облака точек (рис. 1).
Большая или меньшая плотность этого облака означает соответственно большую или меньшую вероятность нахождения электрона в данной области пространства.
Для атома водорода вероятность нахождения электрона быстро уменьшается с увеличением расстояния от ядра.
Однако в нуль она теоретически никогда не обращается.
Из этого, конечно, не следует, что атом необходимо рассматривать как частицу бесконечно большого размера.
Можно выделить такую область атомного пространства, в которой вероятность нахождения электрона будет достаточно большой, например 90, 95 или 99% .
Эту область назовем электронным облаком и будем считать, что за ее пределами электронная плотность равна нулю.
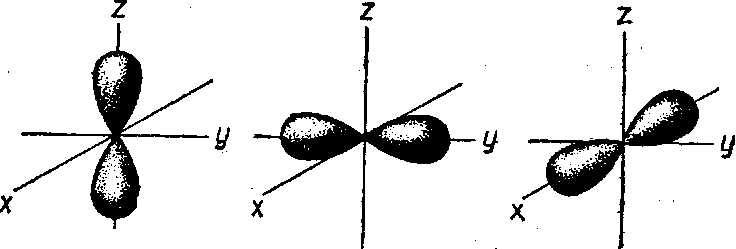
Рис. 3. р— Электронные облака
Геометрическая форма электронного облака зависит от значения орбитального квантового числа lп.
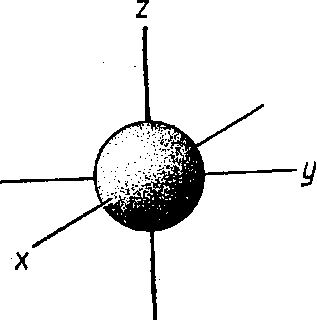
А его ориентировка в пространстве — от значений магнитного квантового числа ml;. s-Электронное облако (l = 0) сферически симметрично; его можно изобразить в виде шара (рис. 2).
Электронные облака р—электронов (l = 1) имеют гантелеобразную форму и направлены вдоль координатных осей х, у и z (рис. 3).
При дальнейшем увеличении орбитального квантового числа геометрическая форма электронных облаков сильно усложняется.
Статья на тему модель электронного облака


Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.