Рис. Образования двухатомных молекул HF
Содержание страницы
Направленность ковалентной связи это
Чем больше степень перекрывания электронных облаков, тем выше энергия химической связи.
Чтобы это перекрывание было максимальным, оно должно происходить в направлении наибольшей электронной плотности.
Например, при образовании двухатомных молекул HF перекрывание s-электронного облака атома водорода и р-электронного облака атома фтора осуществляется вдоль оси р-облака.
В соответствии с тем же принципом происходит образование химических связей и в многоатомных молекулах рис.
Пример образования молекулы воды H2О
Рассмотрим в качестве примера схему образования молекул воды из отдельных атомов.
Конфигурация внешнего квантового слоя атома кислорода 2s2p4.
Из распределения электронов по квантовым ячейкам видно, что валентными в атоме кислорода являются два не спаренных р— электрона.
Один из трех р— подуровней (орбиталей) (пусть это будет рz-подуровень) занят парой электронов с противоположными спинами.
Тогда рх— и рy-подуровни, очевидно, заняты не спаренными электронами.
Отсюда следует, что угол между связями О—Н в молекуле воды должен составлять 90°. В действительности же он равен 104°34′.
Такое расхождение между предполагаемым и экспериментальным значениями валентного угла объясняется взаимным отталкиванием атомов водорода.
Которое проявляется тем сильнее, чем ближе друг к другу они расположены в пространстве.
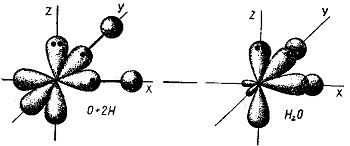
Рис. 3. Образование молекулы воды.
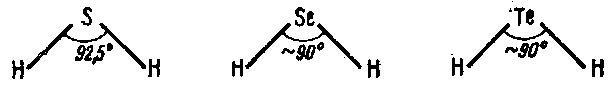
Поэтому в молекулах H2S, H2Se и Н2Те (радиусы центральных атомов в этом ряду возрастают) углы между связями последовательно снижаются, приближаясь к теоретическому смотрим рис. 2.
Аналогичное рассмотрение схемы образования молекул аммиака NH3 приводит к заключению, что они имеют пирамидальную форму, а углы между связями N—Н равны 90°. На самом же деле вследствие взаимного отталкивания атомов водорода эти углы, близки к 107° .
Вывод
Направленность ковалентной связи и ее особенностях в молекулах демонстрирует ключевую роль перекрывания электронных облаков для формирования устойчивых химических соединений.
Максимальное перекрытие происходит в направлении повышенной электронной плотности, что позволяет эффективно образовывать связи между атомами.
Приведенные примеры, такие как вода и аммиак, иллюстрируют, как взаимодействия и расположение электронов влияют на геометрию молекул.
Несмотря на теоретические предположения о валентных углах, на практике наблюдаются отклонения, объясняемые взаимным отталкиванием атомов.
Это подчеркивает важность учета пространственного расположения атомов и их радиусов для понимания молекулярной геометрии.
Сравнение углов в различных молекулах, таких как H2O и NH3, демонстрирует, как рост атомных радиусов меняет углы между связями.
Статья на тему Направленность ковалентной связи

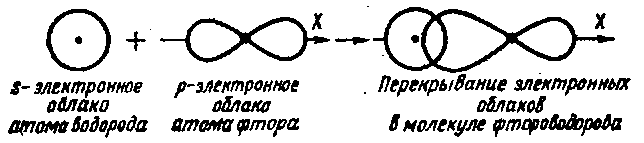
Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.