Изменение свойств атомов в зависимости от строения их оболочек является ключевым аспектом в химии и физике.
Атомы состоят из ядра и оболочек, представляющих собой уровни энергии, на которых находятся электроны.
Структура этих оболочек определяет химические и физические свойства элементов.
Первый уровень оболочки может содержать только два электрона, второй — восемь, и так далее, что создает определенные закономерности в химической активности.
Например, элементы с полностью заполненными наружными оболочками, такие как инертные (газы), имеют низкую реакционную способность.
В то же время, металлы обычно имеют один или два электрона на внешнем уровне, что делает их более склонными к отдаче электронов и образованию ионов.
Изменение свойств атомов в зависимости от строения их оболочек
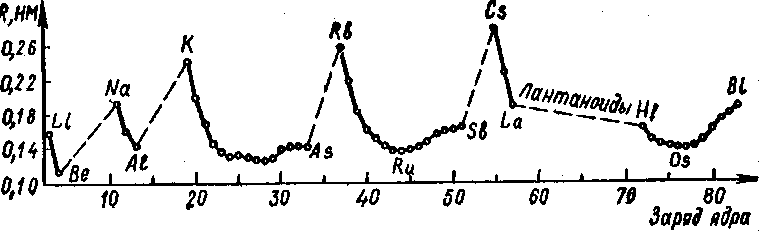
Рис. Атомные радиусы металлов.
Из рассмотренных электронных конфигураций атомов элементов первых трех периодов наглядно прослеживается периодичность в изменении свойств элементов, открытая Д. И. Менделеевым.
Каждый период начинается элементом, в атомах которого застраивается новый энергетический уровень, причем главное квантовое число n для этого уровня равно номеру периода.
В конце каждого периода стоит химический инертный элемент, имеющим на внешнем уровне восемь электронов (в случае гелия— два электрона).
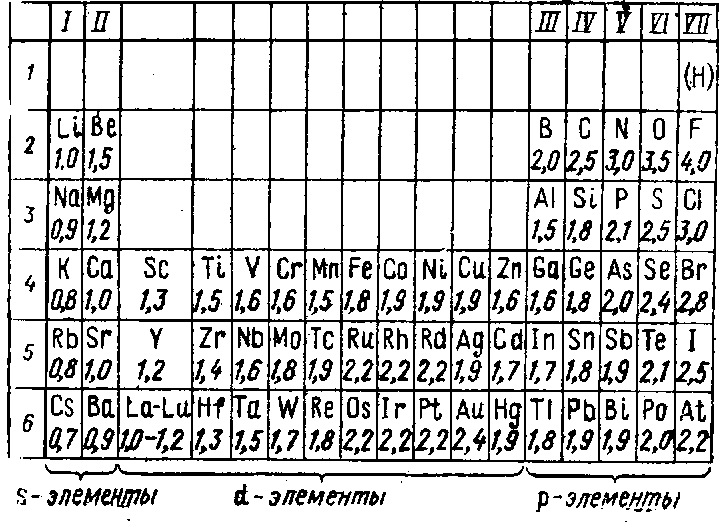
Элементы, атомы которых обладают сходными электронными оболочками, попадают в определенную группу периодической системы.
Например, щелочные металлы (конфигурация ns1) попадают в первую группу, а инертные газы, имеющие завершенный энергетический уровень (ns2p6),— в восьмую группу.
В зависимости от строения электронных оболочек атомов все химические элементы можно разбить на четыре основных семейства:
s-, р-, d-, f-элементы.
Эта классификация основана на том, в какой степени заполнены соответствующие s-, р-, d— и f— подуровни.
Следует, однако, и метить, что периодическое чередование d— и f-элементов в седьмом периоде нарушается.
Поэтому размещение в периодической системе элементов, следующих за актинием (актиноидов), представляет большую трудность.
Содержание страницы
Радиус атомов
Поскольку электроны находятся в непрерывном движении и изменяют форму своих орбит, точно определить размер атома невозможно.
Это обусловлено также и тем, что на распределение электронов в атоме оказывает большое влияние внешнее окружение.
Размер атома не является некоторой постоянной и абсолютной величиной; он может слегка изменяться, например, в зависимости от соединения, в которое входит данный атом.
Тем не менее различные физические методы позволяю определить расстояние, разделяющее центры двух сосед них одинаковых частиц, и рассчитать так называемый «атомный радиус».
Атомные радиусы являются периодической функцией порядкового номера элемента. Это отчетливо видно из рисунках.
В пределах одного периода атомные радиусы уменьшаются слева направо, что обусловлено возрастанием положительного заряда ядер.
Появление нового электронного слоя в атомах элементов следующего периода резко увеличивает их размер, поэтому в группах периодической системы атомные радиусы увеличиваются сверху вниз.
Энергии ионизации атомов
Поглотив из вне определенное количество энергии нейтральный атом теряет свой электрон и превращаете в положительно заряженный ион.
Например:
Li → Li++ē,
К → К+ + ē.
Этот процесс можно рассматривать как переход электрона с энергетического уровня, для которого главное квантовое число равно ni, на уровень с п = п∞.
Энергия, необходимая для отрыва электрона, называется энергией ионизации. Она выражается в кдж/моль или электрон вольтах (1 эв = 96,43 кдж/моль).
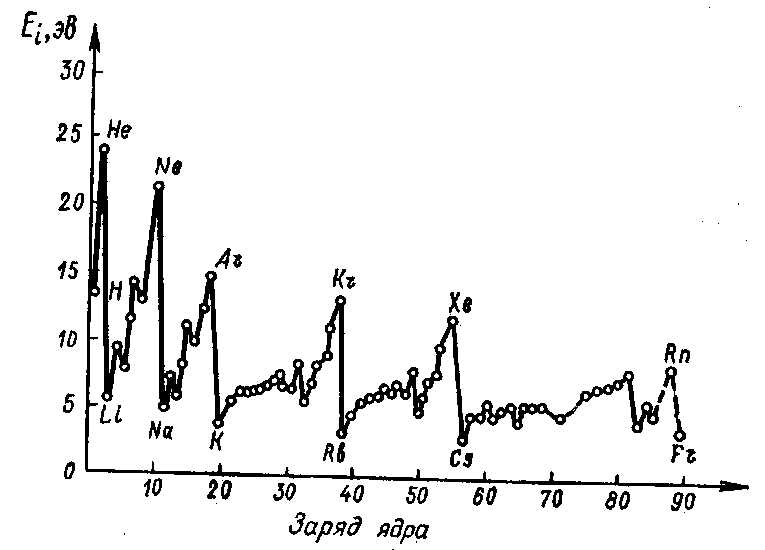
Рис. 2. Энергии ионизации атомов элементов от водорода до франция.
На величину энергии ионизации оказывают влияние многие факторы, главными из которых являются заряд ядра Z, атомный радиус R, общее число квантовых слоев п, степень застроенности данного энергетического подуровня.
Например, увеличение Z приводит к упрочнению связи электрона с ядром, а с возрастанием R эта связь ослаблястся.
На рисунке 2 приведена кривая зависимости энергий ионизации от порядковых номеров элементов. Видна четко выраженная периодичность в изменении этих энергий.
Минимумы на кривой соответствуют щелочным металлам, атомы которых имеют на внешнем уровне один электрон, расположенный на большом расстоянии от ядра.
При переходе от элемента к элементу в пределах одного периода наблюдается постепенное увеличение энергий ионизации, вызываемое ростом зарядов ядер атомов при одновременном уменьшении их радиусов.
Наименьшим значением энергии ионизации обладают в каждом периоде атомы благородных газов, имеющие на внешнем уровне два (гелий) или восемь электронов.
Повышенное значение энергии ионизации наблюдается также у атомов с полностью или наполовину заполненными подуровнями.
Проследим в качестве примера за изменением энергий ионизации атомов элементов второго периода.
Энергия ионизации лития имеет наименьшее значение — 5,4 эв (один s-электрон на внешнем уровне).
Далее следует резкий подъем: Е1 бериллия составляет уже 9,3 эв (s-подуровень полностью заполнен).
В атоме бора появляется один не спаренный р-электрон, что сопровождается незначительным снижением энергии ионизации (8,3 эв).
При переходе к углероду (11,3 эв) она вновь возрастает за счет увеличения общего числа не спаренных электронов.
В атоме азота р— подуровень заполнен наполовину, это приводит к дальнейшему росту энергии ионизации.
Следующий электрон, поступающий на р— подуровень атома кислорода, снижает его устойчивость, что сопровождается незначительным понижением на кривой.
Однако при переходе ко фтору энергия ионизации вновь увеличивается и достигает наибольшего значения для неона в связи с завершением наружного энергетического уровня.
Сродство к электрону
Энергия, выделяющаяся при присоединении электрона к нейтральному изолированному атому, находящемуся в нормальном (невозбужденном) состоянии, называется энергией сродства к электрону или просто сродством к электрону и обозначается значком Ес.
Сродство к электрону экспериментально определить гораздо труднее, чем энергию ионизации.
Поэтому величины Ес определены лишь для небольшого числа элементов.
У первых элементов (первого периода) оно очень мало, но постепенно увеличивается и достигает максимума у р — элементов седьмой группы.
Наибольшим сродством к электрону обладают атомы галогенов и халькогенов.
Это подтверждается на практике тем, что галогены и кислород легче других элементов образуют отрицательно заряженные ионы.
Для атомов элементов одной группы сродство к электрону понижается с ростом заряда ядра.
Это объясняется увеличением радиусов, вследствие уменьшения энергии связи внешних электронов с ядром.
Следует отметить, что присоединение электронов к атомам с малыми радиусами создает в подуровнях очень высокую плотность отрицательного заряда, снижающую общую устойчивость отрицательного иона.
Только этим можно объяснить меньшие значения сродства к электрону для элементов второго периода по сравнению с элементами третьего периода.
Способность атомов превращаться в отрицательные ионы очень хорошо характеризует полусумма:
(Ei+Ec)/2
называемая также электроотрицательностью.
В пределах каждого периода электроотрицательность увеличивается с ростом порядкового номера, достигая максимума у р— элементов седьмой группы.
Внутри каждой группы с увеличением порядкового номера происходит возрастание радиусов атомов, что сопровождается снижением электроотрицательности рис. выше.
Статья на тему Изменение свойств атомов

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.