Дативная связь: примеры объяснения
Эти результаты невозможно объяснить на основе представления о ковалентной, ионной или обычной донорно-акцепторной связи.
Действительно, прочность химической связи между одинаковыми атомами, если она осуществляется по одному и тому же механизму (в данном случае за счет не спаренных р— электронов наружного слоя).
Должна последовательно уменьшаться с увеличением радиусов атомов, т. е. в ряду:
F2 → Cl2 → Br2 →I2
Именно так и изменялась бы прочность связи, если бы взаимодействие между атомами хлора, брома и иода в молекулах Сl2, Вr2, I2 происходило только за счет перекрывания р— электронных облаков наружного слоя.
Однако в атомах Cl, Br, I имеются свободные d-подуровни, на которые частично переходят наружные s— и р— электроны.
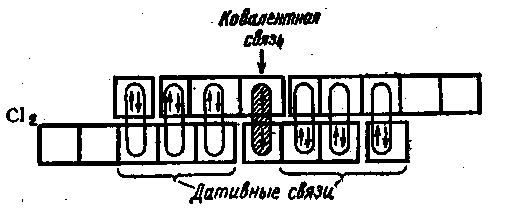
Образующиеся при этом дополнительные химические связи называются дативными. Их возникновение можно показать с помощью следующей схемы смотрим рис. 1.
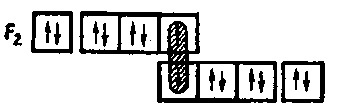
В атомах фтора нет свободных d-подуровней, поэтому связь F—F осуществляется только за счет перекрывания р— электронных облаков:

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.