Теория:
Степень окисления хрома (Cr) в наиболее устойчивых соединениях равна +3 и +6, а также 0, +2. (СО +4 и +5 встречаются редко и неустойчивы).
Это определяется его положением в периодической системе: хром — элемент 6‑й группы (побочная подгруппа), 4‑го периода.
Как переходный металл, он имеет шесть валентных электронов. Особенность хрома — «провал» электрона: один электрон с 4s-подуровня переходит на 3d, образуя конфигурацию 3d54s1.
В отличие от хрома, для многих других элементов положение в таблице даёт лишь базовую информацию о степенях окисления.
Чтобы определить все возможные значения, используют электронную формулу.
Например:
- Для кремния (1s22s22p63s23p2) формула объясняет наличие четырех валентных электронов и возможность проявлять СО от -4 до +4;
- Для марганца (1s22s22p63s23p63d54s2) — возможность достижения высшей степени окисления +7 за счёт участия всех семи валентных электронов.
Хром наиболее стабилен в степенях окисления +3 (самая химически устойчивая) и +6 (высшая, соответствующая номеру группы).
![Степень окисления хрома на примерах Схема: степени окисления хрома (Cr) = 0, +1+2, +3, +4, +5, +6. Свойства (Cr): 6-я группа, электронная формула Cr [Ar] 3d⁵ 4s¹, электроотрицательность 1,66.](https://znaesh-kak.com/wp-content/uploads/2026/03/stepen-okisleniya-khroma.jpg)
Рис. Степень окисления хрома 0, +2, +3, +6, а также не стабильные +1, +4, +5. Факторы, влияющие на СО — наличие пяти d-электронов и одного s-электрона вследствие «провала».
Содержание страницы
- 1. Почему у хрома переменные степени окисления?
- 2. Степень окисления хрома в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Как определить степень окисления хрома
- 3.1. По таблице Менделеева
- 3.2. По электронной конфигурации
- 3.3. По валентности (Число связей)
- 3.4. По электроотрицательности
- 3.5. По химическому соединению (Алгебраический расчет)
- 4. Примеры степеней окисления хрома
- 5. Шпаргалка для определения степени окисления хрома
- 6. Пример решения задачи:
- 7. Проверка знаний
- 8. Часто задаваемые вопросы
Почему у хрома переменные степени окисления?
Причина — наличие шести валентных электронов на 3d и 4s подуровнях и их ступенчатая отдача.
- В простом веществе (Cr⁰): Все 6 электронов на месте. Заряд равен 0.
3d [↑][↑][↑][↑][↑] 4s [↑]. - В соединениях (Cr+6): Хром отдаёт все 6 электронов, достигая конфигурации аргона.
3d [ ][ ][ ][ ][ ] 4s [ ].
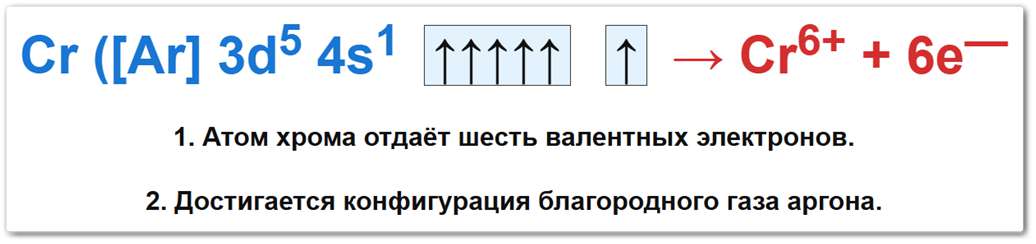
Рис. 2 Схема окисления атома хрома: атом Cr ([Ar] 3d5 4s1) последовательно теряет электроны до высшего состояния +6.
Степень окисления хрома в соединениях
Соединения хрома резко меняют свойства в зависимости от СО: от основных (Cr+2) до амфотерных (Cr+3) и кислотных (Cr+6).
- Оксид хрома(VI) (CrO3): Cr +6, O -2. (Кислотный)
- Дихромат калия (K2Cr2O7): Cr +6, O -2. (Оранжевый)
- Оксид хрома(III) (Cr2O3): Cr +3, O -2. (Зеленый, амфотерный)
- Хлорид хрома(II) (CrCl2): Cr +2, Cl -1. (Синий, восстановитель)
Высшая степень окисления
Высшая СО хрома равна +6 (номер группы). Соединения Cr(+6) — сильнейшие окислители.
Низшая степень окисления
Низшая равна 0 (металлический хром).
Промежуточные степени окисления
- +2 — сильный восстановитель, быстро окисляется на воздухе.
- +3 — самая устойчивая форма. В этой СО хром находится в большинстве минералов.
Как определить степень окисления хрома
По таблице Менделеева
По электронной конфигурации
- Электронная формула хрома: [Ar] 3d5 4s1, подробнее о квантовых числах → [таблица].
- Сначала уходит 1 электрон с 4s-уровня и 1 с 3d (СО +2), затем еще один (+3), и при полной потере всех 6 электронов — высшая СО +6.
По валентности (Число связей)
Валентность хрома в высших соединениях равна VI. Это означает образование шести химических связей.
- В хроматах (CrO42-) атом хрома образует связи, эквивалентные валентности VI.
По электроотрицательности
Степень окисления хрома зависит от того, какой элемент сильнее притягивает электроны. Сравните значения в таблице электроотрицательности.
- Выпишите известные степени (у Кислорода -2, у Металлов I-II групп +1/+2).
- Умножьте заряды на количество атомов.
- Найдите неизвестное X для Хрома так, чтобы сумма всей молекулы стала равной 0.
Пример: в соединении CrO3 кислород (ЭО 3.44) сильнее Хрома (ЭО 1.66), поэтому забирает все 6 электронов, делая хром Cr+6.
По химическому соединению (Алгебраический расчет)
Пример для K2CrO4 (хромат калия): Калий всегда +1, кислород -2. Сумма = 0.
2 · (+1) + x + 4 · (-2) = 0 → 2 + x — 8 = 0 ⇒ x = +6.
Примеры степеней окисления хрома
| СО | Характер свойств | Цвет | Примеры |
|---|---|---|---|
| +6 | Кислотный, окислитель | Оранжевый/Желтый | CrO3, K2Cr2O7 |
| +3 | Амфотерный, устойчивый | Темно-зеленый | Cr2O3, CrCl3 |
| +2 | Основный, восстановитель | Небесно-синий | CrO, CrCl2 |
Шпаргалка для определения степени окисления хрома
Представьте хром как кошелёк, где 6 монет (4s1 3d5). Одна лежит в кармашке (s), пять — в основном отделении (d).
- 0 — «кошелёк полный» (металл Cr).
- +2 — «потеряли s-монету и одну d-монету» (нестабильно, хочет отдать еще).
- +3 — «самый экономный баланс» (наиболее стабильное состояние).
- +6 — «пустой кошелёк» (отдали всё, конфигурация аргона).
Пример решения задачи:
▶️ Дано:
Соединение: K2Cr2O7.
⌕ Найти:
Определите СО хрома.
✨ Решение:
K (+1), O (-2). Расчет: 2·(+1) + 2x + 7·(-2) = 0 → 2 + 2x — 14 = 0 → 2x = 12 → x = +6.
✅ Ответ:
Cr(+6).
Проверка знаний
Отметьте три правильных утверждения для Хрома (Cr):
Показать верные ответы
Правильные ответы: 1, 3, 4 (2 — неверно из-за провала электрона, 5 — хром это металл).
Часто задаваемые вопросы
Нет, хром — металл с низкой электроотрицательностью, он только отдает электроны.
Хром проявляет много состояний, но «рабочими» и стабильными являются три:
+2: проявляет основные свойства (например, Cr+2O — оксид хрома II).
+3: самая устойчивая форма, амфотерная (оксид Cr2+3O3 зеленого цвета).
+6: высшая степень, проявляет сильные кислотные свойства (ангидрид Cr+6O3 и дихроматы).
Это связано с его способностью легко менять степень окисления в зависимости от среды. В кислой среде оранжевый дихромат (Cr+6) легко превращается в зеленый сульфат хрома (Cr+3).
Этот переход — классика задач на ОВР (окислительно-восстановительные реакции), где хром выступает мощнейшим окислителем.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.