
Содержание страницы
- 1. Переход нейтральных атомов в ионное состояние
- 1.1. Переход нейтральных атомов в состояние положительно заряженных ионов
- 1.2. Переход нейтральных атомов в состояние отрицательно заряженных ионов
- 1.3. Изменение числа электронов в наружном квантовом слое атомов в процессе реакций окисления-восстановления
Переход нейтральных атомов в ионное состояние
При обычных химических реакциях атомное ядро остаётся без изменения. Большинство физико-химических свойств связано с электронной оболочкой, при этом решающую роль играет внешний слой оболочки атома.
Имеется глубокая внутренняя связь между строением внешнего слоя оболочки атома и его химическими свойствами.
Зависимость свойств атомов и ионов от второго и третьего снаружи слоев оболочки атома сказывается значительно слабее, а от ещё глубже лежащих слоев сводится почти к нулю.
Электроны наружного слоя (а иногда 2-го и 3-го, считая снаружи) называют валентными.
Валентные электроны наиболее удалены от ядра и наименее прочно связаны с ним. При химических реакциях они легче всего подвергаются внешним воздействиям.
Состав внешнего электронного слоя элементов в периодической системе по мере возрастания порядкового номера изменяется периодически.
В зависимости от этого и химические свойства элементов изменяются периодически.
У элементов, атомы которых имеют сходные электронные структуры и одинаковое число электронов на внешнем слое, химические свойства оказываются очень близкими, хотя общее число электронов и заряд ядра у них различны.
Рис. Структура мицеллы As2S3
По способу заполнения электронных слоев элементы делятся на следующие группы:
а) Элементы, у которых наружный слой оболочки атомов пополняется. Все внутренние слои оболочки атомов у них заполнены электронами. Таких атомов преобладающее количество).
б) Элементы, в оболочке атома которых происходит заполнение электронного слоя соседнего с наружным. Наружный слой у таких атомов имеет два или реже один электрон.
в) Элементы, у которых происходит заполнение ещё более глубокого слоя, считая от внешнего.
На наружном слое они имеют два электрона, а на втором снаружи девять. К этой группе относятся лантаноиды и актиноиды.
В малых периодах периодической системы по мере возрастания порядкового номера число электронов на внешнем слое непрерывно увеличивается.
В связи с этим металлические свойства — способность к отдаче внешних электронов — ослабляется, а неметаллические свойства — способность к принятию внешних электронов — увеличивается.
Каждый период периодической системы начинается с типичного металла (сильного восстановителя) и заканчивается типичным неметаллом (сильным окислителем).
В больших периодах способность к отдаче и принятию электронов в общем происходит так же, как и в малых периодах, с той лишь разницей, что металлические свойства ослабевают гораздо медленнее.
Объясняется это тем, что в больших периодах (например, четвёртом), начиная со скандия (порядковый номер 21) и вплоть до конца первой его половины (элемент Ni), происходит пополнение электронами не последнего электронного слоя, а предпоследнего.
У лантаноидов же, расположенных в шестом периоде, пополняется даже третий электронный слой, считая от внешнего.
Поэтому в четвёртом периоде все элементы первой половины периода имеют в наружном электронном слое два, реже один электрон, и характеризуются преобладанием металлических свойств.
В элементах второй половины четвёртого периода (начиная с Сu и кончая Вr) число электронов на внешнем слое растёт постепенно, как и в малых периодах.
И следовательно, металлические свойства постепенно ослабляются, неметаллические усиливаются.
В пределах главных подгрупп по мере увеличения порядкового номера элемента число электронных слоев оболочки атомов возрастает, внешние электроны постепенно от ядра удаляются.
А потому способность их в реакциях переходить к другим атомам, как правило, усиливается, а способность присоединять к себе электроны других атомов ослабляется.
При столкновении или при сближении нейтральных атомов различных элементов один атом принимает электроны, другой их отдаёт.
Атом, отдающий электроны, переходит в состояние положительно заряженного иона, атом же, принимающий электроны, в свою очередь, переходит в состояние отрицательно заряженного иона.
Например:
Переход нейтральных атомов в состояние положительно заряженных ионов
В наружном электронном слое атомов различных элементов находится от одного до восьми электронов. Эти электроны могут быть перетянуты атомом другого элемента полностью или частично.
Чем меньше ионизационный потенциал, тем атом легче теряет свои электроны и переходит в состояние положительно заряженного иона.
Положительно заряженные ионы образуют атомы всех элементов, за исключением инертных газов (В искусственно созданных условиях инертные газы также могут образовать положительно заряженные ионы (например, в разрядной трубке) и фтора.
Если наружный слой оболочки атома состоит из одного электрона и атом по заполнению электронных слоев относится к группе а).
То у него теряется, как правило, только один электрон, и он переходит в состояние однозарядного положительного иона.
Так, группа щелочных металлов образует только одно заряженные ионы:
Li+1, Na+1, K+1, Rb + 1, Cs+1, Fr+1.
Если наружный электронный слой оболочки атома состоит из двух электронов и атом относится к группе а), то, как правило, от них отрываются сразу два электрона и получается двух зарядный положительный ион.
Так, атомы 2-й группы периодической системы элементов Менделеева (четный ряд) образуют ионы только положительно двух зарядные:
Ве+2, Mg+2 Са+2, Sr+2, Ва+2, Ra+2.
Если наружный электронный слой атома состоит из трёх, пяти или семи, т. е. нечётного числа электронов, то он может терять последовательно от одного до семи электронов.
Атомы, внешний электронный слой которых состоит из трёх электронов, как правило, образуют одно-, двух- и трёх-положительно валентные ионы.
Так, алюминий образует только ион Аl+3, индий — ионы In+1, In+2, In+3, таллий — ионы Tl+1 и Тl+3.
Атомы, внешний электронный слой которых состоит из пяти электронов, как, например, азот, образуют несколько положительных ионов:
N+2, N+3, N+4, N+5.
Аналогично ведёт себя фосфор: Р+1, Р+3, Р+4, Р+5.
Атом хлора, внешний электронный слой которого состоит из семи электронов, образует ионы:
Сl+1, Сl+3, Сl+4, Сl+6, Сl+7.
Если наружный электронный слой атомов состоит из четырёх, шести или восьми, т. е. из чётного числа электронов, то от них электроны отрываются парами.
Например, олово, внешний электронный слой которого состоит из четырёх электронов, образует ионы:
Sn+2, Sn+4;
Сера, имеющая внешний электронный слой из шести электронов, образует ионы:
S+2, S+4, S+6.
Элементы, у атомов которых пополняется электронный слой, соседний с наружным, в первую очередь отрываются электроны наружного слоя.
Затем начинают отрываться электроны от соседнего с наружным слоем, который теперь уже стал наружным, — это происходит до тех пор, пока в нём не остаётся восьми электронов.
Так, например, марганец, максимальная валентность которого + 7, образует ионы:
Мn+2, Мn+3, Мn+4, Мn+6, Мn+7;
Осмий, максимальная валентность которого +8, образует ионы:
Os+2, Os+3, Os+4. Os+6, Os+8.
У лантаноидов и актиноидов в первую очередь отрываются электроны с наружного слоя, затем с соседнего с наружным и, наконец, с ещё более глубокого третьего слоя, считая от внешнего.
Лантаноиды, как правило, образуют трёх зарядные ионы.
Кроме того, Се, Рr, Nd и Тb в некоторых соединениях образуют четырёхвалентные ионы, a Sm Еu и Lb—двухвалентные ионы.
Переход нейтральных атомов в состояние отрицательно заряженных ионов
Образование отрицательно заряженных ионов основано на свойстве атомов, внешний электронный слой которых состоит из четырёх, пяти, шести и семи электронов (неметаллы).
Легче приобрести ещё некоторое количество электронов в наружном слое до восьми.
Например:
Э0 + F0 → Э+1 + F-1
2Э0 + 00 → 2Э+1 + 0-2
3Э0 + P0 → 3Э+1 + P-3
4Э0 + Si → 4Э+1 + Si-4
Э — обозначает атом элемента.
Атомы, наружный слой которых состоит из одного, двух и трёх электронов, не могут притянуть избыточных электронов, и потому они отрицательно зарядных ионов не образуют.
Происходит это потому, что атомы этих элементов, чтобы пополнить свой наружный слой до восьми, притягивают пять, шесть и семь электронов.
Что, естественно, труднее, чем потерять один, два, три электрона и обнажить восьми электронный или восемнадцати электронный слой.
Исходя из величин радиусов атомов и ионизационных потенциалов, нетрудно установить следующее:
а) Наиболее энергично притягивают электроны, при прочих равных условиях, те атомы, внешний электронный слой которых состоит из семи электронов.
То есть те нейтральные атомы, которым нужно притянуть один избыточный электрон.
б) Наименее энергично притягивают электроны те нейтральные атомы, внешний электронный слой которых состоит из четырёх электронов.
То есть атомы, которым для образования октета (8) нужно притянуть четыре электрона.
в) Чем больше радиус атома, тем избыточные электроны удерживаются слабее.
Следует особо заметить:
а) Положительно заряженные ионы образуют как металлы, так и неметаллы;
б) Отрицательно заряженные ионы образуют только неметаллы;
в) Атомы инертных газов в обычных условиях ни положительно, ни отрицательно заряженных ионов не образуют.
Изменение числа электронов в наружном квантовом слое атомов в процессе реакций окисления-восстановления
Элемент — Алюминий. Порядковый номер — 13. Строение электронной оболочки атома — 2:8:3. Строение электронной оболочки иона — Аl••• — 2:8.
Элемент — Кремний. Порядковый номер — 14. Строение электронной оболочки атома — 2:8:4. Строение электронной оболочки иона — Si•• — 2:8:2.
Элемент — Фосфор. Порядковый номер — 15. Строение электронной оболочки атома — 2:8:5. Строение электронной оболочки иона — Р•••— 2:8:8.
Статья на тему Ионное состояние

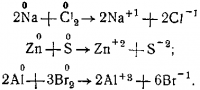
Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.