Теория:
Протактиний (Pa) в периодической системе: 7‑й период, 3‑я группа (по устаревшей классификации — IIIB), атомная масса 231,035 а.е.м.
Занимает положение в 7‑м периоде, что определяет его принадлежность к семейству актиноидов — радиоактивных металлов, завершающих таблицу Менделеева.
Будучи химическим гомологом (аналогом) лантаноида празеодима по положению, он, тем не менее, проявляет уникальные свойства, сближающие его с танталом.
Его поведение в химии растворов часто диктуется переходом между 5f- и 6d-подуровнями, что делает его структуру исключительной.
А его нахождение в 3‑й группе (семейство актиноидов) задает ключевые параметры:
- Возможность проявлять устойчивую высшую степень окисления +5, что нехарактерно для более легких актиноидов, но типично для этого «предвестника актиния».
Структура атома подтверждается его электронной формулой (конфигурацией):
[Rn] 5f2 6d1 7s2.
На которой наглядно можно определить его положение как f-элемента, находящегося в начале актиноидного ряда, сразу после тория.
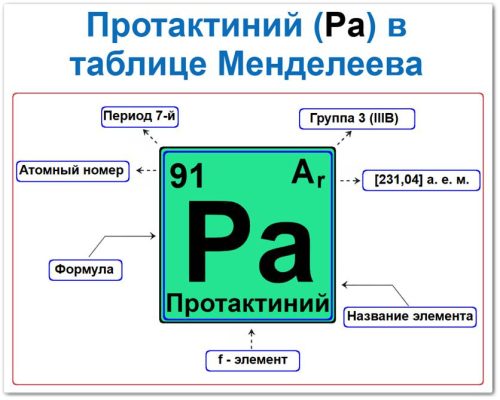
Протактиний в таблице Менделеева можно определить на основании закона периодичности: положение в группе и периоде, а также порядкового номера / атомный номер (Z = 91)
Содержание страницы
- 1. Как определить положение Протактиния в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 91)
- 3. Название и символ
- 4. Группа (3 / III B)
- 5. Период (7‑й)
- 6. Относительная атомная масса (Ar)
- 7. f‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Протактиния по Таблице Менделеева
- 9. Проверка знаний: Как определить протактиний по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Протактиния в Таблице Менделеева
Локация протактиния в таблице описывается характеристиками его природного радиоактивного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (вертикальный ряд актиноидов).
- Период (горизонтальный ряд).
- Электронное семейство (протактиний — f‑элемент).
Порядковый номер / атомный номер (Z = 91)
- Служит уникальным идентификатором элемента в ряду естественных радиоактивных изотопов.
- В ядре — 91 протон; в нейтральной оболочке — 91 электрон.
- Электронное строение: [Rn] 5f2 6d1 7s2.
Важно: Наличие электрона на 6d-подуровне наряду с 5f-электронами объясняет его способность проявлять стабильную степень окисления +5, напоминая переходные металлы 5-й группы.
Название и символ
- Название: «протактиний» (от греческого «protos» — первый, предшественник актиния, так как при распаде он образует актиний).
- Символ: Pa.
- Примечание: Элемент был предсказан еще Менделеевым (как «эка-тантал») и окончательно выделен в чистом виде лишь в 1934 году Аристидом фон Гроссом.
Группа (3 / III B)
Расположен в 3‑й группе (семейство актиноидов), занимая вторую позицию в ряду f-элементов 7-го периода.
Химический потенциал:
- Валентность протактиния: высшая валентность V.
- Степень окисления: наиболее устойчивая +5, реже проявляет +4. В этом его главное отличие от лантаноидов, для которых типична только +3.
Период (7‑й)
Находится в 7‑м периоде — его электроны распределены по семи энергетическим уровням.
Влияние на свойства:
- Металлический блеск: Протактиний — это яркий, серебристо-белый металл, который тускнеет на воздухе, покрываясь тонким слоем оксида.
- Радиоактивность: В природе встречается в урановых рудах в ничтожных количествах, являясь членом радиоактивного ряда урана-235.
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
Относительная атомная масса (Ar)
- Ar(Pa) ≈ 231,035 а.е.м. (для наиболее распространенного природного изотопа 231Pa).
- Определение: атомная масса определяется по стабильному природному нуклиду, входящему в состав земной коры.
- Стабильность: Период полураспада 231Pa составляет около 32 760 лет, что делает его доступным для химических исследований.
Все значения для всех элементов можно узнать в таблице атомных масс.
f‑Элемент (электронное семейство)
Застраивающимся является 5f‑подуровень (5f2).
Специфика блока: Будучи f-элементом, протактиний находится на этапе, когда f-оболочка только начинает заполняться, поэтому его электроны ведут себя более «активно», чем у более тяжелых актиноидов (например, эйнштейния).
Определение энергетических уровней Протактиния по Таблице Менделеева
Положение Протактиния (Pa) в системе Менделеева — это готовый «паспорт» его внутреннего устройства.
1. 7-й период (Количество этажей)
Протактиний находится в седьмой строке таблицы. Номер периода определяет число электронных слоев.
- Итог: У Протактиния 7 энергетических уровней.
2. Список «жильцов» (Распределение электронов)
Атомный номер Протактиния — 91. Его 91 электрон распределен по уровням следующим образом:
Pa ) 2 ) 8 ) 18 ) 32 ) 20 ) 9 ) 2
Для сравнения: У соседа слева, Тория (90), на пятом уровне 18 или 19 электронов (в зависимости от модели), а у Протактиния начинается явное заполнение 5f-оболочки (20 электронов на 5-м уровне).
3. 3-я группа (Химический характер)
Протактиний входит в семейство актиноидов.
- f-элемент: Его свойства диктуются гибкостью перехода электронов между 5f и 6d слоями.
- Место в блоке: Он является аналогом празеодима, но его химия гораздо богаче из-за более высокой валентности.
Проверка знаний: Как определить протактиний по таблице Менделеева
Выберите три верных тезиса, которые однозначно характеризуют Протактиний (Pa) в структуре таблицы.
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3
- 1) Номер 91. Точный порядковый номер элемента Pa.
- 2) Актиноид 7-го периода. Это определяет его принадлежность к f-блоку и 7-слойную структуру.
- 3) Предшественник актиния. Отражает этимологию названия и радиоактивную связь.
- 4) Ошибка. Протактиний чрезвычайно токсичен и радиоактивен, контакт с пищей исключен.
- 5) Ошибка. Это активный металл, а не газ.
- 6) Ошибка. Элемент был выделен в XX веке; древние не могли знать о трансуранах.
Часто задаваемые вопросы:
Он расположен в 7-м периоде и 3-й группе (в ряду актиноидов), под номером 91.
Порядковый номер периода (7) указывает на наличие 7 энергетических уровней.
Является f-элементом и относится к семейству актиноидов.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.