Теория:
Барий (Ba) в периодической системе: 6‑й период, 2‑я группа (по устаревшей классификации — главная подгруппа II группы), атомная масса 137,33 а.е.м.
Занимает положение в 6‑м периоде, что определяет его принадлежность к щелочноземельным металлам — активным элементам, которые в свободном виде встречаются в природе только в виде соединений.
Будучи типичным представителем своего семейства, он входит в состав s-элементов, характеризующихся наличием двух валентных электронов на внешнем слое.
Нахождение Бария во 2‑й группе и специфическое строение атома обуславливают его ключевые параметры:
Постоянную валентность II.
А также высокую химическую активность, способность окрашивать пламя в характерный желтовато-зеленый цвет и широкое применение в рентгенографии и пиротехнике.
Структура атома подтверждается его электронной формулой (конфигурацией):
[Xe] 6s2.
На которой наглядно можно определить его положение как s-блочного элемента, где завершается заполнение внешнего 6s-подуровня.
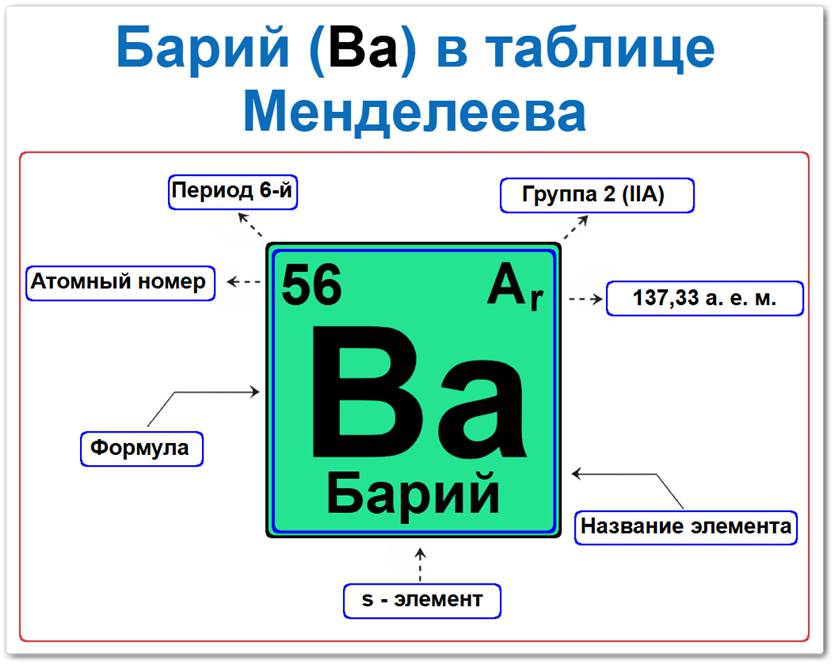
Барий в таблице Менделеева можно определить на основании закона периодичности: положение в группе щелочноземельных металлов, период 6, группа 2, а также по его порядковому номеру (Z = 56).
Содержание страницы
- 1. Как определить положение Бария в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 56)
- 3. Название и символ
- 4. Группа (2 / II A)
- 5. Период (6‑й)
- 6. Относительная атомная масса (Ar)
- 7. s‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Бария по Таблице Менделеева
- 9. Проверка знаний: Как определить барий по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Бария в Таблице Менделеева
Локация бария в таблице описывается характеристиками его атомного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (2-я группа, щелочноземельные металлы).
- Период (горизонтальный ряд).
- Электронное семейство (барий — s‑элемент).
Порядковый номер / атомный номер (Z = 56)
- Служит уникальным кодом элемента в системе.
- В ядре — 56 протонов; в нейтральной оболочке — 56 электронов.
- Электронное строение: [Xe] 6s2.
Важно: Барий — один из самых активных металлов в своей группе. Из-за высокой реакционной способности его хранят под слоем керосина или в герметичных ампулах.
Название и символ
- Название: «барий» (от греч. «barys» — тяжелый).
- Символ: Ba.
- Примечание: Открыт Карлом Шееле в 1774 году в виде оксида, выделен в чистом виде Гемфри Дэви в 1808 году. Основной минерал — барит (тяжелый шпат).
Группа (2 / II A)
Расположен во 2‑й группе (щелочноземельные металлы). В таблице Менделеева барий находится под стронцием и над радием.
Химический потенциал:
- Валентность бария: постоянная валентность II.
- Степень окисления: +2. Большинство солей бария ядовиты, за исключением сульфата бария, который нерастворим.
Период (6‑й)
Находится в 6‑м периоде — его электроны распределены по шести энергетическим уровням.
Влияние на свойства:
- Металлические свойства: Барий обладает более выраженными металлическими свойствами, чем магний или кальций, из-за большого радиуса атома.
- Применение: Соединения бария используются для создания вакуума в электронике и в качестве контрастного вещества при рентгене желудка.
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
Относительная атомная масса (Ar)
- Ar(Ba) ≈ 137,33 а.е.м.
- Определение: среднее значение массы семи природных стабильных изотопов бария.
Все значения для всех элементов можно узнать в таблице атомных масс.
s‑Элемент (электронное семейство)
Застраивающимся является внешний 6s‑подуровень (6s2).
Специфика блока: Как типичный s-элемент, барий проявляет сильные восстановительные свойства и легко отдает два внешних электрона, превращаясь в ион Ba2+.
Определение энергетических уровней Бария по Таблице Менделеева
Положение Бария (Ba) в системе Менделеева — это готовый «паспорт» его внутреннего устройства.
1. 6-й период (Количество этажей)
Номер периода определяет число электронных слоев.
- Итог: У Бария 6 энергетических уровней.
2. Список «жильцов» (Распределение электронов)
Атомный номер Бария — 56. Его 56 электронов распределены по уровням следующим образом:
Ba ) 2 ) 8 ) 18 ) 18 ) 8 ) 2
3. 2-я группа (Химический характер)
Барий — типичный щелочноземельный металл.
- s-элемент: Валентные электроны находятся на внешнем s-слое.
- Активность: В ряду активности металлов стоит значительно левее водорода, бурно реагирует с водой.
Проверка знаний: Как определить барий по таблице Менделеева
Выберите три верных тезиса, которые однозначно характеризуют Барий (Ba) в структуре таблицы.
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3
Часто задаваемые вопросы:
Барий расположен в 6-м периоде, во 2-й группе. Это s-элемент, относящийся к щелочноземельным металлам. Порядковый номер — 56
У бария 6 энергетических уровней, так как он находится в 6-м периоде.
Схема распределения: 2, 8, 18, 18, 8, 2.
Соединения бария окрашивают бесцветное пламя горелки в характерный желто-зеленый (яблочно-зеленый) цвет.
