Нобелий (No) — это синтетический, высокорадиоактивный трансурановый химический элемент с атомным номером 102.
Он относится к группе актинидов и назван в честь Альфреда Нобеля. Не встречается в природе, производится искусственно в очень малых количествах для научных исследований.
Может быть получен бомбардировкой более легких элементов тяжелыми ионами в специальных ускорителях.
Не какого практического применения нет из радиации и больших затрать для его получения.
Содержание страницы
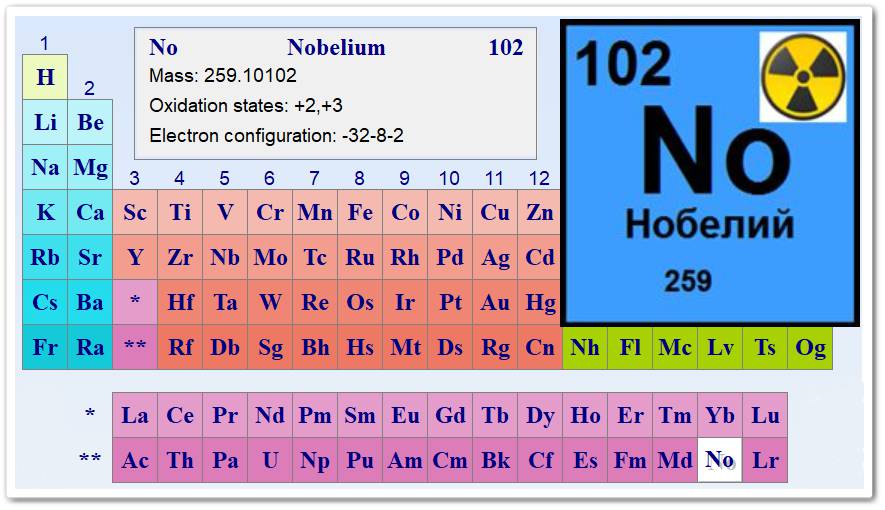
Что такое нобелий
[Nobelium; по имени швед, инженера А. Нобеля (A. Nobel), основателя фонда международных (нобелевских) премий], No — искусственно полученный радиоактивный хим. элемент.
Атомный номер 102; относится к актиноидам.
Название предложено группой амер., англ. и швед, ученых, сообщивших (1957) о синтезе изотопа 102-го элемента с массовым числом 253 или 251 и периодом полураспада около 10 сек.
Проверка амер. учеными (А. Гиорсо и др.) в Беркли (США) и советскими физиками (Г. Н. Флеровым и др.) в Дубне (СССР) показала ошибочность этого сообщения.
Правильные данные о 102-ом элементе и его хим. св-вах были получены (1963-66) в Дубне Г. Н. Флеровым и его сотрудниками, к-рые предложили для 102-го элемента название «Жолиотий» (по имени франц. ученого Ф. Жолио-Кюри).
Физические свойства
Большинство его физических свойств основаны на теоретических предсказаниях и экстраполяции из поведения других актинидов.
Агрегатное состояние: Предполагается, что это твердый металл при комнатной температуре.
Внешний вид: Ожидается, что будет серебристо-белым или серым металлом с металлическим блеском, как и другие актиниды.
Плотность: Расчетная плотность составляет около 9,9 г/см3. (Значения могут варьироваться в разных источниках, например, 9.9(4) g/cm3).
Температура плавления: Предсказана около 800-827 °C (или 1100 K).
Температура кипения: Неизвестна (предположительно).
Радиоактивность: Все известные изотопы нобелия очень радиоактивны и имеют короткие периоды полураспада. Самый стабильный изотоп, 259No, имеет период полураспада около 58 минут.
Более короткоживущие изотопы, такие как 255No (период полураспада 3,1 минуты), чаще используются в химических исследованиях, так как их легче производить в достаточном количестве.
Кристаллическая структура: Предполагается, что имеет гранецентрированную кубическую (face-centered cubic, FCC) структуру.
Металлические свойства: Как актинид, предположительно, является типичным металлом с соответствующей электропроводностью, но прямое измерение этих свойств невозможно.
Интересный факт: связан с историей его открытия и последующими спорами о том, кто же его на самом деле открыл.
1957 год, Швеция (Нобелевский институт).
1966 год, СССР (Объединенный институт ядерных исследований в Дубне).
1966 год, США (Калифорнийский университет в Беркли).
Химические свойства
По химическим свойствам нобелий близок к фермию и калифорнию.
Хлорид нобелий мало летуч, в водных растворах наиболее стойкая степень окисления +2, действием сильных окислителей можно получить No3+ но не выше.
✅ Степени окисления:
+2 (наиболее устойчивая): Это наиболее характерная и уникальная особенность нобелия среди актинидов.
В отличие от большинства других актинидов, для которых степень окисления +3 является доминирующей, для нобелия в водных растворах степень окисления +2 более стабильна.
Это обусловлено стабильностью полностью заполненной 5f-оболочки (5f14) в ионе No2+
(после потери двух 7s электронов).
+3 (также существует, но менее устойчива): Нобелий также может проявлять степень окисления +3, что соответствует типичному поведению актинидов.
Однако ионы No3+ являются сильными окислителями и легко восстанавливаются до No2+.
✅ Электронная конфигурация No:
Предполагаемая электронная конфигурация внешних оболочек: [Rn]5f147s2. Такая конфигурация хорошо объясняет стабильность степени окисления +2.
✅ Реактивность:
Как металл, нобелий предположительно является реакционноспособным, хотя его реакции с воздухом, водой, галогенами, кислотами и щелочами напрямую не изучались из-за его исключительной радиоактивности и дефицита.
Его химическое поведение в водном растворе сравнивают с поведением иттербия (Yb), который является гомологом нобелия среди лантанидов и также проявляет устойчивую степень окисления +2.
Предполагается, что нобелий реагирует с кислородом (образуя оксиды, вероятно NoO или No2O3).
Химики в Дубне (Россия) установили, что нобелий образует нелетучий хлорид, а американские химики подтвердили устойчивость степени окисления +2 в водных растворах.
✅ Комплексообразование:
Ионы нобелия способны образовывать комплексные соединения в растворах. Его поведение в комплексообразовании сопоставимо с другими актинидами и лантанидами, которые проявляют те же степени окисления.
Изотопы элемента
Известны девять изотопов нобелий с массовыми числами 251—259 и периодами полураспада соответственно 0,8 ± ± 0,3; 4,5 ± 1,5; 95 ± 10; 65 ± 15; 180 ± 20; 3,7 ± 0,5; 23 ± 2; 0,0012 сек (спонтанное деление) и 1,5 ± ± 0,5 ч.
Наиболее долгоживущий изотоп получен (1970) в Ок-Ридже (США) при облучении изотопа 248Сm ускоренными ионами тяжелого 180.
Другие изотопы (с массовыми числами от 251No до 258No) образуются в микроколичествах (сотни атомов) при облучении урана, плутония, америция и кюрия ускоренными ионами углерода, азота, кислорода и неона.
Получение
Основной метод получения нобелия — это бомбардировка более легких элементов тяжелыми ионами в ускорителях частиц (циклотронах).
✅ Например:
Мишень: В качестве мишени обычно используются изотопы трансурановых элементов, расположенных ниже нобелия в Периодической таблице, чаще всего изотопы кюрия (Cm) или калифорния (Cf).
Эти мишени должны быть очень чистыми и очень тонкими.
Снаряды (ускоренные ионы): Мишень бомбардируется высокоэнергетическими ядрами более легких элементов (так называемыми «снарядами»), которые ускоряются в циклотроне или линейном ускорителе.
Часто используются ионы углерода (C) или неона (Ne), а иногда ионы кислорода (O) или азота (N).
Ядерная реакция (слияние ядер): При столкновении и слиянии ядра мишени и ядра снаряда образуется составное ядро, которое затем испускает несколько нейтронов (обычно 3-5), чтобы стабилизироваться и образовать ядро нобелия.
✅ Исторические примеры реакций:
+4n (одна из реакций, использованных для получения нобелия в Беркли)
249Cf + 12C → 257No
+4n (реакция, проведенная в Дубне)
244Cm + 12C → 252No
+4n (получение более тяжелых изотопов нобелия)
248Cm + 18O → 262No
✅ Разделение и идентификация:
После реакции образовавшиеся атомы нобелия (которые производятся в крайне малых количествах, часто всего по несколько атомов за раз) должны быть отделены от мишени, пучка снарядов и других продуктов реакции.
Это делается с помощью быстрых радиохимических или физических методов (например, газофазная хроматография, разделение по массе или химическая экстракция).
Их идентификация происходит по характерным энергиям альфа-распада и периодам полураспада, а также по продуктам распада.
✅ Сложности получения:
Крайне малые количества: Нобелий всегда получают в атомарных количествах, что делает его одним из самых редких и дорогих веществ для исследования.
Короткие периоды полураспада: Даже самые стабильные изотопы нобелия имеют периоды полураспада в минутах или часах, что означает, что у исследователей очень мало времени для изучения его свойств.
Интенсивная радиоактивность: Высокая радиоактивность требует строгих мер безопасности и использования дистанционного управления.
Применение
Не имеет никаких практических или коммерческих применений.
Его использование строго ограничено фундаментальными научными исследованиями, где он служит:
✅ Инструментом для изучения свойств трансактинидных и сверхтяжелых элементов: Нобелий находится в самом конце ряда актинидов, на границе с трансактинидными элементами.
Его изучение позволяет ученым понять, как химические и физические свойства изменяются с увеличением атомного номера, проверить теоретические модели строения атомов и предсказать поведение еще более тяжелых элементов.
В частности, изучение его уникальной устойчивости степени окисления +2 имеет большое значение для понимания релятивистских эффектов в тяжелых элементах.
✅ Мишенью для синтеза новых, более тяжелых элементов: Некоторые изотопы нобелия могут потенциально использоваться в качестве мишеней в ускорителях частиц для создания еще более тяжелых, пока неизвестных или малоизученных химических элементов.
Литература
Флеров Г. Н. Синтез и исследование свойств элемента 102. «Атомная энергия»
Часто задаваемые вопросы
Оценочная стоимость одного грамма этого элемента примерно триллионы или квадриллионы долларов.
Потому, что очень большие затраты на оборудование, энергетические и человеческие ресурсы, а также строительство специального ядерного реактора.
Быстро распадается, испуская альфа-частицы, а в некоторых случаях также гамма-лучи и бета-частицы.
Испуская радиоактивность которая плохо влияет на человека в целом, может образоваться рак, ДНК мутация.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.