Содержание страницы
Теория:
Молекула серной кислоты — это химическое соединение с формулой H2SO4.
Одна из сильнейших и наиболее важных неорганических кислот.
Состоит из двух атомов водорода (H), одного атома серы (S) и четырёх атомов кислорода (O).
Имеет тетраэдрическое строение вокруг центрального атома серы.
В чистом виде это тяжёлая, маслянистая жидкость, обладающая сильными водоотнимающими (гигроскопичными) и окислительными свойствами.
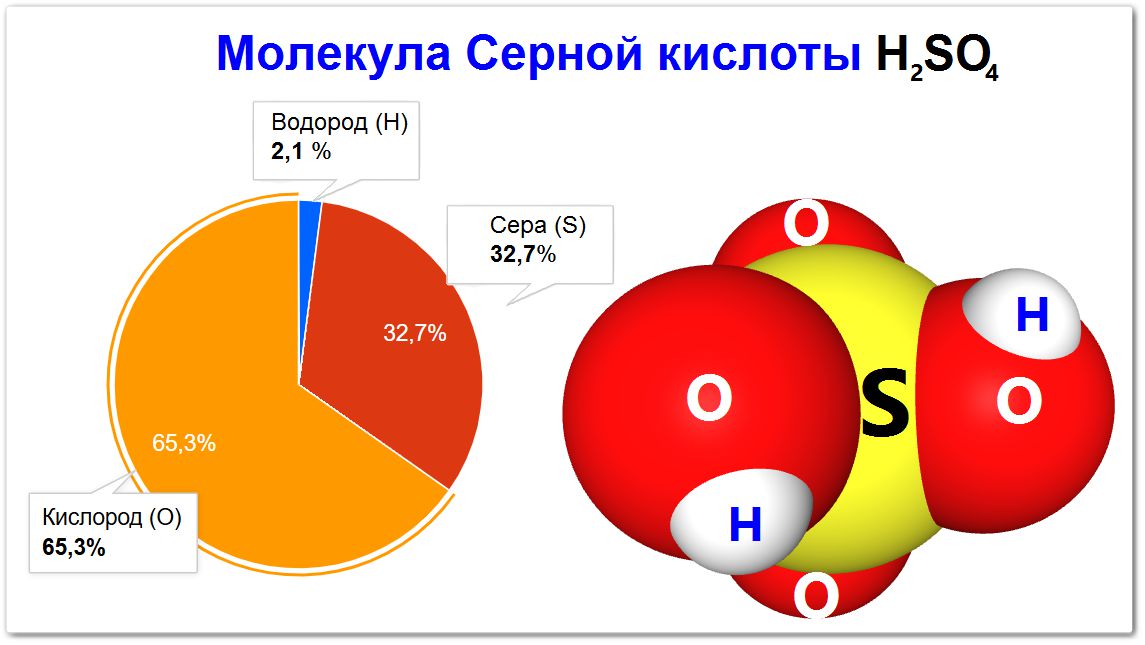
Строение молекулы серной кислоты
Молекула серной кислоты (H2SO4) имеет тетраэдрическое строение вокруг центрального атома серы.
Центральный атом: Сера (S) находится в центре.
Связи с кислородом: Сера связана с четырьмя атомами кислорода (O).
- Две двойные связи (S = O): Два атома кислорода связаны с серой двойными связями.
- Две одинарные связи (S — O): Два других атома кислорода связаны с серой одинарными связями.
Гидроксильные группы: К этим двум атомам кислорода, связанным одинарной связью, присоединено по одному атому водорода (H), образуя две гидроксильные группы (-OH).
Основные характеристики и строение молекулы серной кислоты
Состав:
Одна молекула H2SO4 состоит из:
Двух атомов водорода (H)
Одного атома серы (S)
Четырех атомов кислорода (O)
Строение (Геометрия)
В центре молекулы находится атом серы (S).
Сера связана с четырьмя атомами кислорода (O).
Два атома кислорода связаны с серой двойными связями (S = O).
Два других атома кислорода связаны с серой одинарными связями (S — O), и к каждому из этих атомов кислорода, в свою очередь, присоединен по атому водорода (H).
Таким образом, в молекуле серной кислоты есть две гидроксильные группы (-OH).
Геометрия вокруг атома серы тетраэдрическая (как у метана CH4, но с кислородами вместо водородов).
Атом серы находится в центре тетраэдра, а атомы кислорода — в его вершинах.
Молекула полярная.
Структурная формула серной кислоты
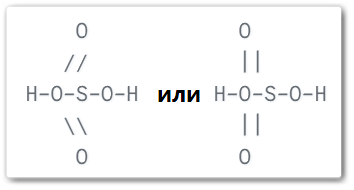
Молекулярная масса
Атомная масса водорода (H) ≈ 1.008 а.е.м.
Атомная масса серы (S) ≈ 32.06 а.е.м.
Атомная масса кислорода (O) ≈ 15.999 а.е.м.
Молекулярная масса H2SO4 = (2 × 1.008) + 32.06 + (4 × 15.999) = 2.016 + 32.06 + 63.996 = 98.072 а.е.м.
Молярная масса H2SO4 ≈ 98.07 г/моль.
Свойства (обусловленные строением)
Сильная двухосновная кислота: Наличие двух гидроксильных групп (-OH) позволяет серной кислоте отдавать два протона (H+).
В водном растворе она является очень сильной кислотой, полностью диссоциируя по первой ступени и сильно по второй.
Гигроскопичность (водоотнимающие свойства): Серная кислота очень «любит» воду. Это свойство широко используется, например, для осушки газов.
Сильный окислитель: Концентрированная серная кислота является сильным окислителем, способным реагировать со многими металлами и органическими веществами.
Серная кислота является одним из важнейших химических продуктов в мире, использующимся во многих отраслях промышленности.
Пример решения, задача:
Задача № 1.
Дано: Какова масса 0.2 моль серной кислоты (H2SO4)?
Решение: Масса (m) = Количество вещества (n) × Молярная масса (M)
m(H2SO4) = 0.2 моль×98.09 г/моль = 19.618 г.
Ответ: 19.618 г.
Задача № 2.
Дано: Сколько моль серной кислоты (H2SO4) содержится в 49.045 граммах чистой серной кислоты?
Решение: Количество вещества (n) = Масса (m) / Молярная масса (M)
n(H2SO4) = 49.045 г/98.09 г/моль = 0.5 моль.
Ответ: 0.5 моль.
Часто задаваемые вопросы:
Состоит из двух атомов водорода (Н), одного атома серы (S) и четырех атомов кислорода (О).
Записывается как H2SO4, читается («аш-два-эс-о-четыре»)
Из двух атомов водорода (Н)(именно из за этого серную кислоту называют двухосновной), одного атома серы (S) и четырех атомов кислорода (О).
В серной кислоте Н2SО4, находиться: 2Н + 1S + 4О = 7.
То есть 7 атомов.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.