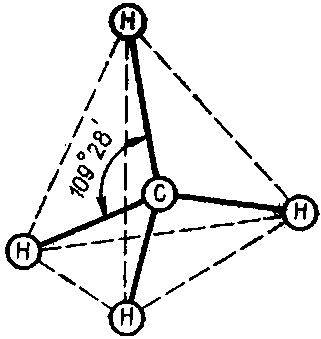
Рис. Строение молекулы метана.
Содержание страницы
Гибридизация атомных орбиталей
В нормальном состоянии атом углерода имеет на внешнем слое два не спаренных электрона.
При возбуждении один s-электрон переходит на р— подуровень и общее число не спаренных электронов становится равным четырем.
Наиболее известными соединениями четырехвалентного углерода являются метан СН4 и четырех хлористый углерод ССl4.
Из рассмотрения электронной конфигурации возбужденного атома углерода следует, что в этих двух соединениях не все химические связи эквивалентны:
- Одна ковалентная связь образована за счет не спаренного s — электрона.
- А три других — с помощью р— электронов.
История открытия
Однако еще в прошлом веке К. Шорлеммер экспериментально доказал равноценность всех четырех связей атома углерода, а Я. Вант Гофф выдвинул гипотезу о его тетраэдрическом строении.
С тех пор правильность тетраэдрической модели была доказана с помощью различных физических и химических методов.
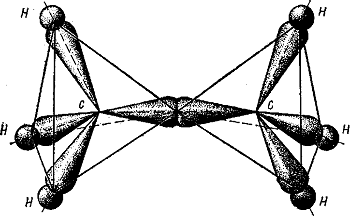
Рис. 2. Электронное строение молекулы этана.
В 1931 г. известный американский химик Лайнус Карл Полинг предположил, что в атоме углерода вместо одной s— и трех р-орбиталей возникают четыре гибридных sp3-орбитали с промежуточной энергией.
Электронные облака этих орбиталей направлены из центра правильного тетраэдра к его четырем вершинам.
Углы между связями равны 109°28′.
Перекрывание sp3— электронных облаков атома углерода с s-электронными облаками атомов водорода происходит в направлениях осей гибридных орбиталей, причем образуются четыре одинаковые ковалентные связи (рис. ).
Устойчивость тетраэдрической конфигурации объясняется максимальной удаленностью всех четырех атомов водорода друг от друга.
Образования гибридных атомных орбиталей
Аналогичное окружение углерода сохраняется во многих его соединениях.
Например, молекулу этана можно представить в виде двух соединенных углами тетраэдров (рис. 2).
Возможны самые различные случаи образования гибридных атомных орбиталей.
Так, если в атоме имеются одна s— и две р— орбитали, то могут возникнуть три sр2— орбитали, которые располагаются в одной плоскости под углами 120° друг к другу.
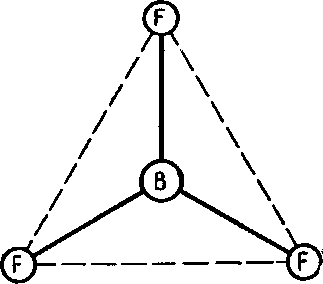
Примером соединения, образованного с помощью таких орбиталей, является трифторид бора.
Молекула BF3 имеет форму равностороннего треугольника, в вершинах которого расположены атомы галогена, а в центре — атом бора (рис. 3).
Пространственное строение предельных углеводородов метана
Атом углерода в состоянии sр3-гибридизации изображают, рисуя направления осей гибридных орбиталей в пространстве:
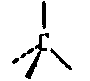
Сплошные линии расположены в плоскости листа, пунктирная линия проходит за этой плоскостью, а жирная линия направлена к читателю.
Симметричные молекулы метана, четырех хлористого углерода и этана выглядят в этом случае так:
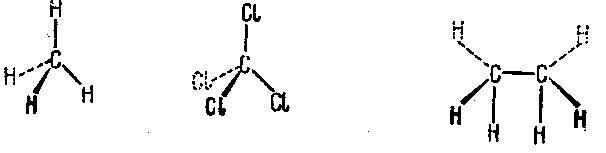
В молекуле этана два связанных между собой атома углерода свободно вращаются вокруг С—С связи.
При том метальные группы СН3 могут ориентироваться друг относительно друга самыми различными способами.
Любое их взаимное расположение называется конформацией.
Поскольку все атомы в молекуле в большей или меньшей степени взаимодействуют друг с другом, конформации несколько различаются по энергии.
Пример изменения энергетического состояния молекул
Рассмотрим, например, изменение энергетического состояния молекулы этана при вращении СН3-групп.
Для удобства будем смотреть на молекулу вдоль оси С—С, соединяющей атомы углерода.
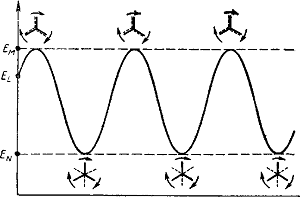
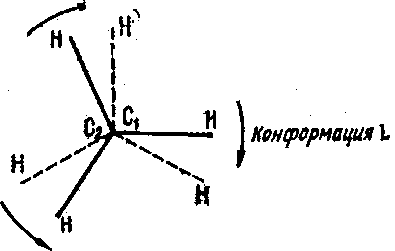
За начальное состояние молекулы этана совершенно произвольно примем конформацию L с энергией EL
(Химические связи атома углерода С2, удаленного от читателя, обозначены штриховой линией.)
Представим теперь, что атом углерода С2 закреплен неподвижно, а метальная группа С1Н3 вращается вокруг связи С—С по часовой стрелке.
В этом случае можно зафиксировать два наиболее характерных состояния молекулы этана:
- Конформацию М, в которой атомы водорода заслоняют друг друга.
- Конформацию N, в которой эти атомы удалены друг от друга на максимально возможное расстояние:
Вследствие взаимного отталкивания атомов водорода энергия конформации М оказывается выше, а энергия конформации N ниже, чем EL, т. е. EN<EL<EM.
Изменение внутренней энергии молекулы этана при вращении вокруг С—С связи показано на рисунке 8.
Поскольку конформация N энергетически наиболее выгодна, молекула этана должна в принципе находиться только в этом состоянии.
Разность EM—EN между наиболее высоким и наиболее низким уровнями энергии настолько мала, что достаточно энергии обычного теплового движения, чтобы происходило свободное вращение вокруг оси С—С.
Пространственное строение циклических соединений углерода
Углерод может образовывать замкнутые цепи — циклы.
Атомы углерода в состоянии sp3-гибридизации образуют четыре ковалентные связи, направленные от центра к вершинам правильного тетраэдра.
Такое состояние углерода в молекулах наиболее устойчиво.
Если углы между направлениями химических связей отличаются от тетраэдрического (109°28′), то связи находятся в напряженном состоянии, а молекула в целом имеет избыток внутренней энергии.
Молекулы с напряженными химическими связями обладают повышенной реакционной способностью, которая тем выше, чем больше отклонение валентного угла от 109°28′.
При переходе от циклопропана к циклобутану, а затем к циклопентану снижение напряженности циклов сопровождается повышением их устойчивости, т. е. снижением реакционной способности.
Циклопропан присоединяет водород и превращается в пропан при 80°С в присутствии мелкораздробленной платины:
Для аналогичной реакции циклобутана требуется более высокая температура:
Циклы больших размеров ниже 200°С не разрываются.
Они устойчивы вследствие того, что принимают такие пространственные положения, при которых все углы между направлениями химических связей приближаются к тетраэдрическому.
В настоящее время наиболее изученными являются конформации циклогексана.
Статья на тему Гибридизация атомных орбиталей

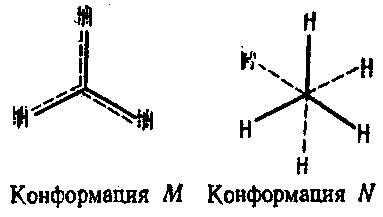
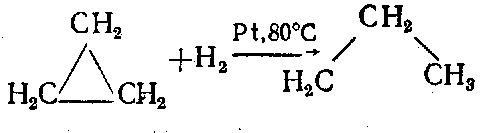
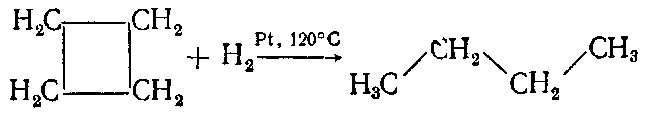
Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.