H водород (hydrogenium) — химический элемент с порядковым номером 1 в периодической системе.
Простое газообразное вещество, в обычных условиях молекула водорода состоит из двух атомов, связанных ковалентной связью.
Молекулярный водород — легчайший газ (в 14,32 раза легче воздуха); плотность его (т-ра 0° С, давление 1 am) 0,089870 г/л; tпл — 259,1° С; tкип -252,6° С.
Находится в периоде. Плотность: 0.0000899 г/см3.
В нормальных условиях это газ без цвета и вкуса, при температуре от −252,76 до −259,2 °C бесцветная жидкость.
При температуре от −259,2 °C твердое вещество которое проявляет сверхпроводящие свойства.
Содержание страницы
Электронная формула
Электронная формула атома водорода:
1s1
Электронно-графическая схема водорода (Н).
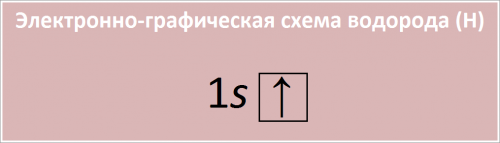
Рис. Схема распределения электронов по атомным орбиталям в атоме водорода.
Энергетические уровни
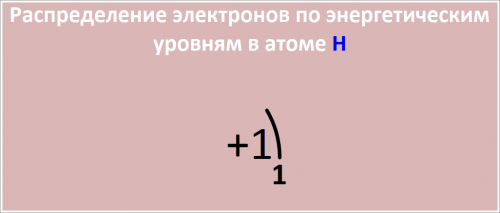
Распределение электронов по энергетическим уровням в атоме H.
1-й уровень (K) : 1
Валентные электроны водорода
Количество валентных электронов в атоме водорода — 1.
Ниже приведены их квантовые числа (N — главное, L — орбитальное, M — магнитное, S — спин).
Стабильные изотопы
| Орбиталь | N | L | M | S |
| s | 1 | 0 | 0 | +1/2 |
Степени окисления водорода, которые может проявлять:
-1, +1.
Валентность водорода: I (1)
Стабильные изотопы
Природный водород состоит из смеси изотопов; легкого водорода, или протия ¹Н (99,98%) и тяжелого водорода (²Н), или дейтерия D (0,02%) с массовыми числами соответственно 1 и 2.
| Изотоп | Протоны | Нейтроны | Атомная масса изотопа |
| 1H | 1 | 0 | 1.00782503223 |
| 2H | 1 | 1 | 2.01410177812 |
