Теория:
Степень окисления рубидия (Rb) во всех сложных соединениях всегда равна +1. Это состояние является единственно возможным и типичным для всех элементов его группы.
Значение 0 встречается только в простом веществе (металлический рубидий).
Отрицательных степеней окисления рубидий не проявляет, так как является чрезвычайно активным металлом.
Рубидий находится в 1-й группе (главная подгруппа I группы) и является s-элементом 5-го периода.
Как s-элемент, он обладает электронной конфигурацией [Kr] 5s1. На внешнем слое у рубидия находится всего один электрон.
Рубидий проявляет единственную степень окисления +1. Это связано с тем, что атому энергетически выгодно отдать один внешний электрон, чтобы приобрести устойчивую электронную конфигурацию благородного газа криптона.
В отличие от лития или натрия, рубидий обладает еще более выраженными металлическими свойствами из-за большего радиуса атома, что делает его одним из самых активных металлов.
Чтобы определить возможные значения, используют электронную формулу.
Например:
- Для рубидия (1s22s22p63s23p63d104s24p65s1) — потеря единственного 5s-электрона дает стабильную СО +1.
- Для стронция (сосед по периоду) — наличие двух электронов на внешнем слое дает максимальную СО +2.
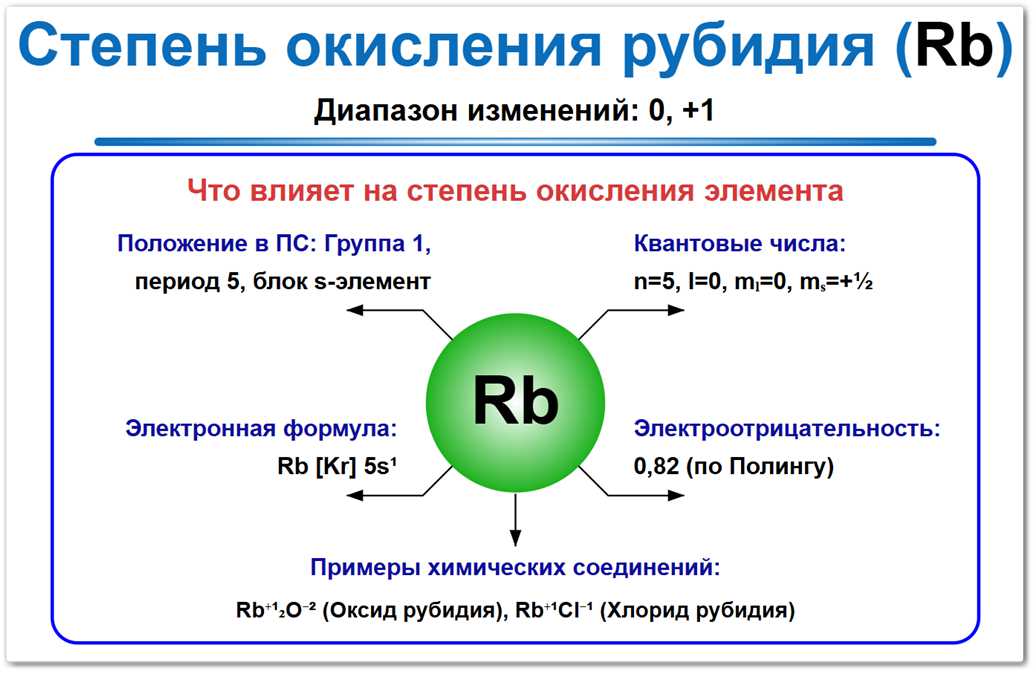
Рис. 1. Возможные степени окисления рубидия: 0, +1. Рубидий никогда не проявляет других степеней окисления в химических реакциях.
На их формирование влияют электронное строение (один s-электрон), положение в 1-й группе (щелочные металлы) и очень низкое значение электроотрицательности 0,82 по шкале Полинга.
Содержание страницы
- 1. Почему у рубидия постоянная степень окисления?
- 2. Степень окисления рубидия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 3. Почему степень окисления рубидия всегда положительная?
- 4. Как определить степень окисления рубидия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления рубидия
- 6. Шпаргалка для рубидия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у рубидия постоянная степень окисления?
Причина стабильности рубидия — наличие единственного валентного электрона, который удерживается ядром очень слабо из-за большого расстояния от центра атома.
- В простом веществе (Rb⁰): Заряд равен 0. Конфигурация:
5s [↑]. - В ионе (Rb+1): Рубидий отдает 1 электрон с 5s-уровня. Конфигурация:
5s [ ](соответствует Kr).

Рис. 2. Процесс окисления рубидия: атом Rb теряет внешний электрон, превращаясь в стабильный катион рубидия (I).
Степень окисления рубидия в соединениях
Все соединения рубидия являются типичными солями или основаниями, где металл всегда имеет положительный заряд:
- Оксид рубидия (Rb2O): Rb +1, O -2.
- Гидроксид рубидия (RbOH): Rb +1 (сильнейшая щелочь).
- Хлорид рубидия (RbCl): Rb +1.
- Сульфат рубидия (Rb2SO4): Rb +1.
- Гидрид рубидия (RbH): Rb +1, H -1.
Высшая степень окисления
Высшая степень окисления рубидия равна +1. Она соответствует номеру его группы (IА) в таблице Менделеева.
Низшая степень окисления
Низшей степени окисления для рубидия (в плане отрицательных значений) не существует. В металлическом состоянии СО равна 0.
Важно: Рубидий настолько активен, что воспламеняется на воздухе, образуя не только оксид, но и надпероксид RbO2, где СО рубидия все равно остается +1.
Почему степень окисления рубидия всегда положительная?
Знак заряда зависит от крайне низкой электроотрицательности (ЭО) рубидия.
- Положительная СО (+): Рубидий — один из самых сильных восстановителей. Он всегда отдает электрон любому партнеру по реакции.
- Отрицательная СО (-): Невозможна для рубидия в обычных химических условиях.
- Нулевая СО (0): Характерна для чистого металлического рубидия (мягкий металл серебристо-белого цвета).
Как определить степень окисления рубидия
По таблице Менделеева
- Семейство: s-элемент (щелочные металлы).
- Валентные электроны: 1.
- Атомная масса рубидия: 85,46 а.е.м. Для сравнения масс других элементов используй таблицу атомных масс.
- Типичная СО: +1.
По валентности (Число связей)
Валентность рубидия всегда равна I.
- Валентность I: Соответствует СО +1.
- Пример: Rb2O. Здесь каждый атом рубидия образует по одной связи с кислородом.
По электронной конфигурации
- Электронная формула рубидия: [Kr] 5s1. Для просмотра квантовых чисел используй таблицу квантовых чисел.
- Наличие одного неспаренного электрона на удаленной 5s-орбитали делает его отдачу неизбежной в химических реакциях.
По химическому соединению (Алгебраический расчет)
Так как Рубидий — щелочной металл 1-й группы, его СО в сложных веществах всегда +1.
Это помогает находить СО других элементов, например, кислорода в сложных пероксидах.
Пример для Rb2SO4 (сульфат рубидия):
Сумма всех СО равна 0. Обозначим СО серы за x. Рубидий +1, кислород -2.
2 · (+1) + x + 4 · (-2) = 0
2 + x — 8 = 0 ⇒ x = +6
Примеры степеней окисления рубидия
| СО | Цвет соединений | Примеры соединений |
|---|---|---|
| +1 | Белый / Бесцветный (ионы Rb⁺ бесцветны) | RbOH, RbCl, Rb2CO3 |
| 0 | Серебристо-белый | Rb (Металлический рубидий) |
Шпаргалка для рубидия
- +1 — единственная степень окисления в любых солях и щелочах.
- Восстановитель — рубидий реагирует со взрывом даже со льдом.
- RbOH — одна из самых сильных щелочей, разрушающая стекло.
- Окраска пламени — ионы Rb⁺ окрашивают пламя в розово-фиолетовый цвет.
Пример решения задачи:
▶️ Дано:
Соединение: Rb2O.
⌕ Найти:
Определите СО рубидия.
✨ Решение:
Рубидий — элемент I группы главной подгруппы. В сложных соединениях он всегда проявляет СО +1.
✅ Ответ:
Rb(+1).
Проверка знаний
Отметьте правильные утверждения для Рубидия (Rb):
Показать ответы
Правильные ответы: 1, 3, 5.
Разбор ошибок:
2 — неверно: у рубидия только +1.
4 — неверно: в RbH у рубидия +1, а у водорода -1.
Часто задаваемые вопросы
Нет, рубидий — щелочной металл, его единственный валентный электрон на 5s-подуровне легко отрывается.
А для отрыва второго электрона потребовалось бы разрушить устойчивый внутренний слой, что невозможно в химических реакциях.
Рубидий обладает крайне низкой электроотрицательностью (0,82). Это означает, что он практически не способен удерживать свои электроны, не говоря уже о притягивании чужих.
Поэтому он всегда выступает только как донор электронов.
В надпероксиде рубидия СО металла остается стабильной и равна +1. Дробный формальный заряд приходится на атомы кислорода в супероксид-ионе.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.