Теория:
Степень окисления криптона (Kr) в подавляющем большинстве случаев равна 0. Это естественное состояние для благородных газов с полностью заполненной электронной оболочкой.
Значения +2 встречаются крайне редко и только в искусственно синтезированных соединениях с фтором (например, KrF2).
Другие степени окисления, такие как +4 или +6, теоретически предсказаны, но на практике не получены из-за колоссальной инертности элемента.
Криптон находится в 18-й группе (главная подгруппа VIII группы) и является p-элементом 4-го периода.
Как p-элемент, он обладает завершенной электронной конфигурацией [Ar] 3d104s24p6. В отличие от селена, у криптона внешний p-слой полностью укомплектован шестью электронами.
Криптон проявляет преимущественную степень окисления 0. Это связано с тем, что «октет» электронов обеспечивает атому максимальную энергетическую стабильность, исключая необходимость отдавать или принимать электроны в обычных условиях.
В отличие от более легких инертных газов (гелия, неона, аргона), криптон способен вступать в химические реакции при экстремальном воздействии, что сближает его по свойствам с ксеноном.
Чтобы определить возможные значения, используют электронную формулу.
Например:
- Для криптона (1s22s22p63s23p63d104s24p6) — завершенный слой делает СО 0 основной.
- Для селена (1s22s22p63s23p63d104s24p4) — нехватка двух электронов заставляет его проявлять активность, которой лишен криптон.
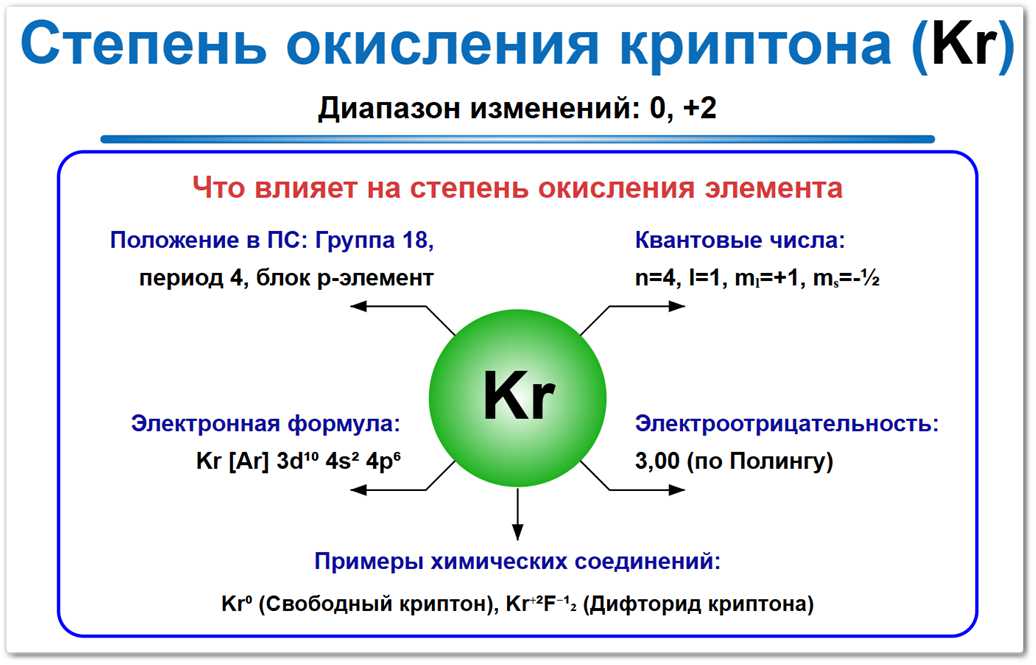
Рис. 1. Возможные степени окисления криптона: 0, +2. Это самый узкий диапазон среди элементов 4-го периода.
На их формирование влияют стабильное электронное строение (октет), положение в 18-й группе и очень высокая энергия ионизации.
Содержание страницы
- 1. Почему у криптона почти нет переменных степеней окисления?
- 2. Степень окисления криптона в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 3. Почему степень окисления почти всегда нулевая?
- 4. Как определить степень окисления криптона
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления криптона
- 6. Шпаргалка для криптона
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у криптона почти нет переменных степеней окисления?
Причина инертности криптона — отсутствие свободных орбиталей на внешнем уровне и прочное удержание своих электронов ядром.
- В простом веществе (Kr⁰): Заряд равен 0. Конфигурация:
4s [↑↓] 4p [↑↓][↑↓][↑↓]. Слой полностью закрыт. - В соединении (Kr+2): Под действием фтора происходит частичное возбуждение электронов, позволяющее образовать две ковалентные связи. Конфигурация условно меняется для участия в связи.

Рис. 2. Состояние криптона: атом Kr ([Ar] 3d10 4s2 4p6) крайне неохотно вступает в реакции, оставаясь в нейтральном состоянии.
Степень окисления криптона в соединениях
Количество соединений криптона крайне мало, и почти все они нестабильны при комнатной температуре:
- Дифторид криптона (KrF2): Kr +2, F -1 (сильнейший фторирующий агент).
- Соли катиона KrF+: Kr +2.
- Комплексы (например, [KrF][SbF6]): Kr +2.
- Клатбиты (соединения включения): Kr 0 (химическая связь отсутствует).
Высшая степень окисления
Высшая практически полученная степень окисления криптона равна +2. Формально, по номеру группы (VIII), она могла бы достигать +8, но для криптона это недостижимо.
Низшая степень окисления
Низшая равна 0. Отрицательных степеней окисления у криптона не существует, так как он не способен принимать дополнительные электроны.
Важно: Криптон — первый из благородных газов (по весу), для которого удалось получить твердое соединение, стабильное при низких температурах.
Почему степень окисления почти всегда нулевая?
Знак заряда и его наличие зависят от энергии ионизации.
- Нулевая СО (0): Электроны криптона находятся в идеальном балансе, энергия для их отрыва требуется колоссальная.
- Положительная СО (+): Проявляется только в паре с фтором (самым электроотрицательным элементом), который способен «вытянуть» электроны даже из инертного газа.
Как определить степень окисления криптона
По таблице Менделеева
- Семейство: p-элемент (инертные газы).
- Валентные электроны: 8 (полный октет).
- Атомная масса криптона: 83,79 а.е.м. Для сравнения масс используй таблицу атомных масс.
- Типичная СО: 0.
По валентности (Число связей)
Валентность криптона в обычном состоянии равна 0, очень редко в соединениях — II.
- Валентность II: Соответствует СО +2.
- Пример: KrF2. Криптон образует две связи с фтором.
По электронной конфигурации
- Электронная формула криптона: [Ar] 3d10 4s2 4p6. Используй таблицу квантовых чисел для анализа уровней.
- Заполненность всех орбиталей 4-го уровня (s и p) — главная причина химического «спокойствия» элемента.
По химическому соединению (Алгебраический расчет)
Для криптона расчет актуален только для фторидов.
Пример для KrF2 (дифторид криптона):
Сумма всех степеней окисления в молекуле равна 0.
Обозначим СО криптона за x, а у фтора она всегда -1.
1 · x + 2 · (-1) = 0
x — 2 = 0 ⇒ x = +2
Примеры степеней окисления криптона
| СО | Состояние | Примеры соединений |
|---|---|---|
| +2 | Белые кристаллы (нестабильны) | KrF2, [KrF]SbF6 |
| 0 | Бесцветный газ без запаха | Kr (Криптон в воздухе) |
Шпаргалка для криптона
- 0 — стандарт во всех условиях.
- +2 — возможно только в лаборатории при низких температурах.
- KrF₂ — единственное бинарное соединение, которое можно выделить.
- 18 группа — причина абсолютной стабильности.
Пример решения задачи:
▶️ Дано:
Соединение: KrF2.
⌕ Найти:
Определите СО криптона.
✨ Решение:
Фтор (F) — самый электроотрицательный элемент, его СО всегда -1. Уравнение: x + 2 · (-1) = 0 → x = +2.
✅ Ответ:
Kr(+2).
Проверка знаний
Отметьте правильные утверждения для Криптона (Kr):
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: криптон не имеет отрицательных степеней окисления.
Часто задаваемые вопросы
Низшая степень окисления: 0. Это самое стабильное состояние криптона как благородного газа (простое вещество).
Высшая степень окисления: +2. Проявляется в редких и химически активных соединениях, таких как дифторид криптона (KrF2).
Это связано с его завершенной электронной оболочкой (4s2 4p6). У атома криптона на внешнем слое уже находится максимально возможное число электронов (8), поэтому ему энергетически невыгодно принимать дополнительные частицы и проявлять отрицательный заряд.
Криптон может только отдавать электроны самым сильным окислителям (например, фтору), проявляя положительную степень окисления +2.
Это объясняется высоким потенциалом ионизации. Электроны криптона расположены ближе к ядру и удерживаются сильнее, чем у тяжелых инертных газов (ксенона или радона).
Энергии фтора хватает только на то, чтобы «раскачать» и задействовать два p-электрона, поэтому стабильные соединения со степенью +4, +6 или +8 для криптона пока не получены.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.