Теория:
Степень окисления олова (Sn) в большинстве соединений принимает значения +2, +4, значительно реже встречаются состояния 0.
Также существуют крайне нестабильные отрицательные степени окисления -4, которые проявляются только в специфических условиях (например, в станнидах щелочных и щелочноземельных металлов).
Например для высшей СО +4: в соединении SnO2 (диоксид олова) степень окисления металла равна +4.
Это происходит потому, что олово находится в 14-й группе и при взаимодействии с таким сильным окислителем, как кислород, оно задействует все свои 4 валентных электрона (5s2 5p2), достигая максимально возможного заряда для своей группы.
Для сравнения, отрицательная СО -4: встречается в таких соединениях, как Mg2Sn (станнид магния).
Здесь ситуация обратная: олово проявляет некоторые неметаллические свойства (как и его сосед по группе — углерод) и «принимает» электроны от менее электроотрицательного магния, заполняя свой внешний электронный слой до октета.
Такие состояния крайне нестабильны на влажном воздухе, так как олово стремится вернуться к положительному заряду или металлическому состоянию, которые для него энергетически естественнее.
Промежуточные же степени окисления, такие как +1 или +3, являются «неудобными» для атома и практически не встречаются в стабильных химических системах.
Обладая конфигурацией [Kr] 4d10 5s2 5p2, олову проще либо отдать два p-электрона (стабильная СО +2), либо все четыре валентных электрона (СО +4).
Именно поэтому соединения олова(II) являются хорошими восстановителями — они легко отдают оставшуюся пару 5s-электронов, переходя в более устойчивое состояние +4.
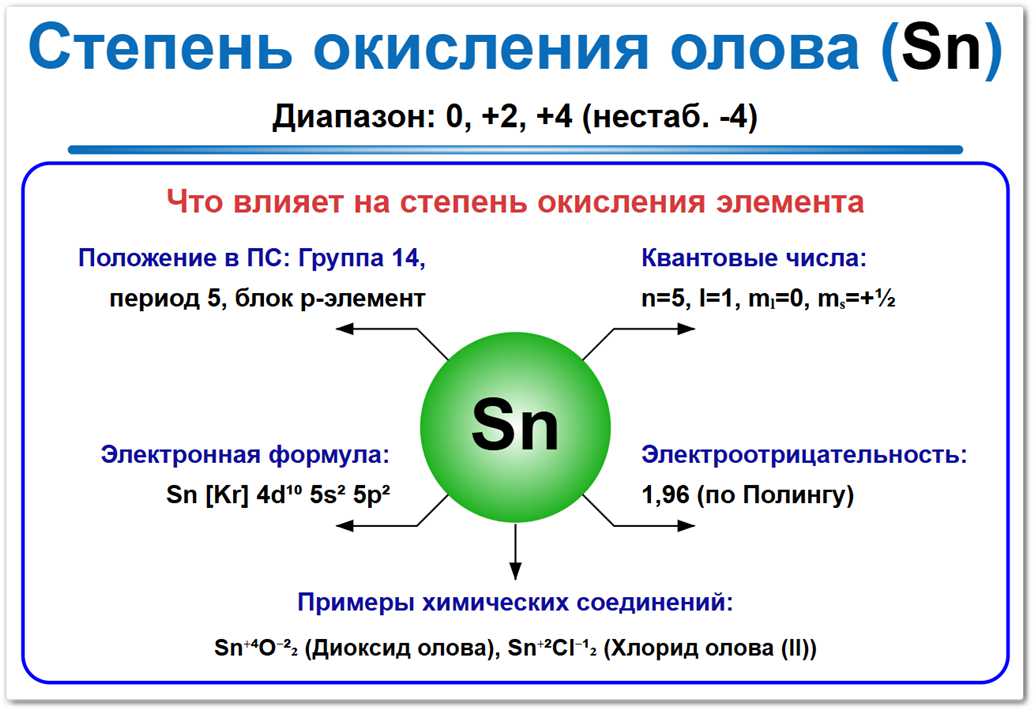
Рис. 1. Возможные степени окисления олова: от -4 до +4. Наиболее устойчивые формы — +2 (хлориды) и +4 (диоксид), характерная для наиболее стабильных минералов.
Обратите внимание, что химия олова во многом схожа с химией германия (Ge) и свинца (Pb), своих соседей по группе. Как и у свинца, у олова ярко выражен «эффект инертной пары», делающий состояние +2 весьма стабильным.
На их формирование влияют электронное строение (5s2 5p2), положение в 14-й группе и значение электроотрицательности 1,96 по шкале Полинга.
Содержание страницы
- 1. Почему у олова стабильная степень окисления?
- 2. Степень окисления олова в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления олова
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления олова
- 6. Шпаргалка для олова
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у олова стабильная степень окисления?
Причина стабильности высших состояний олова заключается в возможности полной отдачи всех p- и s-электронов внешнего слоя, что приводит к образованию устойчивой электронной конфигурации с заполненным 4d-подуровнем.
- В простом веществе (Sn⁰): Заряд равен 0. Конфигурация:
5s [↑↓] 5p [↑][↑][ ]. - В ионе (Sn+4): Олово отдает все 4 валентных электрона. Конфигурация:
[Kr] 4d10.

Рис. 2. Процесс окисления олова: от металлического состояния (белое олово) до высшего состояния +4 в составе оловянного камня (касситерита).
Степень окисления олова в соединениях
В зависимости от реагентов, олово в соединениях проявляет степень окисления, которая меняет характер связи с ионного на ковалентный:
- Диоксид олова (SnO2): Sn +4, O -2.
- Оксид олова(II) (SnO): Sn +2, O -2.
- Хлорид олова(IV) (SnCl4): Sn +4, Cl -1.
- Хлорид олова(II) (SnCl2): Sn +2, Cl -1.
- Станнид магния (Mg2Sn): Sn -4, Mg +2.
Высшая степень окисления
Высшая степень окисления олова равна +4. Это значение полностью соответствует номеру группы (IV или 14) в периодической системе и является наиболее характерным для природных кислородных соединений олова.
Низшая степень окисления
Для олова в соединениях с активными металлами возможна степень окисления -4, однако степень окисления олова равна 0 в металлическом виде — это основное состояние элемента в виде слитков или покрытий (лужение).
Промежуточные степени окисления
Степень окисления олова в веществах часто принимает значение +2. Соединения Sn(+2) являются сильными восстановителями и в водных растворах на воздухе постепенно окисляются до Sn(+4).
Важно: Состояние +4 в виде диоксида (SnO2) — это наиболее химически инертная форма. В то время как степень окисления олова формула соединения SnCl2 указывает на соль, которая широко используется в промышленности как протрава при крашении тканей.
Почему степень окисления чаще положительная?
Знак заряда определяется природой элемента как металла главных подгрупп:
- Положительная СО (+): Олово легче отдает свои внешние электроны неметаллам, приобретая стабильность.
- Нулевая СО (0): Характерна для чистого металла, существующего в виде нескольких аллотропных модификаций (белое и серое олово).
- Отрицательная СО (-): Встречается в станнидах, где олово выступает в роли окислителя по отношению к активным металлам.
Как определить степень окисления олова
По таблице Менделеева
- Семейство: p-элемент.
- Валентные электроны: 4 (2 на s-подуровне и 2 на p-подуровне).
- Атомная масса олова: 118,7 а.е.м.
По валентности (Число связей)
Как и у многих элементов IV группы, валентность олова может быть переменной, принимая значения II или IV.
- В диоксиде (SnO2): Атом олова образует четыре связи с кислородом (по две с каждым). Его валентность — IV, а степень окисления равна +4.
- В хлориде (SnCl2): Олово образует две связи с атомами хлора. Валентность — II, СО олова — +2.
По электронной конфигурации
- Электронная формула олова: [Kr] 4d10 5s2 5p2.
- Атому олова степени окисления +4 достичь выгодно при взаимодействии с сильными неметаллами, так как это освобождает весь 5-й энергетический уровень.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для Na2SnO3 (станнат натрия):
Сумма СО равна 0. Натрий всегда +1, Кислород -2. Обозначим Sn как x.
2 · (+1) + x + 3 · (-2) = 0
2 + x — 6 = 0 ⇒ x = +4
Примеры степеней окисления олова
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +4 | Высшая / Стабильная. Характерна для минералов и станнатов. | SnO2, SnCl4, Na2SnO3 |
| +2 | Устойчивая / Восстановитель. Широко используется в химии. | SnCl2, SnO, SnSO4 |
| 0 | Металл. Состояние чистого вещества. | Sn (белая жесть, припой) |
| -4 | Отрицательная. Встречается только в станнидах. | Mg2Sn, Ca2Sn |
Шпаргалка для олова
- +4 — самая устойчивая степень в природе (касситерит).
- Восстановитель — олово в СО +2 часто применяется для восстановления металлов из их растворов.
- Амфотерность — олово в обеих степенях окисления проявляет амфотерные свойства, растворяясь и в кислотах, и в щелочах.
Пример решения задачи:
▶️ Дано:
Соединение: SnCl4.
⌕ Найти:
Определите СО олова.
✨ Решение:
Хлор (Cl) как более электроотрицательный элемент в соединении с металлом имеет СО -1. Уравнение: x + 4 · (-1) = 0 → x — 4 = 0 → x = +4.
✅ Ответ:
Sn(+4).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: соединения олова(II), напротив, являются типичными восстановителями, так как стремятся перейти в состояние +4.
Часто задаваемые вопросы
В обычных условиях наиболее стабильна степень окисления +4, хотя соединения +2 также весьма устойчивы в твердом виде.
Нет, так как у олова всего 4 валентных электрона на внешнем уровне.
Потому что его оксиды и гидроксиды (в степенях +2 и +4) способны реагировать как с кислотами, так и с сильными основаниями.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.