Теория:
Степень окисления мышьяка (As) в наиболее устойчивых соединениях принимает значения -3, +3 и +5.
В отличие от германия, мышьяк — это типичный неметалл, что определяет его склонность к захвату электронов.
Значения 0, +3 и +5 встречаются чаще всего. Состояние +3 характерно для оксида As2O3, который проявляет амфотерные свойства, а состояние +5 соответствует высшей окислительной способности элемента.
Мышьяк находится в 15-й группе (главная подгруппа V группы) и является p-элементом 4-го периода.
Как p-элемент, он обладает электронной конфигурацией [Ar] 3d104s24p3. На его внешнем p-слое находится три неспаренных электрона, что делает его активным участником химических реакций.
Мышьяк проявляет преимущественные степени окисления +3 и +5.
Это связано с возможностью атома задействовать либо только три p-электрона, либо все пять валентных электронов (два 4s и три 4p) для образования связей.
В отличие от азота, мышьяк легче переходит в состояние +5, однако его высшие оксиды являются более сильными окислителями, чем аналогичные соединения фосфора.
Чтобы определить возможные значения, используют электронную формулу.
Например:
- Для мышьяка (1s22s22p63s23p63d104s24p3) — потеря всех пяти внешних электронов дает СО +5, а присоединение трех электронов до октета дает СО -3.
- Для германия (1s22s22p63s23p63d104s24p2) — наличие только двух p-электронов ограничивает его способность к захвату электронов по сравнению с мышьяком.
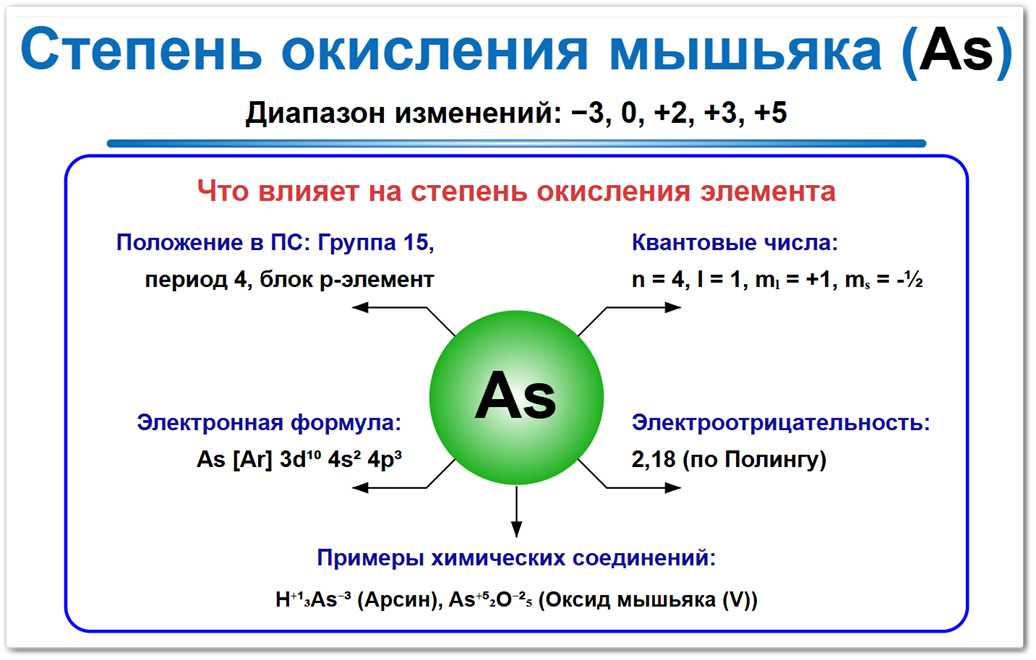
Рис. 1. Возможные степени окисления мышьяка: -3, 0, +3, +5. Также в редких случаях он может проявлять СО +2 или +4 в нестабильных комплексах.
На их формирование влияют электронное строение (три p-электрона), положение в 15-й группе и значение электроотрицательности 2,18 по шкале Полинга.
Содержание страницы
- 1. Почему у мышьяка переменные степени окисления?
- 2. Степень окисления мышьяка в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 3. Почему степень окисления может быть положительной или отрицательной?
- 4. Как определить степень окисления мышьяка
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления мышьяка
- 6. Шпаргалка для мышьяка
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у мышьяка переменные степени окисления?
Причина гибкости мышьяка — наличие пяти валентных электронов, которые могут либо уходить к более электроотрицательным атомам, либо дополняться до полной оболочки.
- В простом веществе (As⁰): Заряд равен 0. Конфигурация:
4s [↑↓] 4p [↑][↑][↑]. - В ионе (As+3): Мышьяк отдает 3 электрона с 4p-уровня. Конфигурация
4s [↑↓] 4p [ ][ ][ ]. - В ионе (As+5): Мышьяк отдает все 5 валентных электронов. Конфигурация
4s [ ] 4p [ ][ ][ ].

Рис. 2. Процесс окисления мышьяка: атом As ([Ar] 3d10 4s2 4p3) теряет внешние электроны, достигая различных устойчивых состояний.
Степень окисления мышьяка в соединениях
Соединения мышьяка подчеркивают его неметаллический характер и высокую токсичность во всех формах:
- Оксид мышьяка(V) (As2O5): As +5, O -2.
- Оксид мышьяка(III) (As2O3): As +3, O -2.
- Арсенат натрия (Na3AsO4): As +5.
- Сульфид мышьяка(III) (As2S3): As +3, S -2.
- Арсин (AsH3): As -3, H +1 (крайне ядовитый газ).
Высшая степень окисления
Высшая степень окисления мышьяка равна +5. Она соответствует номеру его группы (VА) в таблице Менделеева.
Низшая степень окисления
Низшая равна -3. Она проявляется в соединениях с водородом (арсинах) и металлами (арсенидами).
Важно: Отрицательная степень окисления -3 для мышьяка является очень устойчивой, что сближает его по химическим свойствам с фосфором.
Почему степень окисления может быть положительной или отрицательной?
Знак заряда зависит от разности электроотрицательности (ЭО).
- Положительная СО (+): Мышьяк отдает электроны кислороду, сере или фтору (ЭО As = 2,18).
- Отрицательная СО (-): Проявляется в соединениях с водородом (AsH₃) или металлами (GaAs — арсенид галлия), где мышьяк выступает как окислитель.
- Нулевая СО (0): Характерна для серого (металлического), желтого или черного мышьяка.
Как определить степень окисления мышьяка
По таблице Менделеева
- Семейство: p-элемент (группа азота).
- Валентные электроны: 5 (2 на s-уровне и 3 на p-уровне).
- Атомная масса мышьяка: 74,92 а.е.м. Для сравнения масс других элементов используй таблицу атомных масс.
- Типичные СО: +3, +5.
По валентности (Число связей)
Валентность мышьяка чаще всего равна III или V.
- Валентность V: Соответствует высшей СО +5.
- Пример: As2O5. Здесь мышьяк пятивалентен.
По электронной конфигурации
- Электронная формула мышьяка: [Ar] 3d10 4s2 4p3. Для просмотра квантовых чисел используй таблицу квантовых чисел.
- Наличие трех p-электронов объясняет стабильность СО +3, а вовлечение всей оболочки — СО +5.
По химическому соединению (Алгебраический расчет)
Высшая степень окисления мышьяка в сложных веществах с кислородом равна +5.
Это помогает находить СО других элементов. Рассмотрим пример с расчетом неизвестного значения.
Пример для H3AsO4 (мышьяковая кислота):
Сумма всех СО равна 0. Обозначим СО мышьяка за x. У водорода она +1, у кислорода -2.
3 · (+1) + 1 · x + 4 · (-2) = 0
3 + x — 8 = 0 ⇒ x = +5
Примеры степеней окисления мышьяка
| СО | Цвет соединений | Примеры соединений (с индексами) |
|---|---|---|
| +5 | Белый (кристаллический) | As2O5, Na3AsO4 |
| +3 | Белый / Желтый | As2O3, AsCl3, As2S3 |
| 0 | Серый / Черный | As (Мышьяк) |
| -3 | Бесцветный газ | AsH3, GaAs, AlAs |
Шпаргалка для мышьяка
- -3 — крайне ядовитый газ арсин (AsH3).
- +3 — белый мышьяк (As2O3), классический яд и реактив.
- +5 — высшая форма, соли которой называются арсенатами.
- Металлические свойства — серый мышьяк проводит ток, хотя химически остается неметаллом.
Пример решения задачи:
▶️ Дано:
Соединение: As2O3.
⌕ Найти:
Определите СО мышьяка.
✨ Решение:
Кислород (O) имеет СО −2. Следовательно: 2 · x + 3 · (−2) = 0 → 2x = 6 → x = +3.
✅ Ответ:
As(+3).
Проверка знаний
Отметьте правильные утверждения для Мышьяка (As):
Показать ответы
Правильные ответы: 1, 3, 5.
Разбор ошибок:
2 — неверно: низшая СО равна -3.
4 — неверно: арсин чрезвычайно ядовит.
Часто задаваемые вопросы
Арсениты — это соли мышьяковистой кислоты (As +3), а арсенаты — соли мышьяковой кислоты (As +5). Арсенаты обычно более стабильны.
Способность мышьяка (As) проявлять как положительные, так и отрицательные степени окисления обусловлена его положением в таблице Менделеева и особенностями строения его атома.
Отрицательные степени окисления: Чтобы полностью заполнить внешний электронный слой до стабильного состояния (октета), атому мышьяка не хватает 3 электронов.
При взаимодействии с менее электроотрицательными элементами (например, металлами или водородом) мышьяк притягивает эти 3 электрона к себе.
Положительные степени окисления: При взаимодействии с более электроотрицательными элементами (кислород, фтор, хлор) мышьяк, наоборот, отдает свои электроны.
Наиболее устойчивой степенью окисления мышьяка является +3.
Это обусловлено «эффектом инертной электронной пары»: паре электронов на 4s-подуровне энергетически выгоднее оставаться при атоме, чем участвовать в образовании связей.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.