Теория:
Степень окисления индия (In) в большинстве соединений принимает значение +3, значительно реже встречаются состояния +1 и +2.
Также существуют крайне нестабильные 0 (в газообразном состоянии), отрицательных степеней не образует потому, что он типичный металл, а металлы не образуют таких СО.
Которые проявляются только в специфических условиях (например, в некоторых интерметаллидах со щелочными металлами).
Например для высшей СО +3: в соединении In2O3 (оксид индия) степень окисления металла равна +3.
Это происходит потому, что индий находится в 13-й группе и при взаимодействии с окислителями он задействует все свои 3 валентных электрона (5s2 5p1), достигая максимально стабильного для него положительного заряда.
Для сравнения, низшая СО +1: встречается в таких соединениях, как InCl (хлорид индия I).
Здесь ситуация иная: из-за эффекта «инертной пары» s-электронов, индий отдает только один p-электрон.
Это состояние более характерно для индия, чем для его соседа сверху — галлия, так как с увеличением порядкового номера s-электроны прочнее удерживаются ядром.
Такие состояния (+1) часто неустойчивы в водных растворах и стремятся окислиться до +3 или диспропорционировать до металла и высшего оксида.
Промежуточные же степени окисления, такие как +2, являются «неудобными» для атома.
Обладая конфигурацией [Kr] 4d10 5s2 5p1, индию проще либо отдать один электрон, либо сразу три. Состояние +2 обычно реализуется в соединениях со связью металл-металл (In-In).
Именно поэтому промежуточные соединения часто склонны к превращениям — они самопроизвольно переходят в более устойчивые формы в зависимости от среды.
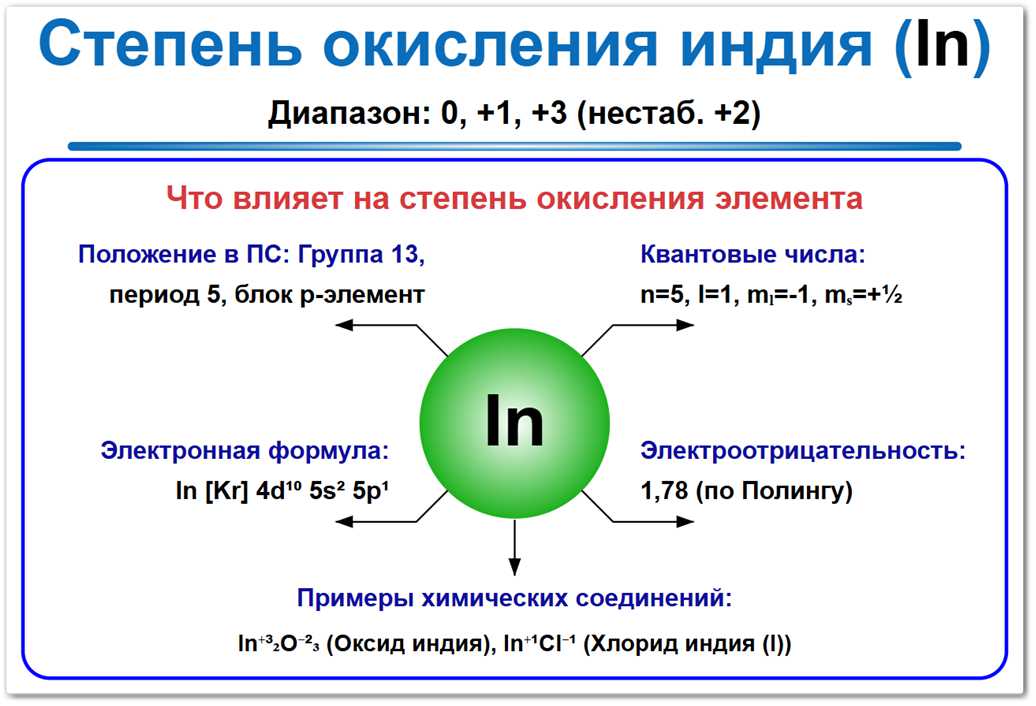
Рис. 1. Возможные степени окисления индия: от 0 до +3. Наиболее устойчивая форма — +3 (оксиды, сульфаты), состояние +1 характерно для некоторых галогенидов.
Содержание страницы
- 1. Почему у индия стабильная степень окисления?
- 2. Степень окисления индия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления индия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления индия
- 6. Шпаргалка для индия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у индия стабильная степень окисления?
Причина стабильности высшего состояния индия (+3) заключается в возможности полностью освободить 5s- и 5p-орбитали, оставляя под ними устойчивую заполненную 4d10 оболочку.
- В простом веществе (In⁰): Заряд равен 0. Конфигурация:
5s [↑↓] 5p [↑][ ][ ]. - В ионе (In+3): Индий отдает все 3 валентных электрона. Конфигурация:
[Kr] 4d10.

Рис. 2. Процесс окисления индия: от металлического состояния до наиболее устойчивого состояния +3 в составе большинства солей.
Степень окисления индия в соединениях
В зависимости от реагентов, индий в соединениях проявляет степень окисления, которая меняет характер связи и физические свойства:
- Оксид индия(III) (In2O3): In +3, O -2.
- Хлорид индия(I) (InCl): In +1, Cl -1.
- Сульфид индия(III) (In2S3): In +3, S -2.
- Нитрат индия(III) (In(NO3)3): In +3.
- Дибромид индия (InBr2): In +1 и +3 (фактически In[InBr4]).
Высшая степень окисления
Высшая степень окисления индия равна +3. Это значение полностью соответствует номеру группы (13 или III-A) в периодической системе и является пределом для данного элемента в обычных условиях.
Низшая степень окисления
Для индия в редких интерметаллидах возможны степени окисления -1 и -2, однако степень окисления индия равна 0 в металлическом виде — это наиболее типичное низшее состояние для этого мягкого металла.
Промежуточные степени окисления
Степень окисления индия в веществах часто принимает значение +1, особенно в высокотемпературных фазах, но такие формы менее стабильны по сравнению с +3 и легко окисляются.
Важно: Состояние +3 в виде оксида (In2O3) — это наиболее коммерчески важная форма индия, используемая для создания прозрачных проводящих покрытий (ITO), где степень окисления индия формула соединения всегда +3.
Почему степень окисления чаще положительная?
Знак заряда определяется металлической природой элемента и его положением в таблице:
- Положительная СО (+): Индий отдает электроны неметаллам, так как обладает типичными свойствами металлов подгруппы алюминия.
- Нулевая СО (0): Характерна для чистого металла (слитки, фольга).
- Отрицательная СО (-): Встречается крайне редко, только в соединениях с очень активными металлами.
Как определить степень окисления индия
По таблице Менделеева
- Семейство: p-элемент.
- Валентные электроны: 3 (2 на s-подуровне и 1 на p-подуровне).
- Атомная масса индия: 114,8 а.е.м.
По валентности (Число связей)
В отличие от щелочных металлов, валентность индия может быть переменной, хотя чаще всего она равна III.
- В оксиде (In2O3): Каждый атом индия образует три связи с кислородом. Его валентность — III, а степень окисления равна +3.
- В монохлориде (InCl): Индий образует одну связь с хлором. Валентность — I, СО индия — +1.
По электронной конфигурации
- Электронная формула индия: [Kr] 4d10 5s2 5p1.
- Атому индия степени окисления +3 достичь выгодно, так как это полностью очищает пятый энергетический уровень.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для In2(SO4)3 (сульфат индия):
Сумма СО равна 0. Сульфат-ион (SO4) целиком имеет заряд -2. Обозначим In как x.
2 · x + 3 · (-2) = 0
2x — 6 = 0 ⇒ x = +3
Примеры степеней окисления индия
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +3 | Высшая / Типичная. Основная химия индия. | In2O3, InCl3, In(OH)3 |
| +1 | Низкая. Характерна для галогенидов при недостатке окислителя. | InCl, InBr, In2O (черный) |
| +2 | Промежуточная. Часто встречается в смешанных валентностях. | InCl2 (In[InCl4]), InS |
| 0 | Металл. Состояние чистого вещества. | In (пластичный металл) |
Шпаргалка для индия
- +3 — высшая и самая устойчивая степень, встречается в большинстве минералов.
- Эффект инертной пары — причина появления устойчивых соединений индия в СО +1.
- Цвет — многие соли индия (+3) бесцветны, но оксид In2O3 имеет желтоватый оттенок.
Пример решения задачи:
▶️ Дано:
Соединение: InCl3 (хлорид индия III).
⌕ Найти:
Определите СО индия.
✨ Решение:
Хлор (Cl) обычно равен -1. Уравнение: x + 3 · (-1) = 0 → x — 3 = 0 → x = +3.
✅ Ответ:
In(+3).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 3, 5.
Разбор ошибок:
4 — неверно: оксид индия(III) имеет формулу In₂O₃, так как кислород имеет заряд -2, а индий +3.
Часто задаваемые вопросы
Наиболее стабильной и часто встречающейся является степень окисления +3.
Да, это возможно в некоторых соединениях (например, InCl), и это состояние становится всё более устойчивым у тяжелых элементов 13-й группы.
Это связано с наличием трех валентных электронов и возможностью s-электронов оставаться неспаренными (эффект инертной пары).

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.