Теория:
Основная степень окисления европия (Eu) — +3, значительной особенностью является относительно высокая стабильность степени окисления +2 по сравнению с большинством лантаноидов (наряду с иттербием).
В металлическом состоянии степень окисления европия равна 0.
В отличие от многих других редкоземельных элементов, для европия состояние +2 является аномально стабильным, что объясняется особенностями строения его электронной оболочки.
Например для характерной СО +3: в соединении Eu2O3 (оксид европия III) степень окисления металла равна +3.
Это происходит потому, что европий стремится отдать три валентных электрона (два с 6s-подуровня и один с 4f-подуровня).
Формируя устойчивую конфигурацию, типичную для большинства элементов своего семейства.
Для сравнения, стабильная СО +2: встречается в таких соединениях, как EuCl2 (хлорид европия II).
Здесь ситуация иная: европий отдает только два электрона с внешнего уровня.
Это состояние энергетически выгодно, так как при потере двух электронов у атома остается наполовину заполненная 4f-орбиталь (4f7).
Согласно правилу Хунда, такая симметричная конфигурация обладает повышенной устойчивостью.
Такие состояния (+2) являются сильными восстановителями, так как металл может окисляться до +3, но в безвоздушной среде они могут существовать длительное время.
Промежуточные же степени окисления для европия практически не встречаются в виде стабильных фаз.
Обладая конфигурацией [Xe] 4f7 6s2, европию проще всего либо сохранить «магическое» число электронов на f-слое (7 штук), либо перейти к стандартному для лантаноидов состоянию +3.
Именно поэтому химия европия часто рассматривается через призму конкуренции между этими двумя устойчивыми состояниями.
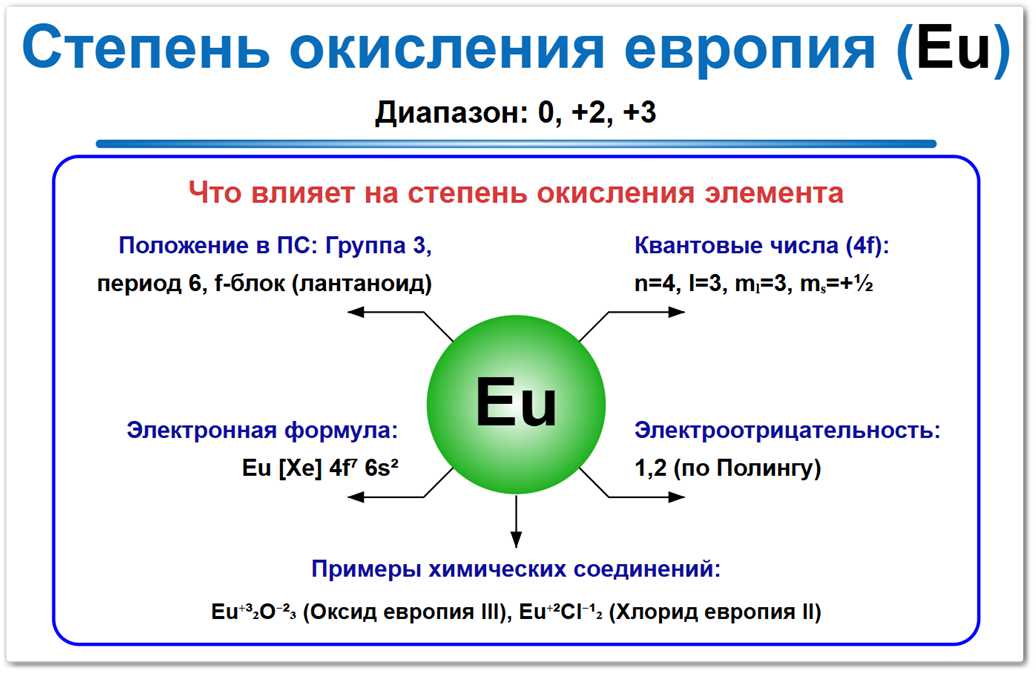
Рис. 1. Возможные степени окисления европия: наиболее устойчивые формы — +3 (оксиды) и +2 (галогениды), что выделяет его на фоне соседей по группе.
Обратите внимание, что химия европия (II) во многом напоминает химию щелочноземельных металлов, например бария (Ba).
Это проявляется в растворимости некоторых солей и схожих радиусах ионов.
На формирование его степеней окисления влияют электронное строение (4f7 6s2), положение в середине ряда лантаноидов и значение электроотрицательности 1,2 по шкале Полинга.
Содержание страницы
- 1. Почему у европия стабильная степень окисления?
- 2. Степень окисления европия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления европия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления европия
- 6. Шпаргалка для европия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у европия стабильная степень окисления?
Причина стабильности состояния +2 заключается в достижении конфигурации 4f7, которая является наполовину заполненной и обладает пониженной энергией.
- В простом веществе (Eu0): Заряд равен 0. Конфигурация:
[Xe] 4f7 6s2. - В ионе (Eu+2): Европий отдает 2 электрона. Конфигурация:
[Xe] 4f7.

Рис. 2. Процесс окисления европия: переход от нейтрального атома к ионам +2 и +3 за счет потери электронов с 6s и 4f уровней.
Степень окисления европия в соединениях
В зависимости от условий синтеза, европий в соединениях проявляет степень окисления, которая меняет не только химические, но и магнитные свойства:
- Оксид европия(III) (Eu2O3): Eu +3, O -2.
- Монооксид европия (EuO): Eu +2, O -2.
- Сульфид европия(II) (EuS): Eu +2.
- Хлорид европия(III) (EuCl3): Eu +3.
- Фторид европия(II) (EuF2): Eu +2.
Высшая степень окисления
Высшая степень окисления европия равна +3. В отличие от церия или тербия, европий не проявляет степени окисления +4, так как для этого потребовалось бы разрушить очень устойчивый наполовину заполненный f-подуровень.
Низшая степень окисления
Для европия наиболее важной низшей степенью окисления является +2, однако степень окисления европия равна 0 в чистом металлическом состоянии, которое является исходным для всех реакций.
Промежуточные степени окисления
Степень окисления европия в веществах иногда может казаться дробной в сложных смешанных оксидах (например, Eu3O4), но фактически это сочетание ионов Eu+2 и Eu+3 в одной кристаллической решетке.
Важно: Способность европия легко переходить в состояние +2 используется для его отделения от других редкоземельных металлов, у которых это состояние гораздо менее стабильно.
Почему степень окисления чаще положительная?
Знак заряда определяется низкой электроотрицательностью металла и его активным характером:
- Положительная СО (+): Европий отдает электроны неметаллам, стремясь к стабильной электронной конфигурации.
- Нулевая СО (0): Характерна для мягкого, серебристого металла.
- Отрицательная СО (-): Как и для других лантаноидов, отрицательные состояния для европия не характерны и не встречаются в обычных условиях.
Как определить степень окисления европия
По таблице Менделеева
- Семейство: Лантаноиды.
- Валентные электроны: 9 (7 на 4f и 2 на 6s подуровнях).
- Атомная масса европия: 152 а.е.м.
По валентности (Число связей)
В отличие от большинства соседей, валентность европия часто принимает значение II наряду с типичным III.
- В оксиде (Eu2O3): Атом европия проявляет валентность III, что соответствует степени окисления +3.
- В монооксиде (EuO): Европий образует связи, соответствующие валентности II, а его СО равна +2.
По электронной конфигурации
- Электронная формула европия: [Xe] 4f7 6s2.
- Атому европия степени окисления +2 достичь энергетически «приятно», так как остается стабильный слой 4f7.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для EuCl2 (хлорид европия II):
Сумма СО равна 0. Хлор всегда -1. Обозначим Eu как x.
x + 2 · (-1) = 0 ⇒ x — 2 = 0 ⇒ x = +2
Примеры степеней окисления европия
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +3 | Высшая/Стабильная. Типичная форма для лантаноидов. | Eu2O3, EuCl3, EuF3 |
| +2 | Уникальная. Обладает стабильностью благодаря слою 4f7. | EuO, EuCl2, EuSO4 |
| 0 | Металл. Простое вещество. | Eu (кусок металла) |
Шпаргалка для европия
- +2 и +3 — две главные степени окисления, определяющие всю химию элемента.
- Люминесценция — ионы европия (+3 — красный, +2 — синий) используются в производстве люминофоров для экранов.
- Магнетизм — европий в СО +2 обладает сильными парамагнитными свойствами.
Пример решения задачи:
▶️ Дано:
Соединение: EuSO4 (сульфат европия II).
⌕ Найти:
Определите СО европия.
✨ Решение:
Сульфат-ион (SO4) имеет общий заряд -2. Уравнение: x + (-2) = 0 ⇒ x = +2.
✅ Ответ:
Eu(+2).
Проверка знаний
Показать ответы
Правильные ответы: 1, 3, 4.
Разбор ошибок:
2 — неверно: +3 — это самая обычная и стабильная степень окисления для европия.
5 — неверно: высшая СО европия — +3, переход к более высоким зарядам энергетически невозможен.
Часто задаваемые вопросы
В водных растворах и большинстве минералов наиболее стабильна степень окисления +3, хотя +2 необычайно устойчива для f-элемента.
У него нет отрицательных степеней окисления по двум основным причинам:
1. Низкая электроотрицательность (1.2 по Полингу): Eu — это типичный активный металл. Он гораздо охотнее отдает свои электроны другим элементам, чем притягивает чужие.
2. Энергетика уровней: Европию энергетически выгодно избавиться от двух электронов с внешнего 6s2-слоя (образуя Eu2+) или еще одного с d-подуровня (образуя Eu3+), чтобы достичь стабильной полузаполненной f-оболочки (4f7).
Ионы европия (III) могут выступать в роли слабых окислителей, переходя в состояние +2.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.