Теория:
Степень окисления церия в большинстве соединений принимает значения +3 и +4, значительно реже встречается состояние +2.
В отличие от многих других лантаноидов, церий уникален тем, что легко переходит в состояние +4, которое является для него весьма стабильным в определенных условиях.
Например для высшей СО +4: в соединении CeO2 (диоксид церия) степень окисления металла равна +4.
Это происходит потому, что церий относится к семейству лантаноидов и при взаимодействии с сильным окислителем, таким как кислород.
Он задействует свои валентные электроны с 4f, 5d и 6s подуровней (4f1 5d1 6s2), достигая максимально возможного заряда и устойчивой электронной конфигурации инертного газа ксенона.
Для сравнения, редкая СО +2: встречается в таких экзотических соединениях, как CeI2 (иодид церия II).
Здесь ситуация иная: церий отдает только электроны с внешнего 6s-слоя, сохраняя электронную плотность на внутренних орбиталях.
Такие состояния крайне нестабильны и являются сильными восстановителями, так как металл стремится перейти в более естественное для него состояние +3.
Такие соединения легко окисляются на воздухе или при контакте с водой, возвращаясь к положительному заряду, который энергетически выгоднее.
Промежуточные же или дробные степени окисления для церия практически не характерны, так как атом «предпочитает» либо стабильную конфигурацию f1 (в состоянии +3), либо полностью пустую f-орбиталь (в состоянии +4).
Обладая конфигурацией [Xe] 4f1 5d1 6s2, церию проще всего достичь устойчивости, полностью освободив валентные слои.
Именно поэтому соединения церия(IV) являются мощными окислителями — они стремятся захватить один электрон, чтобы вернуться к очень стабильному состоянию +3.
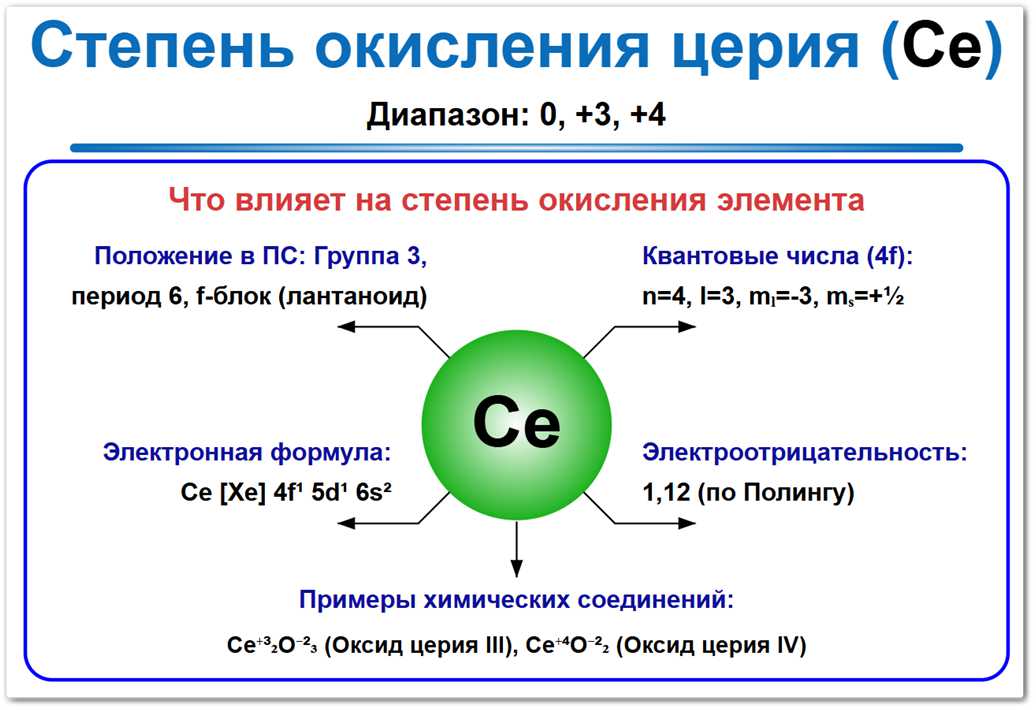
Рис. 1. Возможные степени окисления церия: наиболее устойчивые формы — +3 (типичная для лантаноидов) и +4 (характерная для цериевой подгруппы).
Содержание страницы
- 1. Почему у церия стабильная степень окисления?
- 2. Степень окисления церия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления церия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления церия
- 6. Шпаргалка для церия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у церия стабильная степень окисления?
Причина стабильности высшего состояния церия (+4) заключается в возможности полностью освободить 4f, 5d и 6s орбитали, что приводит к достижению электронной конфигурации инертного газа ксенона.
- В простом веществе (Ce⁰): Заряд равен 0. Конфигурация:
[Xe] 4f¹ 5d¹ 6s². - В ионе (Ce+4): Церий отдает все 4 валентных электрона. Конфигурация:
[Xe].

Рис. 2. Процесс окисления церия: переход от металлического состояния к наиболее устойчивому катиону Ce3+ или высшему Ce4+.
Степень окисления церия в соединениях
В зависимости от реагентов, церий в соединениях проявляет степень окисления, которая определяет его химическую активность:
- Диоксид церия (CeO2): Ce +4, O -2.
- Оксид церия(III) (Ce2O3): Ce +3, O -2.
- Сульфат церия(IV) (Ce(SO4)2): Ce +4.
- Хлорид церия(III) (CeCl3): Ce +3.
- Нитрат церия(III)-аммония ( (NH4)2[Ce(NO3)6] ): Ce +4.
Высшая степень окисления
Высшая степень окисления церия равна +4. Это состояние выделяет его среди других лантаноидов и позволяет использовать соединения церия в качестве сильных окислителей в органическом синтезе.
Низшая степень окисления
Для церия в редких комплексах возможна степень окисления +2, однако степень окисления церия равна 0 в металлическом виде — это наиболее типичное низшее состояние для большинства расчетов и промышленного применения.
Промежуточные степени окисления
Степень окисления церия в веществах чаще всего принимает значение +3.
Это «стандартное» состояние для всех редкоземельных элементов, которое является термически и химически устойчивым в большинстве водных сред.
Важно: Состояние +4 в виде диоксида (CeO2) — это наиболее распространенная и термически стабильная форма, где степень окисления церия формула соединения всегда +4. Диоксид церия широко применяется как абразив и катализатор.
Почему степень окисления чаще положительная?
Знак заряда определяется металлической природой лантаноида и его низкой электроотрицательностью:
- Положительная СО (+): Церий легко отдает электроны сильным неметаллам, достигая стабильных оболочек.
- Нулевая СО (0): Характерна для чистого металла (мишметалл).
- Отрицательная СО (-): Для церия практически невозможна в обычных химических условиях из-за его высокой активности как восстановителя.
Как определить степень окисления церия
По таблице Менделеева
- Семейство: f-элемент (лантаноид).
- Валентные электроны: 4 (1 на f, 1 на d и 2 на s-подуровне).
- Атомная масса церия: 140 а.е.м.
По валентности (Число связей)
В отличие от многих металлов, валентность церия может меняться. В стабильных соединениях она чаще всего равна III или IV.
- В диоксиде (CeO2): Атом церия образует четыре связи с кислородом. Его валентность — IV, а степень окисления равна +4.
- В хлориде (CeCl3): Церий образует три связи с хлором. Валентность — III, СО церия — +3.
По электронной конфигурации
- Электронная формула церия: [Xe] 4f1 5d1 6s2.
- Атому церия степени окисления +4 достичь выгодно, так как это полностью освобождает внешний валентный слой, переводя его в состояние иона с оболочкой ксенона.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для Ce2(SO4)3 (сульфат церия III):
Сумма СО равна 0. Сульфат-ион (SO4) всегда имеет заряд -2. Обозначим Ce как x.
2 · x + 3 · (-2) = 0
2x — 6 = 0 ⇒ x = +3
Примеры степеней окисления церия
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +4 | Высшая. Сильный окислитель, используется в катализаторах. | CeO2, Ce(SO4)2 |
| +3 | Стабильная. Типичная для большинства солей. | CeCl3, Ce2O3, Ce(NO3)3 |
| +2 | Низкая. Редкая, сильный восстановитель. | CeI2, CeS |
| 0 | Металл. Состояние чистого элемента. | Ce (слиток) |
Шпаргалка для церия
- +4 — высшая степень, проявляется в желтом CeO2.
- Окислитель — церий в СО +4 широко применяется в титровании для определения восстановителей.
- Цвет — соединения церия(III) обычно бесцветны, а соединения церия(IV) окрашены в желтый или оранжевый цвета.
Пример решения задачи:
▶️ Дано:
Соединение: CeO2 (диоксид церия).
⌕ Найти:
Определите СО церия.
✨ Решение:
Кислород (O) равен -2. Уравнение: x + 2 · (-2) = 0 → x — 4 = 0 → x = +4.
✅ Ответ:
Ce(+4).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: церий(IV) является мощным окислителем, так как стремится принять электрон и перейти в стабильное состояние +3.
Часто задаваемые вопросы
Наиболее стабильной и распространенной в большинстве природных условий является степень окисления +3.
Да, это его высшая и весьма важная степень окисления, которая делает его уникальным среди лантаноидов.
Является типичным активным металлом, и отсутствие у него отрицательных степеней окисления объясняется следующими причинами:
Низкая электроотрицательность.
Энергетическая выгода: Атому церия энергетически выгоднее отдать 3 или 4 электрона.
Природа лантаноидов: Все элементы семейства лантаноидов проявляют только положительные степени окисления

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.