Теория:
Степень окисления самария (Sm) в большинстве соединений принимает значение +3, однако для этого элемента также весьма характерно состояние +2.
А так же имеет СО равную 0 сам химический элемент.
В отличие от многих других лантаноидов, самарий обладает уникальной способностью стабилизировать низшие состояния окисления, что делает его важным реагентом в органическом синтезе.
Например для наиболее устойчивой СО +3: в соединении Sm2O3 (оксид самария III) степень окисления металла равна +3.
Это происходит потому, что самарий, как типичный редкоземельный элемент, при взаимодействии с окислителями легко отдает три электрона (два с 6s-подуровня и один с 4f-подуровня).
Достигая стабильного энергетического состояния, характерного для большинства лантаноидов.
Для сравнения, важная СО +2: встречается в таких соединениях, как SmI2 (иодид самария II).
Здесь ситуация иная: самарий отдает только два внешних 6s-электрона, сохраняя конфигурацию 4f6.
Это состояние является мощным восстановителем, так как атом стремится перейти к более выгодной «трехэлектронной» потере.
Такие соединения, как реагент Кагана (SmI2), широко используются в химии для проведения специфических реакций восстановления, где самарий активно «отдает» избыточный электрон субстрату, возвращаясь к заряду +3.
Высшие же степени окисления, такие как +4, для самария нехарактерны и крайне неустойчивы, в отличие от того же церия.
Обладая конфигурацией [Xe] 4f6 6s2, самарию проще всего работать в диапазоне от +2 до +3.
Попытка забрать большее количество электронов из f-слоя требует огромных затрат энергии, которые не компенсируются образованием новых связей.
Именно поэтому химия самария сосредоточена вокруг перехода между двух- и трехзарядными ионами, что сопровождается ярким изменением цвета растворов (от кроваво-красного до желтого).
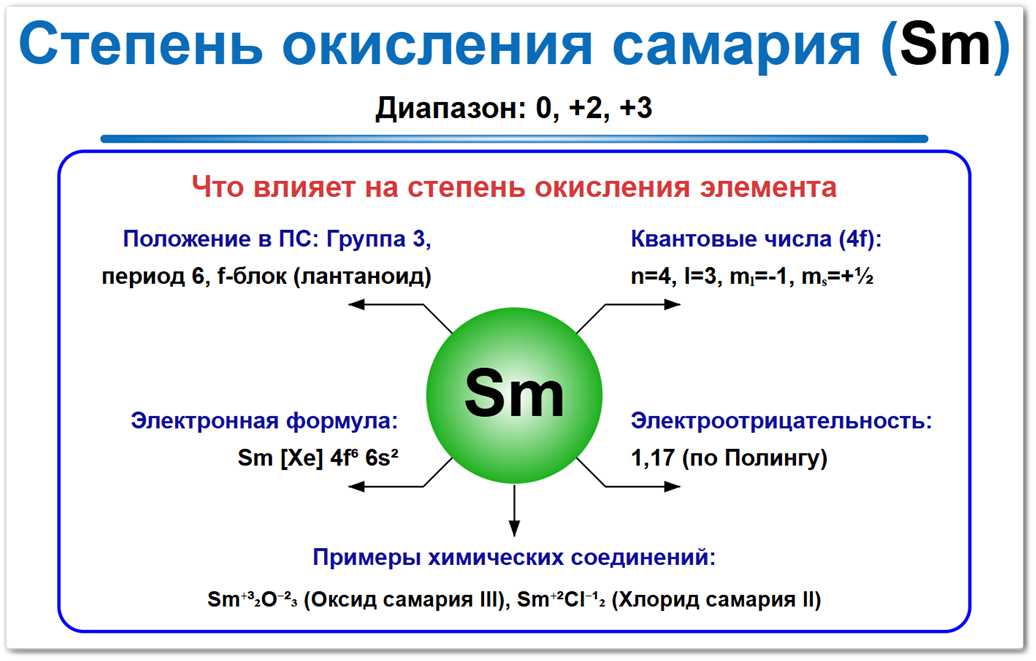
Рис. 1. Возможные степени окисления самария: наиболее типичная — +3, и важная восстановительная — +2. Состояние 0 характерно для металлического самария.
Обратите внимание, что химия самария в состоянии +2 во многом перекликается с химией европия (Eu).
Который является его соседом по группе лантаноидов и также склонен к образованию стабильных двухвалентных соединений.
На их формирование влияют электронное строение (4f6 6s2), положение в ряду лантаноидов и значение электроотрицательности 1,17 по шкале Полинга.
Содержание страницы
- 1. Почему у самария стабильная степень окисления?
- 2. Степень окисления самария в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления самария
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления самария
- 6. Шпаргалка для самария
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у самария стабильная степень окисления?
Причина преобладания состояния +3 заключается в стандартном для лантаноидов балансе энергий ионизации.
В то время как доступность состояния +2 объясняется близостью конфигурации f6 к наполовину заполненному f-слою.
- В простом веществе (Sm⁰): Заряд равен 0. Конфигурация:
[Xe] 4f6 6s2. - В ионе (Sm+3): Самарий отдает 3 валентных электрона. Конфигурация:
[Xe] 4f5.
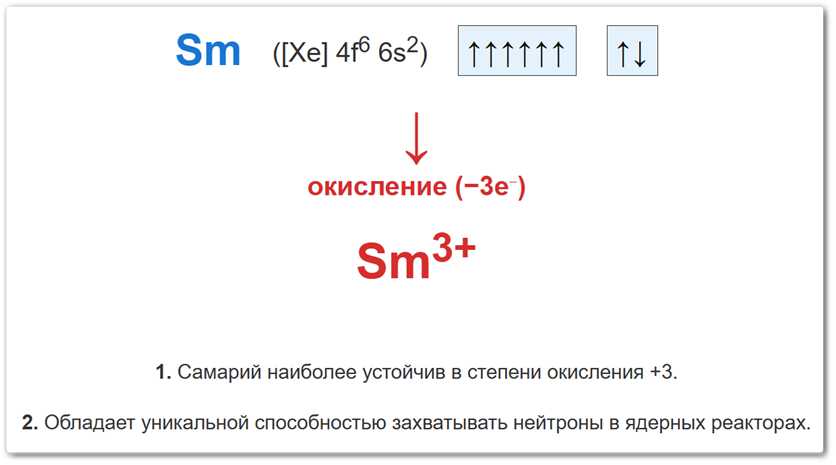
Рис. 2. Процесс окисления самария: переход от металлического состояния к катиону Sm3+, сопровождающийся потерей внешних электронов.
Степень окисления самария в соединениях
В зависимости от условий синтеза, самарий в соединениях проявляет степень окисления, которая определяет его химическую мощь:
- Оксид самария(III) (Sm2O3): Sm +3, O -2.
- Иодид самария(II) (SmI2): Sm +2, I -1.
- Хлорид самария(III) (SmCl3): Sm +3.
- Кобальтит самария (SmCo5): Sm +3 (в составе мощных магнитов).
Высшая степень окисления
Высшая степень окисления самария в обычных химических условиях равна +3.
Хотя в экстремальных условиях теоретически упоминаются следы +4, в стабильном виде такие соединения не существуют.
Низшая степень окисления
Для самария в растворах и твердых телах хорошо известна степень окисления +2, однако степень окисления самария равна 0 в чистом металлическом виде — это базовая форма элемента.
Промежуточные степени окисления
Степень окисления самария в веществах редко отклоняется от +3. Состояние +2, хоть и является промежуточным в процессе полного окисления, может сохраняться долгое время в безводных средах.
Важно: Соединение SmI2 является одним из самых популярных «одноэлектронных» восстановителей в современной органической химии, где степень окисления самария формула соединения всегда фиксируется как +2 перед началом реакции.
Почему степень окисления чаще положительная?
Знак заряда продиктован низкой электроотрицательностью и принадлежностью к металлам:
- Положительная СО (+): Самарий охотно отдает электроны более электроотрицательным элементам (галлогенам, кислороду).
- Нулевая СО (0): Характерна для простого вещества — светло-серого металла.
- Отрицательная СО (-): Для лантаноидов, включая самарий, такие состояния нехарактерны и в обычных условиях не встречаются.
Как определить степень окисления самария
По таблице Менделеева
- Семейство: f-элемент (редкоземельный металл).
- Валентные электроны: теоретически до 8 (6 на f-подуровне и 2 на s-подуровне), но реально участвуют 2 или 3.
- Атомная масса самария: 150,36 а.е.м.
По валентности (Число связей)
В отличие от d-металлов, валентность самария обычно ограничена значениями II или III.
- В оксиде (Sm2O3): Самарий образует три связи. Его валентность — III, СО — +3.
- В дииодиде (SmI2): Самарий связан с двумя атомами иода. Валентность — II, СО — +2.
По электронной конфигурации
- Электронная формула самария: [Xe] 4f6 6s2.
- Атому самария степени окисления +3 достичь выгодно, так как это типичный ионизационный предел для лантаноидов, обеспечивающий стабильность солей.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для SmCl3 (хлорид самария III):
Сумма СО равна 0. Хлор всегда -1. Обозначим Sm как x.
x + 3 · (-1) = 0 ⇒ x = +3
Примеры степеней окисления самария
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +3 | Наиболее стабильная. Характерна для большинства минералов и магнитов. | Sm2O3, SmCl3, SmCo5 |
| +2 | Восстановительная. Важна в органических реакциях. | SmI2, SmO, SmS |
| 0 | Металл. Состояние чистого элемента. | Sm (металлический) |
Шпаргалка для самария
- Магниты — сплав SmCo5 позволяет создавать мощнейшие постоянные магниты, устойчивые к высоким температурам.
- Реагент Кагана — SmI2 в степени окисления +2 является «золотым стандартом» для химиков-синтетиков.
- Цвет — ионы Sm3+ дают растворам бледно-желтую окраску, а Sm2+ — интенсивную красную или темно-синюю.
Пример решения задачи:
▶️ Дано:
Соединение: SmI2 (иодид самария II).
⌕ Найти:
Определите СО самария.
✨ Решение:
Иод (I) в солях лантаноидов равен -1. Уравнение: x + 2 · (-1) = 0 → x — 2 = 0 → x = +2.
✅ Ответ:
Sm(+2).
Проверка знаний
Показать ответы
Правильные ответы: 3, 4, 5.
Разбор ошибок:
1 — неверно: самарий — это f-элемент, относящийся к лантаноидам.
2 — неверно: ионы Sm2+ быстро окисляются водой, поэтому их используют в органических растворителях (ТГФ).
Часто задаваемые вопросы
Наиболее стабильной формой в природе и технике является степень окисления +3.
Она критически важна для специфических химических превращений в лабораториях, где требуется мягкий и селективный перенос электронов.
Все металлы, включая самарий (Sm), имеют низкую электроотрицательность и легко отдают свои внешние электроны.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.