Теория:
Степень окисления урана (U) в различных соединениях может принимать широкий диапазон значений: +3, +4, +5 и +6.
Такое разнообразие валентных состояний обусловлено тем, что электроны на 5f, 6d и 7s орбиталях имеют близкие энергетические уровни и могут поочередно участвовать в химических взаимодействиях.
Кроме того, выделяют показатель 0, характерный для урана в виде простого вещества (тяжелый, плотный серебристо-белый металл).
Например для наиболее стабильной СО +6: в соединении UO2Cl2 (дихлорид диоксоурана VI) или в ионе уранила UO22+ заряд металла равен +6.
Это самая устойчивая форма урана в аэробных условиях.
Для сравнения, СО +4: встречается в таких веществах, как UO2 (диоксид урана) или UF4 (тетрафторид урана).
Данное состояние преобладает в восстановительных средах и является основным для многих минералов.
- Почему +6? Это высшее состояние, при котором атом отдает все 6 валентных электронов. Образующийся при этом ион уранила (UO22+) обладает исключительной прочностью и стабильностью в растворах.
- Почему +3 и +5 менее распространены? Соединения урана(III) — мощные восстановители, легко окисляющиеся даже водой. Состояние +5 (например, в UF5) склонно к диспропорционированию, то есть распаду на +4 и +6.
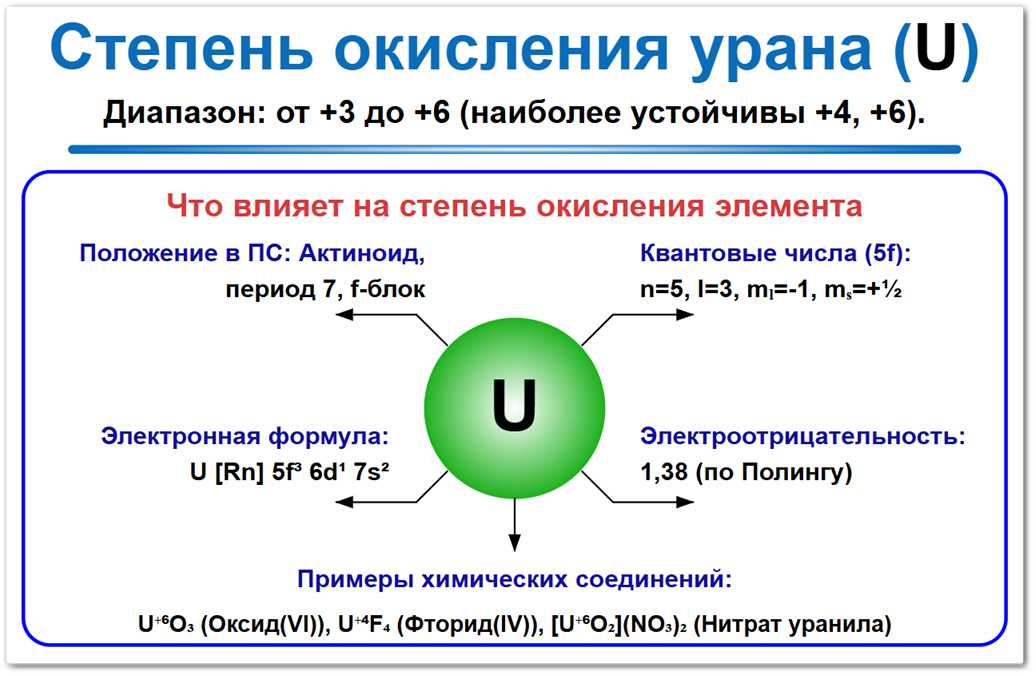
Рис. 1. Основные степени окисления урана: от 0 до +6.
Форма +6 является наиболее устойчивой в присутствии кислорода, в то время как форма +4 характерна для твердых оксидов и топливных элементов ядерных реакторов.
Необходимо учитывать, что уран не только химически токсичен, но и радиоактивен.
Его химия неразрывно связана с вопросами ядерной энергетики и экологии.
На свойства этого актиноида влияют его электронная формула (5f3 6d1 7s2), эффекты релятивистского сжатия и значение электроотрицательности 1,38 по шкале Полинга.
Содержание страницы
- 1. Почему +6 и +4 — самые важные степени окисления у урана
- 2. Степень окисления урана в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему уран имеет так много положительных зарядов?
- 4. 4 способа определить степень окисления урана
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления урана
- 6. Шпаргалка для урана
- 7. Уран вне учебника: какие степени окисления существуют только в теории?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +6 и +4 — самые важные степени окисления у урана
Причина превалирования этих состояний заключается в достижении наиболее энергетически выгодных конфигураций или формировании сверхстабильных молекулярных ионов.
- В простом веществе (U0): Заряд равен 0. Конфигурация:
[Rn] 5f3 6d1 7s2. - В высшем ионе (U+6): Уран формально лишается всех 6 внешних электронов. Конфигурация:
[Rn](электронный остов радона).

Рис. 2. Схема окисления урана: удаление валентных электронов с превращением атома в ионы с зарядами до +6.
Степень окисления урана в соединениях
В зависимости от типа лиганда и условий среды, уран в соединениях проявляет степень окисления, которая определяет цвет и растворимость вещества:
- Гексафторид урана (UF6): U +6.
- Тетрафторид урана (UF4): U +4 (зеленая соль).
- Диоксид урана (UO2): U +4.
- Триоксид урана (UO3): U +6.
- Трихлорид урана (UCl3): U +3.
Высшая степень окисления
Высшая степень окисления урана равна +6. В этом состоянии он образует летучий гексафторид, используемый для разделения изотопов, и соли уранила.
Низшая степень окисления
Для урана характерна степень окисления 0 в металлическом виде. В химических соединениях низшим стабильным значением считается +3.
Промежуточные степени окисления
Степень окисления урана в веществах часто встречается в виде смешанных оксидов.
Например, в закиси-окиси урана (U3O8) атомы металла находятся одновременно в состояниях +5 и +6.
Важно: Ион уранила (UO22+) — это уникальная «визитная карточка» химии урана. Благодаря своей структуре, уран в степени +6 остается растворимым в воде, что критически важно для геохимии и добычи металла.
Почему уран имеет так много положительных зарядов?
Многообразие степеней окисления обусловлено «пластичностью» его электронной оболочки:
- Положительная СО (+): Металлическая природа и большой радиус позволяют легко отрывать до 6 электронов.
- Отсутствие отрицательных СО (-): Из-за низкой электроотрицательности уран никогда не принимает электроны, выступая исключительно в роли донора.
4 способа определить степень окисления урана
По таблице Менделеева
- Семейство: f-элемент.
- Валентные электроны: 6 электронов (5f3 6d1 7s2).
- Атомная масса урана: 238,03 а.е.м.
По валентности (Число связей)
В химии чаще всего фигурирует валентность урана IV или VI.
- В UF6: Уран связан с шестью атомами фтора, что соответствует СО +6.
- В UO2: Атом образует связи, эквивалентные валентности IV, СО — +4.
По электронной конфигурации
- Электронная формула урана: [Rn] 5f3 6d1 7s2.
- Атому урана степени окисления +6 достичь проще всего в химически активных средах, так как это освобождает все уровни за пределами инертного ядра радона.
Для детального разбора распределения электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для UO2SO4 (сульфат уранила):
Сумма СО равна 0. Кислород -2, группа SO4 имеет заряд -2. Обозначим уран как x.
x + 2 · (-2) + (-2) = 0 ⇒ x — 4 — 2 = 0 ⇒ x = +6
Примеры степеней окисления урана
| СО | Краткое описание | Примеры соединений |
|---|---|---|
| +6 | Максимально стабильная. Форма существования в растворах и летучих фторидах. | UO3, UF6, UO22+ |
| +4 | Устойчивая в кристаллах. Основная форма в ядерном топливе. | UO2, UF4, UCl4 |
| +3 | Восстановительная. Легко переходит в +4, крайне нестабильна в воде. | UH3, UCl3 |
Шпаргалка для урана
- +6 — доминирующее состояние, образует характерный желтый цвет солей уранила.
- +4 — типично для диоксида урана, имеет зеленый или черный цвет.
- Окислительно-восстановительные переходы — уран легко меняет СО, что используется в радиохимических технологиях.
Уран вне учебника: какие степени окисления существуют только в теории?
+1 и +2: В классической химии эти состояния считаются несуществующими для урана.
Однако ученым удалось стабилизировать ионы урана (II) в составе специфических органических комплексов при сверхнизких температурах.
В свободном виде такие формы мгновенно распадаются.
+5: Хотя это состояние реально существует (например, в PaCl5-подобном UF5), оно крайне неустойчиво в растворах.
Уран(V) обычно существует лишь доли секунды, прежде чем превратиться в смесь +4 и +6.
Отрицательные степени: Для урана они не зафиксированы даже в экстремальных условиях.
Высокий положительный заряд ядра и специфика f-орбиталей делают прием электронов сверх необходимого набора невозможным.
Интересный факт: Цвет соединений урана напрямую зависит от его степени окисления. СО +3 дает пурпурный цвет, СО +4 — глубокий зеленый, а СО +6 — ярко-желтый. Именно благодаря СО +6 старинное «урановое стекло» так красиво светится в ультрафиолете.
Пример решения задачи:
▶️ Дано:
Соединение: UO2 (диоксид урана).
⌕ Найти:
Вычислите СО урана.
✨ Решение:
Кислород (O) имеет постоянную СО -2. Уравнение: x + 2 · (-2) = 0 → x — 4 = 0 → x = +4.
✅ Ответ:
U(+4).
Проверка знаний
Показать ответы
Правильные ответы: 2, 3.
Разбор ошибок:
1 — неверно: уран является актиноидом.
4 — неверно: уран — металл, он проявляет только положительные СО или 0.
Часто задаваемые вопросы
Главная причина кроется в электронном строении его атома. Уран — тяжелый элемент (№92), и его электроны распределены по очень сложной схеме.
1. Близость энергетических уровней.
2. Огромное расстояние от ядра.
3. Релятивистские эффекты.
Наиболее стабильной в обычных условиях является СО +6.
Это состояние энергетически выгодно при образовании прочных кристаллических решеток оксидов и фторидов, используемых в ядерных реакторах.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.