Теория:
Степень окисления хассия (Hs) в химических соединениях проявляет высшую и наиболее характерную степень окисления +8.
Это обусловлено положением элемента в 8-й группе Периодической системы, где он является тяжелым аналогом осмия (Os) и рутения (Ru).
Хассий — один из немногих элементов, способных достигать такой высокой степени окисления.
Кроме того, выделяют показатель 0, который относится к хассию в виде простого вещества (сверхтяжелый радиоактивный металл).
Например для наиболее стабильной СО +8: в соединении HsO4 (тетраоксид хассия) заряд иона равен +8.
В этом состоянии хассий проявляет поразительное химическое сходство с тетраоксидом осмия, будучи весьма летучим соединением.
Для сравнения, другие СО: теоретически возможны состояния +6, +4, +3 и +2, однако экспериментально наиболее надежно зафиксировано именно восьмивалентное состояние в газовой фазе.
- Почему +8? Электронная формула хассия [Rn] 5f14 6d6 7s2 позволяет атому задействовать все восемь электронов внешних оболочек для образования прочных ковалентных связей с кислородом.
- Почему другие СО менее вероятны? Для элементов 8-й группы (особенно для осмия и хассия) достижение максимальной степени окисления с кислородом является энергетически выгодным, что приводит к формированию устойчивых тетраоксидов.
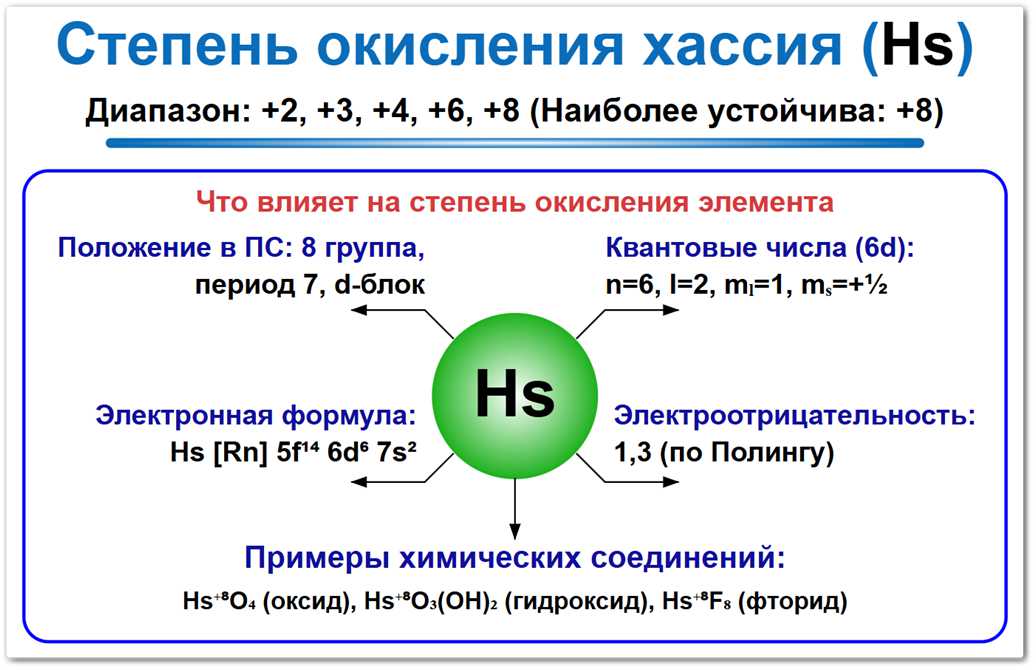
Рис. 1. Основная степень окисления хассия: 0 и +8.
Состояние +8 является «визитной карточкой» химии хассия, подтвержденной в уникальных экспериментах по термохроматографии.
Важно заметить, что хассий — крайне радиоактивный элемент, время жизни изотопов которого составляет доли секунды или минуты.
Его нельзя накопить в макроскопических количествах.
Эксперименты проводятся с единичными атомами. Релятивистские эффекты в хассии настолько сильны, что они напрямую влияют на стабильность орбиталей, однако групповое сходство с осмием все равно остается доминирующим.
Содержание страницы
- 1. Почему +8 — самая устойчивая степень окисления у хассия
- 2. Степень окисления хассия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему хассий предпочитает заряд +8?
- 4. 4 способа определить степень окисления хассия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления хассия
- 6. Шпаргалка
- 7. Хассий вне учебника: что скрывает наука?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +8 — самая устойчивая степень окисления у хассия
Стабильность обусловлена симметрией и прочностью связей в молекуле тетраоксида.
- В простом веществе (Hs0): Заряд равен 0. Конфигурация:
[Rn] 5f14 6d6 7s2. - В восьмивалентном состоянии (Hs+8): Хассий задействует все 8 валентных электронов. Конфигурация иона:
[Rn] 5f14.

Рис. 2. Схема образования степени окисления +8: участие 6d и 7s электронов в связях.
Степень окисления хассия в соединениях
- Тетраоксид хассия (HsO4): Hs +8.
- Хассат-ион (в растворах) ([HsO4(OH)2]2-): Hs +8.
- Металлоорганический карбонил (Hs(CO)5): Hs 0.
Высшая степень окисления
Высшая степень окисления Hs равна +8.
Низшая степень окисления
Характерна степень окисления 0 в металлическом состоянии или сложных комплексах с CO.
Промежуточные степени окисления
В отличие от железа (+2, +3), у хассия промежуточные состояния (+4, +6) изучены крайне слабо из-за высокой нестабильности атомов.
Важно: Хассий назван в честь немецкой земли Гессен (Hassia), где в Дармштадте он был впервые синтезирован.
Почему хассий предпочитает заряд +8?
- Групповой аналог осмия: В 8-й группе ПСХЭ способность проявлять высокую валентность растет сверху вниз.
- Летучесть оксидов: Образование HsO4 позволяет элементу существовать в газовой фазе, что энергетически подтверждает его состояние +8.
4 способа определить степень окисления хассия
По таблице Менделеева
- Семейство: Трансактиноиды (d-элементы).
- Валентные электроны: 8.
- Атомная масса: ~270 а.е.м.
По валентности (Число связей)
Валентность хассия (Hs) в его самом известном соединении равна VIII.
Атом хассия образует четыре двойные ковалентные связи с атомами кислорода в молекуле тетраоксида.
Детальные примеры:
- В HsO4: Тетраэдрическая молекула, где хассий находится в центре, проявляя высшую валентность группы.
- В комплексных солях: Хассий может координировать дополнительные гидроксид-ионы, сохраняя при этом состояние +8.
По электронной конфигурации
Электронная формула хассия: [Rn] 5f14 6d6 7s2.
Как происходит ионизация:
- Валентные электроны: У хассия 8 электронов на уровнях 6d и 7s.
- Механизм: При образовании оксида электроны переходят в общее пользование с кислородом, формально определяя заряд +8.
- Результат: Достижение устойчивой конфигурации за счет полного использования валентной зоны.
По химическому соединению (Алгебраический расчет)
Пример для HsO4:
- 1. Степень окисления кислорода (O) равна -2.
- 2. В соединении 4 атома кислорода: 4 · (-2) = -8.
- 3. Сумма всех СО должна быть 0: x + (-8) = 0.
- 4. Отсюда x = +8.
✅ Вывод: Степень окисления хассия в тетраоксиде равна +8.
Примеры степеней окисления хассия
| СО | Характеристика | Примеры |
|---|---|---|
| +8 | Высшая и наиболее изученная. | HsO4 |
| 0 | Металлическое состояние. | Hs |
Шпаргалка
- +8 — главная СО хассия.
- Аналог осмия — ищи сходство в летучести и форме оксидов.
Хассий вне учебника: что скрывает наука?
Газовая химия:
Химия хассия уникальна тем, что ученые смогли «прогнать» отдельные атомы через термохроматографическую колонку и увидеть, при какой температуре они оседают.
Это доказало, что HsO4 химически почти идентичен OsO4.
Релятивистские эффекты:
Хотя хассий ведет себя как аналог осмия, расчеты показывают, что его d-орбитали расширяются, а s-орбитали сжимаются из-за скорости электронов.
Это делает хассий даже более склонным к высшей степени окисления, чем можно было бы ожидать.
Химия в растворах:
В начале 2000-х были проведены опыты по растворению хассия в щелочах, где он образовал хассат-ионы.
Это подтвердило, что хассий может существовать не только как летучий газ, но и проявлять свойства активного центра в сложных ионах.
Пример решения задачи:
▶️ Дано:
Соединение: Na2[HsO4(OH)2] (хассат(VIII) натрия).
⌕ Найти:
Определите степень окисления хассия.
✨ Решение:
1. Натрий (Na) всегда +1. Для двух атомов: 2 · (+1) = +2.
2. Кислород (O) -2. Для четырех атомов: 4 · (-2) = -8.
3. Группа (OH) имеет заряд -1. Для двух групп: 2 · (-1) = -2.
4. Уравнение электронейтральности: (+2) + x + (-8) + (-2) = 0.
5. x — 8 = 0 ⇒ x = +8.
✅ Ответ:
СО хассия (Hs) в этом комплексном соединении равна +8.
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 3, 5.
Разбор ошибок:
4 — неверно: хассий — крайне радиоактивный трансактиноид.
Часто задаваемые вопросы
Это связано с тем, что в 8-й группе валентные электроны d- и s-подуровней имеют схожую энергию и могут все вместе участвовать в образовании связей, особенно с сильными окислителями типа кислорода.
Теоретически да, но такие соединения будут мгновенно окисляться или распадаться. В условиях современного эксперимента фиксируется только максимально стабильное состояние +8.
Хассий — это тяжелый радиоактивный металл, который стремится только к потере электронов (положительные СО), а не к их приобретению.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.