Теория:
Степень окисления серебра в большинстве соединений принимает значение +1, значительно реже встречаются состояния +2, +3 и крайне редкое +4.
Также существуют состояния с СО 0 (металл) и крайне нестабильная отрицательная СО -1, которая проявляется только в специфических условиях (например, в ауридах-аргентидах щелочных металлов).
Например для высшей СО +3: в соединении KAgF4 (тетрафтороаргентат калия) степень окисления металла равна +3.
Это происходит потому, что серебро находится в 11-й группе и при воздействии сильнейших окислителей (фтор) оно способно отдавать электроны не только с внешнего 5s-слоя, но и с предвнешнего d-подуровня (4d10 5s1), достигая высокого заряда.
Для сравнения, отрицательная СО -1: встречается в таких экзотических соединениях, как CsAg.
Здесь ситуация обратная: серебро проявляет неметаллические свойства и «принимает» электрон от менее электроотрицательного цезия на свою 5s-орбиталь, стремясь завершить её до конфигурации 5s2.
Такие состояния крайне нестабильны, так как серебро — типичный благородный металл, и оно стремится вернуться к положительному или нулевому заряду.
Промежуточные же степени окисления, такие как +2, являются «неудобными» для атома в обычных растворах.
Обладая конфигурацией [Kr] 4d10 5s1, серебру проще всего отдать один электрон, получив полностью заполненный и стабильный 4d10 слой.
Именно поэтому соединения серебра(II) являются мощнейшими окислителями и часто склонны к превращению в более устойчивую форму +1.
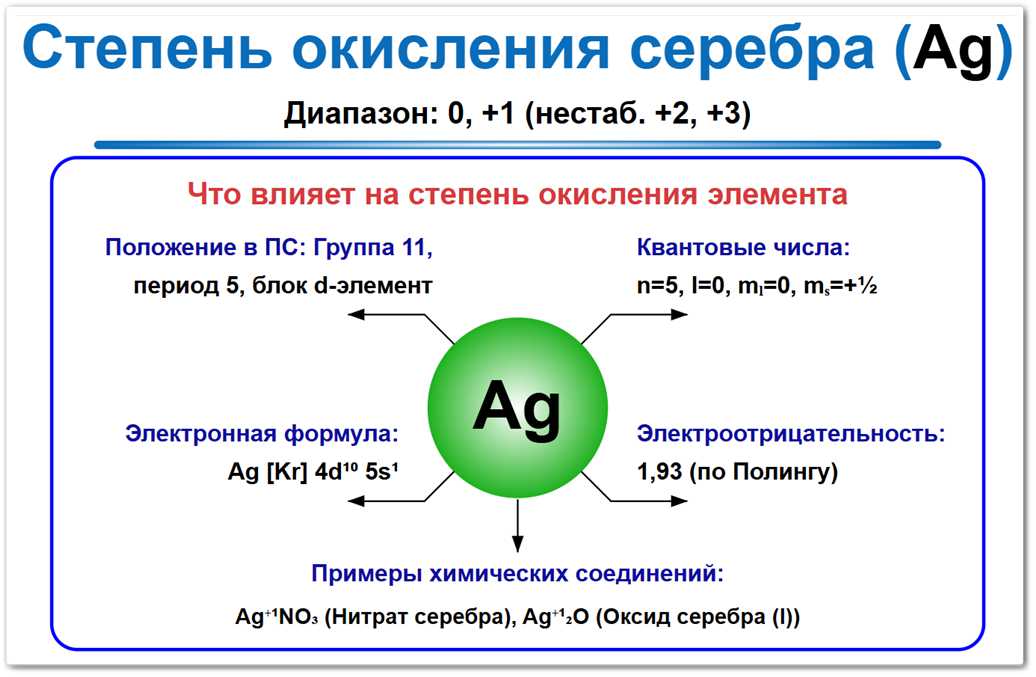
Рис. 1. Возможные степени окисления серебра: от -1 до +4. Наиболее устойчивая форма — +1 (нитраты, хлориды), значительно реже +2 и +3.
Обратите внимание, что химия серебра во многом отличается от химии меди (Cu), своего соседа сверху по группе, для которой состояние +2 является основным, в то время как для серебра оно вторично.
На их формирование влияют электронное строение (4d10 5s1), положение в 11-й группе и значение электроотрицательности 1,93 по шкале Полинга.
Содержание страницы
- 1. Почему у серебра стабильная степень окисления?
- 2. Степень окисления серебра в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления серебра
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления серебра
- 6. Шпаргалка для серебра
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у серебра стабильная степень окисления?
Причина стабильности основного состояния серебра (+1) заключается в том, что при потере единственного 5s-электрона атом приобретает полностью заполненный 4d-подуровень, который обладает высокой симметрией и низкой энергией.
- В простом веществе (Ag⁰): Заряд равен 0. Конфигурация:
5s [↑] 4d [↑↓][↑↓][↑↓][↑↓][↑↓]. - В ионе (Ag+1): Серебро отдает 1 валентный электрон. Конфигурация:
[Kr] 4d10.

Рис. 2. Процесс окисления серебра: от металлического состояния до самого стабильного катиона +1.
Степень окисления серебра в соединениях
В зависимости от условий реакции, серебро в соединениях проявляет степень окисления, которая определяет растворимость и светочувствительность соли:
- Нитрат серебра (AgNO3): Ag +1, N +5, O -2.
- Оксид серебра (I) (Ag2O): Ag +1, O -2.
- Фторид серебра (II) (AgF2): Ag +2, F -1.
- Оксид серебра (I, III) (AgO): Ag +1 и +3 (смешанный оксид).
- Тетрафтороаргентат (III) цезия (CsAgF4): Ag +3.
Высшая степень окисления
Высшая степень окисления серебра в химически стабильных (в особых условиях) формах равна +3. В крайне редких случаях в составе специфических фтористых комплексов зафиксирована СО +4.
Низшая степень окисления
Для серебра возможна степень окисления -1 в сплавах с активными металлами, однако степень окисления серебра равна 0 в свободном металлическом виде — это наиболее естественное состояние для самородного серебра.
Промежуточные степени окисления
Степень окисления серебра в веществах может принимать значение +2 (например, в черном осадке AgF2), но такие соединения являются мощными окислителями и легко восстанавливаются до +1.
Важно: Почти вся аналитическая химия и фотографические процессы строятся на степени окисления серебра +1, где степень окисления серебра формула соединения чаще всего включает один атом металла на один однозарядный анион (AgCl, AgBr).
Почему степень окисления чаще положительная?
Знак заряда определяется типично металлическим характером элемента:
- Положительная СО (+): Серебро легко отдает внешний электрон более электроотрицательным элементам.
- Нулевая СО (0): Характерна для ювелирного серебра и зеркальных покрытий.
- Отрицательная СО (-): Проявляется только в присутствии сверхсильных восстановителей (щелочных металлов).
Как определить степень окисления серебра
По таблице Менделеева
- Семейство: d-элемент.
- Валентные электроны: 11 (10 на d-подуровне и 1 на s-подуровне).
- Атомная масса серебра: 107,8 а.е.м.
По валентности (Число связей)
В отличие от более сложных соседей, валентность серебра обычно постоянна и равна I.
- В хлориде серебра (AgCl): Атом серебра образует одну связь с хлором. Его валентность — I, а степень окисления равна +1.
- В оксиде (Ag2O): Два атома серебра связаны с одним атомом кислорода. Валентность каждого — I, СО — +1.
По электронной конфигурации
- Электронная формула серебра: [Kr] 4d10 5s1. Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
- Атому серебра степени окисления +1 достичь выгодно, так как это оставляет заполненную 4d-оболочку.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для Ag2SO4 (сульфат серебра):
Сумма СО равна 0. Кислород -2, Сера +6. Обозначим Ag как x.
2x + 6 + 4 · (-2) = 0
2x + 6 — 8 = 0 ⇒ 2x = 2 ⇒ x = +1
Примеры степеней окисления серебра
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +3 | Высшая (типичная). Проявляется в сильных окислителях. | KAgF4, Ag2O3 (нестабилен) |
| +1 | Основная / Самая стабильная. Форма большинства солей. | AgNO3, AgCl, Ag2S |
| +2 | Редкая. Существует в виде фторидов и оксидов. | AgF2, [Ag(Py)4]S2O8 |
| 0 | Металл. Состояние свободного элемента. | Ag (банковское серебро) |
| -1 | Отрицательная. Крайне редкая (аргентиды). | CsAg, RbAg |
Шпаргалка для серебра
- +1 — главная СО, образует растворимый нитрат серебра (ляпис).
- Бактерицидность — ионы серебра Ag+ обладают мощным дезинфицирующим свойством.
- Свет — соли серебра +1 разлагаются на свету до металлического серебра (0).
Пример решения задачи:
▶️ Дано:
Соединение: Ag2O.
⌕ Найти:
Определите СО серебра.
✨ Решение:
Кислород (O) равен -2. Уравнение для двух атомов серебра: 2x + (-2) = 0 → 2x = 2 → x = +1.
✅ Ответ:
Ag(+1).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 3, 5.
Разбор ошибок:
4 — неверно: высшая СО серебра достигает +3 (редко +4), но никогда не равна номеру группы 11.
Часто задаваемые вопросы
Наиболее стабильной и распространенной является степень окисления +1.
Да, это возможно в некоторых соединениях (например, фторид AgF2), но они являются очень сильными окислителями.
Это связано с его низкой химической активностью и устойчивостью степени окисления 0.
