Теория:
Степень окисления селена (Se) в наиболее устойчивых соединениях принимает значения -2, +4 и +6.
Будучи типичным неметаллом, селен проявляет окислительные свойства, особенно в высших состояниях.
Значения 0, +2 встречаются реже. Состояние +2 характерно для некоторых нестабильных соединений, таких как дихлорид селена (SeCl2), однако они стремятся перейти в более устойчивые формы +4 или +6.
Селен находится в 16-й группе (главная подгруппа VI группы) и является p-элементом 4-го периода.
Как p-элемент, он обладает электронной конфигурацией [Ar] 3d104s24p4. В отличие от германия, у селена на внешнем p-слое находится уже четыре электрона.
Селен проявляет преимущественные степени окисления -2, +4 и +6.
Это связано с тем, что атом может либо принять два электрона до завершения октета (СО -2), либо задействовать в образовании связей свои внешние электроны (четыре 4p для СО +4 или все шесть электронов 4s и 4p для СО +6).
В отличие от серы, селен обладает чуть более выраженными металлическими признаками (полупроводниковые свойства), но его химия прочно связана с неметаллами.
Чтобы определить возможные значения, используют электронную формулу.
Например:
- Для селена (1s22s22p63s23p63d104s24p4) — принятие двух электронов достраивает слой до устойчивого состояния (СО -2).
- Для германия (1s22s22p63s23p63d104s24p2) — наличие лишь двух p-электронов определяет его склонность к отдаче электронов (СО +4).
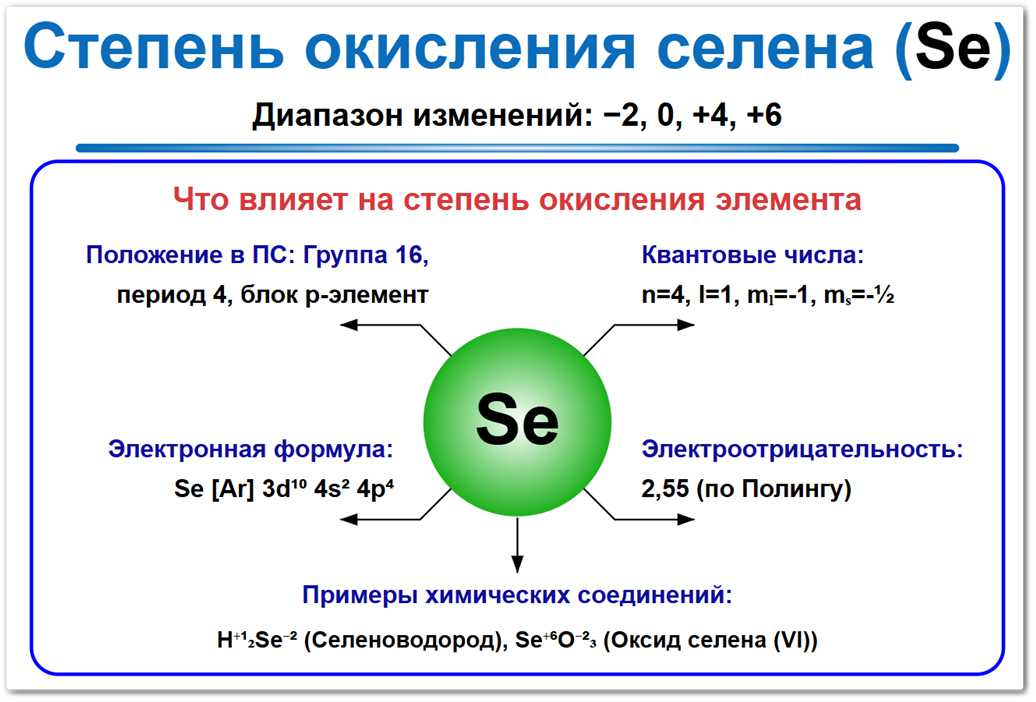
Рис. 1. Возможные степени окисления селена: -2, 0, +2, +4, +6. Обратите внимание, что высшая степень окисления всегда положительная.
На их формирование влияют электронное строение (наличие четырех p-электронов на внешнем слое), положение в 16-й группе и значение электроотрицательности 2,55 по шкале Полинга.
Содержание страницы
- 1. Почему у селена переменные степени окисления?
- 2. Степень окисления селена в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 3. Почему степень окисления может быть положительной или отрицательной?
- 4. Как определить степень окисления селена
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления селена
- 6. Шпаргалка для селена
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у селена переменные степени окисления?
Причина гибкости селена — наличие 6 валентных электронов и возможность как достраивать оболочку до октета (СО -2), так и поэтапно отдавать электроны (СО +4, +6).
- В простом веществе (Se⁰): Заряд равен 0. Конфигурация:
4s [↑↓] 4p [↑↓][↑][↑]. - В ионе (Se-2): Селен принимает 2 электрона на 4p-уровень. Конфигурация
4s [↑↓] 4p [↑↓][↑↓][↑↓]. - В ионе (Se+4): Селен отдает 4 электрона с 4p-уровня. Конфигурация
4s [↑↓] 4p [ ][ ][ ]. - В ионе (Se+6): Селен отдает 4 электрона с 4p и 2 электрона с 4s. Конфигурация
4s [ ] 4p [ ][ ][ ].

Рис. 2. Процесс изменения степени окисления селена: атом Se ([Ar] 3d10 4s2 4p4) может превращаться как в анион, так и в катион в зависимости от химической реакции.
Степень окисления селена в соединениях
Соединения селена демонстрируют его способность выступать в роли окислителя или восстановителя:
- Селеновая кислота (H2SeO4): Se +6, O -2.
- Диоксид селена (SeO2): Se +4, O -2 (белые кристаллы).
- Селенистая кислота (H2SeO3): Se +4.
- Селеноводород (H2Se): Se -2, H +1 (ядовитый газ).
- Селенид натрия (Na2Se): Se -2.
Высшая степень окисления
Высшая степень окисления селена равна +6. Она соответствует номеру его группы (VIА) в таблице Менделеева.
Низшая степень окисления
Низшая равна -2. Она проявляется в соединениях с водородом (селеноводороде) и активными металлами (селенидах).
Важно: В отличие от кислорода, селен охотнее переходит в положительные степени окисления (+4, +6) из-за большего радиуса атома и меньшей электроотрицательности.
Почему степень окисления может быть положительной или отрицательной?
Знак заряда зависит от разности электроотрицательности (ЭО).
- Положительная СО (+): Селен отдает электронную плотность более сильным неметаллам (F, O, Cl).
- Отрицательная СО (-): Проявляется в соединениях с металлами или водородом, где селен притягивает электроны к себе.
- Нулевая СО (0): Характерна для простых веществ (серый, красный или черный селен).
Как определить степень окисления селена
По таблице Менделеева
- Семейство: p-элемент (группа халькогенов).
- Валентные электроны: 6 (2 на s-уровне и 4 на p-уровне).
- Атомная масса селена: 78,96 а.е.м. Для сравнения масс других элементов используй таблицу атомных масс.
- Типичные СО: -2, +4, +6.
По валентности (Число связей)
Валентность селена чаще всего равна II, IV или VI.
- Валентность VI: Соответствует высшей СО +6.
- Пример: H2SeO4. Здесь селен шестивалентен.
«А вы знали?» Селен в своей высшей степени окисления +6 превращается в «пожирателя золота». Селеновая кислота — единственная индивидуальная кислота, способная растворить золото без посторонней помощи.
По электронной конфигурации
- Электронная формула селена: [Ar] 3d10 4s2 4p4. Для просмотра значений квантовых чисел используй таблицу квантовых чисел.
- Наличие двух неспаренных p-электронов объясняет СО -2, а возможность распаривания электронов приводит к состояниям +4 и +6.
По химическому соединению (Алгебраический расчет)
Так как Селен — неметалл 16-й группы, его степень окисления в высших оксидах рассчитывается через ЭО кислорода.
Это правило помогает находить степени окисления элементов в молекуле через простое уравнение.
Пример для SeO2 (диоксид селена):
Сумма всех степеней окисления в молекуле равна 0.
Обозначим СО селена за x, а у кислорода она всегда -2.
1 · x + 2 · (-2) = 0
x — 4 = 0 ⇒ x = +4
Примеры степеней окисления селена
| СО | Цвет соединений | Примеры соединений (с индексами) |
|---|---|---|
| +6 | Бесцветный (жидкость/кристаллы) | H2SeO4, SeF6, Na2SeO4 |
| +4 | Белый (кристаллы) | SeO2, H2SeO3, SeCl4 |
| 0 | Серый, красный, черный | Se (Селен) |
| -2 | Газообразное (H2Se) / Твердое | H2Se, Na2Se, Al2Se3 |
Шпаргалка для селена
- -2 — проявляется в ядовитом газе селеноводороде.
- +4 — типична для диоксида селена и селенистой кислоты.
- +6 — высшая степень, проявляет сильнейшие окислительные свойства.
- Полупроводник — в свободном состоянии (СО 0) широко применяется в фотоэлементах.
Пример решения задачи:
▶️ Дано:
Соединение: Na2SeO4.
⌕ Найти:
Определите СО селена.
✨ Решение:
Na имеет СО +1, O имеет СО −2. Следовательно: 2 · (+1) + x + 4 · (−2) = 0 → 2 + x − 8 = 0 → x = +6.
✅ Ответ:
Se(+6).
Проверка знаний
Отметьте правильные утверждения для Селена (Se):
Показать ответы
Правильные ответы: 1, 3, 4.
Разбор ошибок:
2 — неверно: селен — это неметалл.
5 — неверно: в SeO2 у селена степень окисления +4.
Часто задаваемые вопросы
Базовая степень окисления селена в его высшем оксиде (SeO3) — +6.
Это зависит от того, забирает селен электроны или отдает их, чтобы заполнить свой внешний слой:
Отрицательная (-2): Селен стоит в VI группе, ему не хватает 2 электронов до стабильного состояния (октава из 8 электронов). Он забирает их у менее электроотрицательных элементов (например, металлов или водорода).
Положительная (+4, +6): Селен отдает свои внешние электроны более сильным «охотникам» — кислороду или фтору. Если отдает 4 электрона (p-подуровень) +4. Если отдает все 6 электронов слоя +6 (высшая степень по номеру группы).
С точки зрения токсичности газов наиболее опасен селен в состоянии -2 (H2Se). С точки зрения химической активности — состояние +6 (сильный окислитель).

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.