Теория:
Степень окисления нобелия (No) в химических соединениях принимает значения +2 и +3, причем состояние +2 является для него необычайно устойчивым.
Это уникальная особенность нобелия, обусловленная завершением электронной оболочки 5f-подуровня.
Кроме того, выделяют показатель 0, который относится к нобелию в виде простого вещества (серебристый радиоактивный металл).
Например для наиболее стабильной СО +2: в соединении NoCl2 (хлорид нобелия II) заряд иона равен +2.
В этом состоянии нобелий по химическим свойствам напоминает щелочноземельные металлы, такие как барий или радий.
Для сравнения, СО +3: проявляется реже и требует очень сильных окислителей, так как переход от стабильного +2 к +3 энергетически невыгоден.
- Почему +2? Атом нобелия при потере двух электронов достигает конфигурации 5f14 — полностью заполненного f-подуровня, что является энергетически крайне выгодным (стабильным) состоянием.
- Почему другие СО менее стабильны? СО +3 требует нарушения целостности заполненного f-слоя, что требует затрат большой энергии, поэтому соединения нобелия (III) являются крайне сильными окислителями.
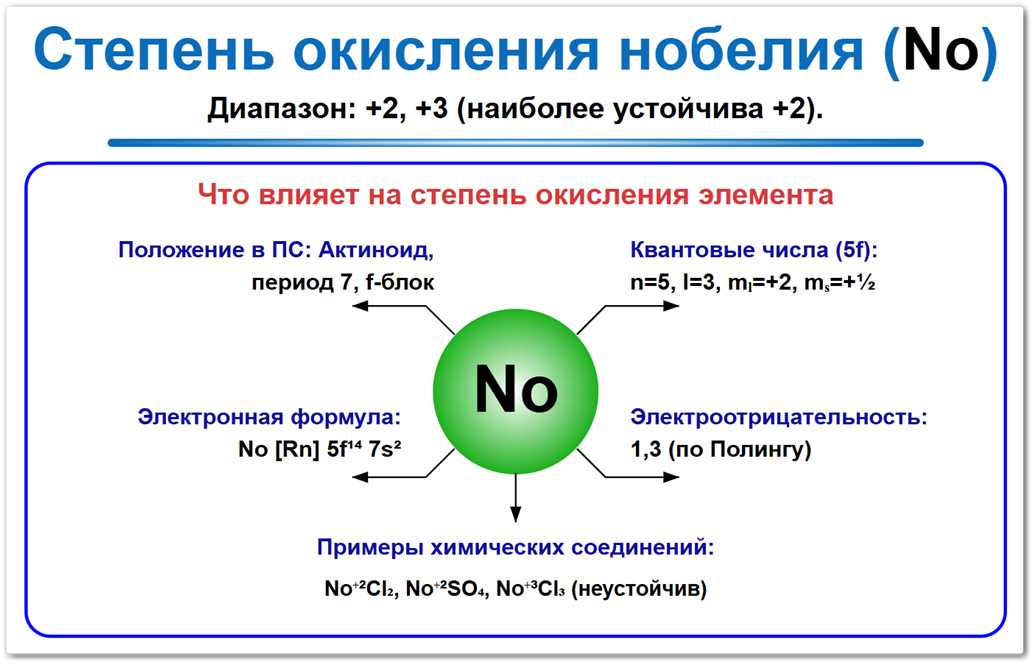
Рис. 1. Основные степени окисления нобелия: 0, +2 и +3.
Состояние +2 является наиболее устойчивым в водных растворах, что делает нобелий «аномальным» актиноидом, ведущим себя скорее как элемент второй группы.
Важно заметить, что нобелий крайне радиоактивен. Работы с ним ведутся исключительно в специализированных ядерных центрах, так как он синтезируется искусственно в ускорителях.
На свойства этого элемента влияют электронное строение (5f14 7s2), эффект актиноидного сжатия и низкая электроотрицательность.
Содержание страницы
- 1. Почему +2 — самая устойчивая степень окисления у нобелия
- 2. Степень окисления нобелия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему нобелий предпочитает заряд +2?
- 4. 4 способа определить степень окисления нобелия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления нобелия
- 6. Шпаргалка для нобелия
- 7. Нобелий вне учебника: что скрывает наука?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +2 — самая устойчивая степень окисления у нобелия
Причина стабильности двухвалентного состояния — достижение максимально устойчивой электронной оболочки.
- В простом веществе (No0): Заряд равен 0. Конфигурация:
[Rn] 5f14 7s2. - В двухвалентном ионе (No+2): Нобелий теряет 2 электрона с 7s-подуровня, оставляя заполненный 5f14. Конфигурация:
[Rn] 5f14.

Рис. 2. Схема образования степени окисления +2: удаление внешних 7s-электронов и превращение нобелия в стабильный катион No2+.
Степень окисления нобелия в соединениях
В зависимости от условий, нобелий в соединениях проявляет степень окисления, определяющую его ограниченный химический характер:
- Хлорид нобелия(II) (NoCl2): No +2.
- Оксид нобелия(II) (NoO): No +2.
- Сульфат нобелия(II) (NoSO4): No +2.
Высшая степень окисления
Высшая степень окисления No равна +3. В этом состоянии нобелий существует крайне непродолжительное время и сразу пытается восстановиться до +2.
Низшая степень окисления
Для нобелия характерна степень окисления 0 в металлическом виде. Отрицательные степени окисления для него теоретически невозможны.
Промежуточные степени окисления
Степень окисления нобелия в веществах почти всегда +2. Другие состояния — это скорее результат редких экспериментальных наблюдений.
Важно: Нобелий назван в честь Альфреда Нобеля. Изучение его химии — это проверка теории о стабильности электронных оболочек в тяжелых элементах.
Почему нобелий предпочитает заряд +2?
Характер взаимодействия продиктован его положением в конце ряда актиноидов:
- Положительная СО (+): Нобелий — металл, он отдает электроны.
- Завершенный f-слой: Стабильность 5f14 делает ион No2+ уникально устойчивым среди всех трансуранов.
4 способа определить степень окисления нобелия
По таблице Менделеева
- Семейство: f-элемент.
- Валентные электроны: 2 электрона (7s2).
- Атомная масса нобелия: ~259 а.е.м.
По валентности (Число связей)
Обычно валентность нобелия принимают равной II.
- В NoCl2: Нобелий образует две связи, СО — +2.
По электронной конфигурации
- Электронная формула нобелия: [Rn] 5f14 7s2.
- Атому нобелия степени окисления +2 достичь легче, так как это создает конфигурацию 5f14.
По химическому соединению (Алгебраический расчет)
Пример для NoO:
Сумма СО равна 0. Кислород -2. Обозначим нобелий как x.
x + (-2) = 0 ⇒ x = +2
Примеры степеней окисления нобелия
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +2 | Наиболее стабильная. Стандарт для нобелия. | NoCl2, NoO |
| +3 | Окислительная. Крайне нестабильна. | NoCl3 |
| 0 | Металл. Простое радиоактивное вещество. | No (металл) |
Шпаргалка для нобелия
- +2 — доминирующая степень окисления, аномалия среди актиноидов.
- +3 — проявляется редко, как вынужденное состояние.
- Электронная стабильность — причина уникальной устойчивости иона No2+.
Нобелий вне учебника: что скрывает наука?
+1: Ведутся дискуссии о возможности существования No (I), но экспериментальных подтверждений нет.
Интересный факт: Нобелий — это тот элемент, который заставляет химиков пересматривать теорию актиноидного сжатия, так как он «ломает» привычную картину поведения +3 элементов в этой группе.
Пример решения задачи:
▶️ Дано:
Соединение: NoCl2.
⌕ Найти:
Определите СО нобелия.
✨ Решение:
Хлор -1, два атома хлора -2. Для нейтральности No равен +2.
✅ Ответ:
No(+2).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 3, 5.
Разбор ошибок:
4 — неверно: нобелий — типичный металл.
Часто задаваемые вопросы
В химических соединениях — СО +2, в виде металла — СО 0.
В обычных условиях это состояние не получено.
Низкая электроотрицательность и типичные металлические свойства исключают это.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.