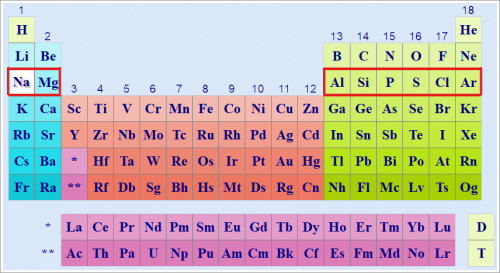
Третий период периодической системы элементов начинается с элемента натрия (Na) и заканчивается элементом аргоном (Ar).
Он включает в себя следующие элементы:
Все эти элементы имеют общую особенность: их валентные электроны расположены в третьем энергетическом уровне.
Элементы третьего периода демонстрируют разнообразие свойств.
Например, натрий и магний являются металлами, тогда как алюминий имеет как металлические, так и неметаллические характеристики.
Кремний и фосфор представляют неметаллы, а сера и хлор относятся к более реакционно способным неметаллам.
Содержание страницы
Физические свойства элементов третьего периода
Три первых элемента — натрий, магний и алюминий — являются металлами. Они имеют высокие температуры плавления и температуры кипения, которые повышаются при переходе от элемента к элементу.
Эта тенденция отражает упрочнение связей в кристалле. Одновременно с повышением температур плавления и температур кипения наблюдается уменьшение атомного объема.
Свойства элементов третьего периода периодической таблицы
| Свойства | Na | Mg | Al | Si | Р | S | Сl | Аr |
| Порядковый номер | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| Атомный вес | 22,9 | 24,3 | 26,9 | 28 | 30,9 | 32 | 35,4 | 39,9 |
| Молекулярная формула | Металл | Металл | Металл | Кристаллический | Р4 | S8 | Сl2 | Аr |
| Температура кипения °К | 1162 | 1393 | 2600 | 2628 | 553 | 718 | 238,9 | 87 |
| Температура кипения °С | 889 | 1120 | 2327 | 2355 | 280 | 445 | —34,1 | — 186 |
| Температура плавления °К | 371 | 923 | 933 | 1683 | 317,2 | 392 | 172 | 84 |
| Температура плавления °С | 98 | 650 | 660 | 1410 | 44,2 | 119 | —101 | —189 |
| Атомный объем в твердом состоянии, см3/моль атомов | 27,3 | 14,0 | 9,99 | 12,1 | 16,9 | 15,6 | 18,7 | 24,2 |
Четвертый элемент — кремний — твердое вещество, в котором каждый атом кремния связан с четырьмя соседними атомами кремния, расположенными на одинаковом расстоянии друг от друга (в вершинах правильного тетраэдра).
Такое расположение атомов приводит к образованию трехмерной структуры; эти твердые соединения называются сетчатыми.
Твердое вещество с такой структурой характеризуется высокой температурой плавления и высокой температурой кипения.
Остальные четыре элемента образуют молекулярные твердые вещества.
Атомы белого фосфора, серы и хлора прочно связаны в небольшие молекулы (они имеют формулы Р4, S8 и Сl2), но притяжение между молекулами незначительно.
Разумеется, изменение свойств у этих элементов не носит простого характера, так как их молекулы построены весьма различно.
Соединения элементов третьего периода
Для того чтобы лучше изучить изменение химических свойств элементов расположенных в горизонтальном ряду, рассмотрим три типа соединений:
Гидриды
Гидриды — это соединения элементов с водородом. Горячий , расплавленный металлический натрий реагирует с газообразным водородом, образуя твердый, солеобразный гидрид с эмпирической формулой NaH.
Предполагают, что в твердом гидриде натрия присутствуют ионы Na+ и Н—. Ион Н— существует в твердом гидриде или в расплаве, но не может существовать в водном растворе.
Магний образует аналогичный солеобразный гидрид, имеющий эмпирическую формулу MgH2.
Нейтральный атом магния отдает два электрона, превращаясь в положительно заряженный ион Mg2+ (с устойчивой электронной конфигурацией инертного газа).
Алюминий образует гидрид молекулярного, а не солеобразного характера. Однако его эмпирическая формула АlН3.
Остальные элементы образуют гидриды, которые представляют собой молекулярные газообразные соединения. Они имеют формулы SiH4, PH3, H2S и НСl соответственно.
Мы видим закономерность в соотношениях взаимодействующих атомов. Элементы натрий и магний (и до некоторой степени алюминий) приобретают электронную конфигурацию неона, отдавая электроны атомам водорода — по одному электрону каждому атому водорода.
Следует отметить, что при этом каждый атом водорода приобретает электронную конфигурацию гелия.
Начиная с кремния, образование молекулярных соединений указывает на то, что элементы принимают электронную конфигурацию последующего инертного газа (аргона) путем образования обобщенных электронных пар с атомами водорода.
В этих соединениях связь с атомами водорода напоминает скорее ковалентную связь в молекуле Сl2, чем ионную связь в молекуле хлористого натрия.
Однако независимо от природы химической связи реакционная способность каждого элемента зависит от склонности атома к приобретению электронной конфигурации предшествующего или последующего инертного газа.
Хлориды и окислы
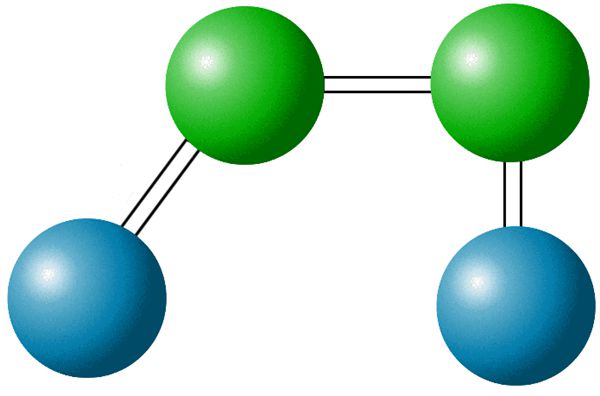
Рис. 2.Строение молекулы S2Cl2.
Такую же зависимость реакционной способности от строения мы можем обнаружить при рассмотрении хлоридов и окислов.
Мы снова находим, что химическую связь можно объяснить отдачей электронов или образованием обобщенной пары электронов, в результате чего приобретается устойчивая конфигурация инертного газа.
Единственной аномалией является способность серы к образованию соединения S2Cl2. Однако аномалия эта чисто внешняя, так как структура этого соединения показывает, что валентность серы в нем равна 2.
Структура хлористой серы приведена на рис. 2.
Атомы в этой молекуле расположены таким образом, что каждый атом серы обладает одной обобщенной парой электронов совместно с атомом хлора.
А другой — совместно со вторым атомом серы, благодаря чему достигается электронная конфигурация аргона.
Выводы
Изменение типа строения молекул (молекулярных формул) при переходе от щелочного металла к инертному газу, наблюдаемое у элементов третьего периода, показывает важность электронной конфигурации инертного газа.
Ценность этих закономерностей вполне очевидна. По положению двух атомов в периодической таблице элементов можно предсказывать наиболее вероятные молекулярные формулы.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.