Регенерация электролита меди
Обновление или очистка электролита необходимы для предупреждения накопления примесей и удаления избытка меди, которая накапливается из-за частичного растворения химическим путем при участии кислорода воздуха:
2Cu + O2 + 2H2SО4=2CuSО4+2H2O.
Кроме того, в анодах содержится Cu2О, она растворяется по уравнению. В итоге в электролит переходит на 0,5—1% больше меди, чем осаждается на катодах. От постоянного накопления может начаться кристаллизация CuSО4•5H2О, особенно на поверхности анодов, близ которых концентрация Сu2+ наиболее высокая.
Если содержание примесей невелико и требуется только удалить избыток меди, часть электролита подвергают электролизу в ваннах с нерастворимыми свинцовыми анодами. Медь при этом осаждается на катодах, а на анодах выделяется кислород, в растворе накапливается свободная серная кислота. После некоторого обеднения раствор можно возвратить в систему циркуляции. Напряжение при электролизе с нерастворимым анодом около 2,0 В, а расход энергии почти в 10 раз больше.
По мере обеднения раствора медью и усиления концентрационной поляризации потенциал катода все более сдвигается в отрицательном направлении пока не достигнет величины, достаточной для разряда ионов меди вместе с водой.
Сu2+ + Н2O + 2е = СuО + Н2; Е0= — 0,22 В.
Начало этой реакции обнаруживается по появлению черного, рыхлого осадка, слабо прикрепленного к катоду.
Приведенного выше нормального потенциала в литературе найти не удалось, мы его вычислили по уравнению. Чтобы не ошибиться в знаке, следует реакцию переписать, показав справа ее окислительную часть:
Подобно этому можно вычислить термодинамические потенциалы других окислительно-восстановительных систем.
Возвращаясь к примеру, легко пояснить сравнительно высокий практический расход энергии на электролиз против расчетного. На нерастворимом свинцовом аноде кислород выделяется с перенапряжением. Потенциал (38) от этого увеличится приблизительно на 0,6 В и станет равным 1,38 В. Потенциал разряда ионов меди на катоде примем 0,3 В, а падение напряжения в цепи ванны и поляризацию по примеру рафинирования меди — также 0,3 В. Тогда общее напряжение на ванне составит
υ= 1,83+ 0,3 — 0,3= 1,83 В.
Средний выход по току при электролизе на истощение зависит от остаточной концентрации, пусть он будет 75%. Подставляя все это в уравнение, найдем расход энергии на осаждение 1 т меди с нерастворимым анодом
w = 0,84•103(1,83 : 0,75) = 2060 кВт•ч.
Если необходимо не только обеднить раствор, но и удалить примеси, электролитический способ невыгоден: потребовалось бы предварительное осаждение всей меди с низким виходом по току и получением рыхлого осадка. В этом случае выведенную часть электролита нейтрализуют медной окалиной или гранула-ми меди при нагревании и продувке воздуха . Горячий раствор сливают в кристаллизаторы, где выпадают кристалла CuSО4•5H2О. Маточный раствор выпаривают и вновь кристаллизуют, получая дополнительно медный купорос. Иногда для выпарки и кристаллизации применяют вакуумные аппараты.
Часто пользуются комбинированным способом регенерации, по которому одну порцию электролита подвергают электролизу только для обеднения медью и возвращают в циркуляцию; другую перерабатывают на медный купорос, а из маточного раствора полностью осаждают медь электролизом и выкристаллизовывают никелевый купорос NiSО4•7H2О, если никель накапливается в электролите.
Переработка шлама меди
Шлам выгружают, периодически очищая ванны, и натравляют на переработку; состав его приведен выше. При переработке необходимо извлечь главные ценные составляющие шлама — благородные металлы, селен и теллур.
Прежде всего удаляют медь, выщелачивая ее горячим раствором серной кислоты при продувке воздухом. Остаток спекают с содой. Селен и теллур образуют при этом растворимые в воде селениты и теллуриты натрия — Na2SeО3 и Na2TeО3. Селен также частично улетучивается в виде SeО2; его улавливают из газов и пускают в оборот.
Спек выщелачивают водой, а из полученных растворов выделяют селен и теллур. Остаток от выщелачивания плавят с содой и окислителями, получая сплав золота и серебра — металл доре, который отправляют на аффинажные заводы, где очищают от примесей и разделяют на золото и серебро . Известны и другие способы переработки шламов.
Статья на тему Регенерация электролита меди

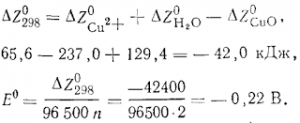
Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.