ПОЛУЧЕНИЕ КРИОЛИТА
Криолит встречается в природе, однако известно только одно его промышленное месторождение — на западном побережьи Гренландии. Поэтому все страны получают криолит, а также AlF3 и NaF искусственно из плавикового шпата.
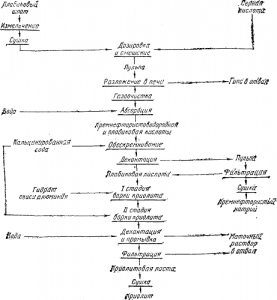
Из природного плавикового шпата получают концентрат, содержащий до 96% CaF2. Из концентрата криолит и другие фтористые соли получают кислотным способом (рис.). Плавиковый шпат нагревают в смеси с крепкой серной кислотой до 200° С в трубчатых вращающихся печах; при этом получается фтористый водород и сульфат кальция по реакции
CaF2 + H2SO4 = CaSO4 + 2HF.
Наряду с фтористым водородом образуется кремнефтористый водород:
SiO2 + 4HF = SiF4 + 2Н2O,
SiF4+2HF = H2SiF6.
Необходимо отметить, что вся аппаратура этого производства требует тщательной герметизации, так как выделяющиеся газы очень ядовиты.
Рис., Технологическая схема производства криолита кислотным способом
Последняя реакция протекает обычно вне печи (в газоходах и башнях). Газообразные продукты реакции поглощаются водой в башнях, в результате чего получается раствор плавиковой кислоты с примесью кремнефтористоводородной кислоты.
Для очистки плавиковой кислоты к ней добавляют соду, причем выпадает малорастворимый кремнефтористый натрий
H2SiF6 + Na2CO3 = Na2SiF6 + H2O + CO2
Эта операция по аналогии с очисткой растворов от кремнезема в глиноземном производстве называется обескремниванием.
В Очищенной плавиковой кислоте сначала растворяют строго по расчету гидроокись алюминия в соответствии с реакцией
12HF + Аl2O3 • 3Н2O = 2H3AlF6 + 6Н2O.
Полученную фторалюминиевую кислоту в этом же аппарате нейтрализуют содой, в результате чего выпадает малорастворимый криолита
2H3AlF6 + 3Na2CO3 = 2Na3AlF6 + 3H2O + 3СО2
Криолиту отделяют от раствора, промывают и сушат при 140—160° С.
Для получения других фтористых солей плавиковую кислоту полностью нейтрализуют гидратом окиси алюминия (для получения AlF3), либо содой (для получения NaF).
Кислотный способ производства криолита имеет серьезные недостатки: высокую токсичность (HF и H2SiF6 — ядовитые газы), необходимость в дорогой кислотоупорной аппаратуре, низкое извлечение фтора в криолит.
Pазработаны и другие способы получения криолита, которые пока не получили промышленного применения. Заслуживает внимания щелочной способ получения криолита, разработанный Б. А. Кузьминым под руководством А. И. Лайнера. Сущность этого способа заключается в спекании плавикового шпата с поташом и аморфным кремнеземом (трепел и др.). Полученный спек, содержащий хорошо растворимый KF, легко выщелачивают и из отфильтрованного раствора содой осаждают кристаллы фтористого натрия. Вводя эти кристаллы в алюминатный раствор, осаждают натриевый криолит. Этот способ можно осуществлять в обычной стальной и чугунной аппаратуре. Протекающие процессы не связаны с выделением паров плавиковой кислоты и поэтому не вредны для обслуживающего персонала.
Статья на тему Получение криолита

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.