Техническая азотная кислота
Получение азотной кислоты осуществляется тремя способами, которые мы опишем в том порядке, в каком они начали применяться в промышленности.
1.Получение азотной кислоты из селитры. Наиболее старый способ получения азотной кислоты, которым пользовались уже в середине XVII в., заключается в нагревании натриевой селитры с концентрированной серной кислотой: NaNО3 + H2SО4 = NaHSО4 + HNО3
Выделяющиеся при нагревании пары азотной кислоты направляются в охлаждаемый водой приемник, где они сгущаются в жидкость. При слабом нагревании и избытке серной кислоты реакция идет с образованием кислой соли. Если же взять достаточное количество селитры и нагревать сильнее, то получается нормальная соль:
2NaNО3 + H2SО4 = Na2SО4 + 2HNО3
Однако при этом происходит значительная потеря азотной кислоты вследствие ее разложения. Поэтому процесс ведут таким образом, чтобы реакция протекала по первому уравнению.
До начала текущего столетия описанный способ получения азотной кислоты был единственным применяемым в промышленности. Затем он был почти полностью вытеснен другими способами, основанными на фиксации атмосферного азота.
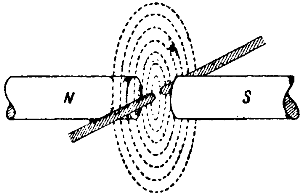
2. Получение азотной кислоты из воздуха дуговым методом. В основе этого метода, впервые технически осуществленного в Норвегии в 1905 г., лежит описанная в реакция непосредственного соединения азота с кислородом. Необходимая для этой реакции высокая температура получается при помощи электрической душ, питаемой мощным источником электрического тока. Если пламя электрической дуги поместить между двумя полюсами сильного электромагнита (рис. 98), то оно принимает форму плоского диска, вследствие чего поверхность пламени сильно увеличивается. Этот огненный диск, достигающий 3 м в диаметре, образуется в сложенной из огнеупорных кирпичей специальной печи, температура в которой достигает 3000—3500°. Стенки печи пронизаны каналами, через которые в печь вдувается воздух. Приходя в соприкосновение с пламенем электрической дуги, воздух сильно нагревается, и в нем образуется некоторое количество окиси азота.
Выходящие из печи газы, содержащие 2—3% окиси азота, быстро охлаждают до 1000—1100°, чтобы образовавшаяся окись азота не могла разложиться обратно на азот и кислород. В процессе дальнейшего охлаждения газовой смеси окись азота присоединяет кислород, переходя в двуокись азота, которая поглощается водой и превращается в азотную кислоту.
Получение азотной кислоты описанным методом связано с затратой большого количества электрической энергии. Наибольшее развитие этот метод получил в Норвегии, располагающей значи-тельными ресурсами дешевой электроэнергии. К 1925 г. мировое производство азотных соединений, получаемых по дуговому методу, достигло 42 000 т в год в пересчете на азот. Однако в последнее время дуговой метод применяется в сравнительно небольших масштабах, так как оказалось экономически выгоднее получать азотную кислоту новым методом — окислением синтетического аммиака.
3. Получение азотной кислоты окислением аммиака. Наиболее важным из современных способов получения азотной кислоты является каталитическое окисление аммиака кислородом воздуха. При описании свойств аммиака было указано , что он горит в кислороде, причем продуктами реакции являются вода и свободный азот. Но в присутствии катализаторов окисление аммиака может протекать иначе. Если, например, пропускать смесь аммиака с воздухом сквозь накаленную сетку из платиновой проволоки, служащей катализатором, то при 750° и определенном составе смеси происходит почти количественное превращение аммиака в окись азота:
4NH3 + 5О2 = 4NO + 6Н2О + 216,7 ккал
Окись азота легко переходит в двуокись азота, которая с водой образует азотную кислоту.
Возможность каталитического окисления аммиака в азотную кислоту была известна давно, но только в начале XX в. удалось использовать этот процесс для заводского получения азотной кислоты. В первых аппаратах для окисления аммиака катализатором служила платина. В настоящее время применяют преимущественно сплав платины с родием, содержащий 5—10% родия. Выход окиси азота составляет 96—98%.
На рис. 99 представлена схема заводской установки для окисления аммиака при атмосферном давлении. Освобожденный фильтрованием от механических примесей воздух подается вентилятором 1 в теплообменник 2, где он нагревается выходящими из контактного аппарата газами примерно до 300°, и затем поступает в смеситель 3. Сюда же вентилятором 4 подается газообразный аммиак. Изсмесителя аммиачно-воздушная смесь, содержащая 10—11% аммиака, поступает в контактный аппарат 5, состоящий из двух полых конусов, соединенных основаниями. В широкой части аппарата закреплены горизонтально несколько сеток из тонких платино-родиевых нитей, служащих катализатором. В контактном аппарате происходит окисление аммиака в окись азота.
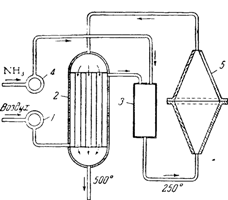
Выходящая из контактного аппарата горячая газовая смесь направляется в теплообменник. Здесь горячие газы охлаждаются до 500—550°, после чего их пропускают последовательно через паровой котел (для использования тепла), особые холодильники и, наконец, поглотительные башни, где в основном и происходит окисление окиси азота в двуокись и образование азотной кислоты.
Получаемая из башен кислота обычно содержит 50—55% HNО3. Превращение ее в более концентрированную кислоту достигается путем перегонки с серной кислотой, которая служит удерживающим воду средством. Кроме того, в последнее время разработан способ получения концентрированной азотной кислоты взаимодействием жидкой двуокиси азота с водой (или с разбавленной азотной кислотой) в присутствии кислорода под давлением 50 ат при температуре 75°. Реакция протекает по суммарному уравнению
2N2О4 + О2 + 2Н2О = 4HNО3 + 14,2 ккал
По этому способу, называемому «прямым синтезом», получают сразу 98%-ную азотную кислоту.
В настоящее время большая часть азотной кислоты, вырабатываемой в огромных количествах, получается окислением аммиака. А так как главная масса аммиака получается путем синтеза из элементов, то в конечном счете этот способ, как и предыдущий, основан на фиксации атмосферного азота.
Основоположником отечественного производства синтетической азотной кислоты был инженер И. И. Андреев, который в 1914 г. впервые поставил вопрос об организации в России производства азотной кислоты окислением аммиака, образующегося при коксовании угля. Андреев тщательно изучил реакцию окисления аммиака на изготовленных под его руководством катализаторах и построил опытную промышленную установку. Полученные на этой установке экспериментальные данные были использованы при составлении проекта первого завода синтетической азотной кислоты, который был построен в Юзовке (ныне Сталино, Донецк) и пущен в ход в июле 1917 г. Опыт работы этого завода был широко использован советскими инженерами при проектировании новых заводов, построенных в годы первых пятилеток.
Вы читаете, статья на тему Техническая азотная кислота

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.