Адсорбция
Как указывалось выше, уголь обладает свойством поглощать на своей поверхности различные вещества. Поглощение газов, паров и растворенных веществ поверхностным слоем других веществ называется адсорбцией . Поглотителями, или адсорбентами, могут быть как твердые вещества, так и жидкости; однако наилучшими адсорбентами являются твердые вещества.
Явление адсорбции объясняется тем, что частицы, расположенные на поверхности вещества, находятся в иных условиях, чем частицы, лежащие внутри него. Внутри вещества все действующие между частицами силы взаимно уравновешиваются, а на поверхности вещества уравновешены только силы, направленные внутрь вещества и в плоскости самой поверхности. Поэтому поверхностный слой может притягивать к себе частицы изсоприкасающейся с ним жидкой или газообразной фазы. Во многих случаях адсорбированный слой частиц является мономолекулярным, т. е. имеет толщину одной молекулы.
Адсорбированные молекулы совершают определенные колебания. Некоторые из молекул отрываются и переходят обратно в окружающую среду, на их место поступают новые молекулы, и в результате устанавливается определенное состояние адсорбционного равновесия, при котором в единицу времени столько же молекул поглощается поверхностью, сколько и покидает ее.
Состояние адсорбционного равновесия зависит как от концентрации поглощаемого вещества в соприкасающейся садсорбентом фазе, так и от температуры. С увеличением концентрации абсолютное количество адсорбированных молекул растет, хотя в процентном отношении их адсорбируется меньше, чем при малых концентрациях.
Смещение равновесия при изменении температуры определяется тем, что адсорбция сопровождается выделением тепла. Поэтому, согласно принципу Ле-Шателье, повышение температуры смещает адсорбционное равновесие, вызывая десорбцию, т. е. обратное выделение адсорбированных молекул. Понижение температуры, наоборот, увеличивает количество адсорбированного вещества.
Таблица 23
Содержание страницы
Увеличение поверхности вещества при его дроблении
| Длина ребра куба | Число кубиков в см3 | Общая поверхность | Длина ребра куба | Число кубиков в 1 см3 | Общая поверхность |
| 1 см 1 мм
0,1 мм 0,01 мм |
1103
106 109 |
6 см260 см2
600 см2 6000 см2 |
1 μ.1 mμ
0,1 mμ |
10121021
1024 |
6 м2 6000 м2
60000 м2 |
Так как адсорбция есть явление, происходящее только на поверхности вещества, то понятно, что чем больше общая поверхность адсорбента, тем больше молекул он может поглотить. Поэтому вещества пористые и порошкообразные, как правило, обладают большей поглотительной способностью, чем вещества, не имеющие пор. Наглядное представление о том, как сильно увеличивается поверхность вещества при его дроблении, дает табл. 23. В ней показано увеличение поверхности куба с ребром в 1 см при последовательном делении его на кубики с ребром 1 мм, 0,1 мм и т. д. Особенно большой адсорбционной способностью обладает обыкновенный древесный-уголь, что в значительной мере объясняется его пористым строением.
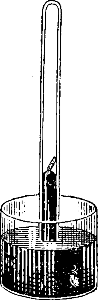
Чтобы наблюдать поглощение газов углем, произведем следующий опыт. Наполним аммиаком стеклянный цилиндр и опустим открытый конец его в чашку с ртутью (рис. 105). Затем, прокалив на горелке кусочек древесного угля, погрузим его для охлаждения в ртуть и подведем под отверстие цилин-дра с аммиаком. Уголь всплывает на поверхность ртути в цилиндре, и ртуть сейчас же начинает подниматься вверх вследствие поглощения аммиака углем.
Количество поглощаемого адсорбентом газа зависит как от свойств адсорбента, так и от природы газа. При этом наблюдается некоторая закономерность, состоящая в том, что газ, как правило,
поглощается тем лучше, чем выше его критическая температура, т. е. чем легче он сжижается.
В табл. 24 указаны количества различных газов в миллилитрах, адсорбируемые 1 г древесного угля при 15° и нормальном давлении.
Таблица 24
Адсорбция газов углем
| Адсорбируемое вещество | Темп. кип. в °С | Количествоадсорбированного газа в мл | Адсорбируемое вещество | Темп. кип. в°С | Количество хадсорбиро-ванногогаза в мл |
| Сернистый газ Хлор
Аммиак Сероводород |
— 10,1— 34
— 33,4 — 60,7 |
380 235
181 99 |
Углекислый газ МетанКислород | — 78,5— 161,5
— 183 — 252,7 |
47,6 16,2
8,2 4,7 |
Особенно хорошо поглощает газы активированный уголь. Один из лучших способов приготовления активированного угля заключается в том, что обыкновенный березовый уголь подвергают сильному нагреванию в струе водяного пара. От такой обработки уголь становится очень пористым и его поглотительная способность резко увеличивается .
Активированный уголь применяется для поглощения паров летучих жидкостей из воздуха и газовых смесей. Бензин, например, улавливается активированным углем из природных газов, выделяющихся в больших количествах в нефтеносных районах. Поглощение летучих жидкостей углем и другими адсорбентами, с последующей десорбцией поглощенных веществ, широко применяется в промышленности и позволяет экономить значительные количества ценных растворителей.
Сильно охлажденный активированный уголь служит прекрасным средством для получения высоких степеней разрежения, поглощая последние следы газа, которые уже не могут быть удалены вакуум-насосом. Активированный уголь используется также в качестве катализатора в некоторых химических производствах.
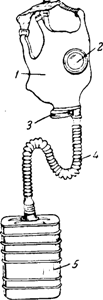
Во время первой мировой войны 1914—1918 гг. активированный уголь был использован, по предложению Н. Д. Зелинского, для защиты органов дыхания от отравляющих веществ. Наполненные активированным углем «противогазы Зелинского» спасли во время первой мировой войны десятки тысяч русских солдат от мучительной смерти. Активированный уголь применяется и в современных противогазах (рис. 106).

Николай Дмитриевич Зелинский родился в 1861 г. в г. Тирасполе. По окончании в 1884 г. Новороссийского университета (в Одессе) он был оставлен при нем для научной работы. В 1891 г. Зелинский защитил докторскую диссертацию, посвященную исследованию явлений стереоизомерии. В 1893 г. он получил кафедру органической и аналитической химии в Московском университете, в котором и работал до конца своей жизни. В 1929 г. Н. Д. Зелинский был избран действительным членом Академии наук СССР.
Диапазон научных интересов Н. Д. Зелинского был необычайно широк. Работы Зелинского и его учеников в области органического катализа заняли ведущее место в мировой науке. Исключительный интерес представляют исследования Зелинского в области нефти и гидролиза белковых соединений, впервые давшие указания на циклическую структуру белковых молекул.
Адсорбция углем растворенных веществ была открыта в конце XVIII в. русским академиком Т. Е. Ловицем, применившим уголь для очистки -винного спирта. С тех пор на винокуренных заводах винный спирт очищают от содержащихся в нем примесей (так называемых сивушных масел) фильтрованием через уголь. На сахарно-рафинадных заводах таким же путем производят очистку сахара от веществ, сообщающих ему желтоватую окраску.
Кроме угля, ярко выраженной способностью к адсорбции обладает и целый ряд других веществ. Так, например, на адсорбции растворенных веществ растительными и животными волокнами основаны процессы крашения тканей, дубления кож и др.
Различные вещества по-разному адсорбируются на одном и том же адсорбенте. Используя это явление, русский ученый-ботаник М. С. Цвет (1872—1919) разработал метод хроматографического («цветного») анализа, успешно примененный им для разделения пигмента зеленых листьев растений — хлорофилла, состоящего из двух весьма близких по строению веществ. Он извлек хлорофилл из листьев бензином и пропустил раствор через стеклянную колонку, плотно набитую углекислым кальцием. Окрашенный бензин, пройдя через колонку, обесцветился, а отдельные пигменты, последовательно адсорбируясь на углекислом кальции, образовали в цилиндрической колонке ряд цветных колец. Вынув из колонки столбик углекислого кальция, Цвет разделил его на окрашенные кольца, извлек из каждого кольца адсорбированное вещество соответствующим растворителем и таким образом получил химически чистые виды хлорофилла.
Рис. 106. Противогаз: 1- резиновая маска, 2- очки, 3- выдыхательный клапан, 4- гофрированная трубка, 5- поглотительная коробка.
Создав необычайно тонкий метод адсорбционного анализа. Цвет осуществил заветную мечту химиков — разделять смесь родственных химических соединений на отдельные компоненты, не подвергая ее активным химическим или физическим воздействиям. Хроматографический метод в настоящее время широко применяется во всякого рода исследованиях. С помощью этого метода на современных производствах получают чистейшие препараты различных витаминов, гормонов, пенициллина и других веществ.
Академиком П. А. Ребиндером установлено влияние адсорбции на механическую прочность различных материалов. Им показано, что при адсорбции твердыми телами так называемых поверхностно-активных веществ, т. е. веществ, значительно понижающих поверхностное натяжение жидкостей, молекулы их «расклинивают» мельчайшие трещины в твердых телах, уменьшая прочность последних. Это явление имеет важное значение в практике бурения горных пород, при механической обработке сплавов и т. п.
Вы читаете, статья на тему Адсорбция

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.