Теория:
Эйнштейний (Es) занимает положение в 7‑м периоде, что определяет его принадлежность к ряду тяжелых трансурановых элементов — актиноидов.
Будучи химическим гомологом (аналогом) лантаноида гольмия, он проявляет свойства типичного радиоактивного металла.
Его поведение в растворах и кристаллической решетке продиктовано заполнением 5f-подуровня.
А его нахождение в 3‑й группе (семейство актиноидов) задает ключевые параметры: наиболее характерную валентность III.
А также возможную степень окисления +2, которая становится более доступной из-за специфики электронного строения в конце ряда.
Структура атома подтверждается его электронной формулой (конфигурацией):
[Rn] 5f11 7s2.
На которой наглядно можно определить его положение как представителя f-блока, находящегося за калифорнием и перед фермием.
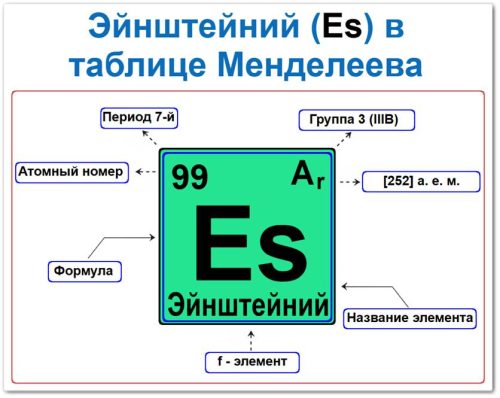
Эйнштейний в таблице Менделеева можно определить на основании закона периодичности: положение в группе и периоде, а также порядкового номера / атомный номер (Z = 99)
Содержание страницы
- 1. Как определить положение Эйнштейния в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 99)
- 3. Название и символ
- 4. Группа (3 / III B)
- 5. Период (7‑й)
- 6. Относительная атомная масса (Ar)
- 7. f‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Эйнштейния по Таблице Менделеева
- 9. Проверка знаний: Как определить Эйнштейний по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Эйнштейния в Таблице Менделеева
Локация эйнштейния в таблице описывается характеристиками его радиоактивного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (вертикальный ряд актиноидов).
- Период (горизонтальный ряд).
- Электронное семейство (эйнштейний — f‑элемент).
Порядковый номер / атомный номер (Z = 99)
- Служит уникальным кодом элемента в ряду искусственно полученных трансуранов.
- В ядре — 99 протонов; в нейтральной оболочке — 99 электронов.
- Электронное строение: [Rn] 5f11 7s2.
Важно: Наличие 11 электронов на 5f-подуровне определяет его магнитные свойства и химическое сходство с гольмием (семейство лантаноидов).
Название и символ
- Название: «эйнштейний» (в честь великого физика-теоретика Альберта Эйнштейна).
- Символ: Es.
- Примечание: Элемент был открыт в 1952 году группой Гиорсо при анализе радиоактивных осадков после термоядерного испытания «Айви Майк».
Группа (3 / III B)
Расположен в 3‑й группе (в ряду актиноидов), которая объединяет элементы со схожими свойствами внешних оболочек.
Химический потенциал:
- Валентность эйнштейния: доминирующая валентность III.
- Степень окисления: наиболее стабильна +3, но эйнштейний стал первым тяжелым актиноидом, для которого была получена устойчивая степень окисления +2 в твердом теле.
Период (7‑й)
Находится в 7‑м периоде — его электроны распределены по семи энергетическим уровням.
Влияние на свойства:
- Актиноидное сжатие: Как и у всех элементов этого ряда, радиус иона Es3+ закономерно уменьшается по сравнению с предыдущими элементами.
- Радиогенность: Высокая удельная активность делает эйнштейний самосветящимся в темноте из-за интенсивного альфа-излучения, которое возбуждает окружающую среду.
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
Относительная атомная масса (Ar)
- Ar(Es) ≈ [252] а.е.м. (для наиболее стабильного изотопа 252Es).
- Определение: средняя масса долгоживущего нуклида.
- Стабильность: Эйнштейний — последний из элементов, который можно получить в весомых (миллиграммовых) количествах в реакторах. Период полураспада 252Es составляет около 471 дня.
Все значения для всех элементов можно узнать в таблице атомных масс.
f‑Элемент (электронное семейство)
Застраивающимся является 5f‑подуровень (5f11).
Специфика блока: Это типичный представитель f-блока. Его свойства во многом определяются тем, что f-электроны глубоко экранированы внешними оболочками, что ограничивает их участие в образовании химических связей.
Определение энергетических уровней Эйнштейния по Таблице Менделеева
Положение Эйнштейния (Es) в системе Менделеева — это готовый «паспорт» его внутреннего устройства.
1. 7-й период (Количество этажей)
Эйнштейний находится в седьмой строке таблицы. Номер периода определяет число электронных слоев.
- Итог: У Эйнштейния 7 энергетических уровней.
2. Список «жильцов» (Распределение электронов)
Атомный номер Эйнштейния — 99. Его 99 электронов распределены по уровням следующим образом:
Es ) 2 ) 8 ) 18 ) 32 ) 29 ) 8 ) 2
Для сравнения: У соседа слева, Калифорния (98), на пятом уровне 28 электронов, а у Эйнштейния (99) — 29.
3. 3-я группа (Химический характер)
Эйнштейний входит в семейство актиноидов.
- f-элемент: Его свойства диктуются 5f-оболочкой.
- Место в блоке: Он является «тяжелым аналогом» гольмия, что подтверждается сходством их спектров поглощения и магнитных моментов.
Проверка знаний: Как определить Эйнштейний по таблице Менделеева
Часто задаваемые вопросы:
Занимает ячейку под номером 99. Он находится в 7-м периоде и принадлежит к семейству актиноидов (f-блок).
Это тяжелый трансурановый элемент, расположенный сразу после Калифорния.
Атомная масса самого стабильного изотопа (252Es) составляет [252] а.е.м. Скобки означают, что у элемента нет стабильных изотопов.
Он настолько радиоактивен, что его ядро постоянно распадается; время жизни самого стойкого изотопа — всего около 472 дней.
Да. Из-за чудовищной радиоактивности кусок Эйнштейния испускает интенсивное голубое свечение.
Выделяемая энергия настолько велика (около 1000 Ватт на грамм), что металл самопроизвольно разогревается и может начать плавиться под действием собственного излучения.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.