Теория:
Хром (Cr) в периодической системе: 4-й период, 6-я группа (по устаревшей классификации — VI B), атомная масса 51,996 а.е.м.
Занимает положение в 4-м периоде, что определяет его принадлежность к переходным металлам (d-блоку).
Хром является одним из важнейших легирующих элементов, придающим сталям твердость и коррозионную стойкость.
Будучи типичным d-элементом, он располагается в центральной части таблицы Менделеева, открывая подгруппу хрома (вместе с молибденом и вольфрамом).
Нахождение Хрома в 6-й группе и наличие пяти неспаренных электронов на d-подуровне обуславливают его ключевые параметры:
Переменную валентность (наиболее характерные II, III и VI).
А также широкое применение в гальванотехнике (хромирование), производстве нержавеющих сталей и создании сверхтвердых сплавов.
Структура атома подтверждается его электронной формулой (конфигурацией):
[Ar] 3d5 4s1.
На которой заметен «провал» (проскок) электрона с s- на d-подуровень для создания более устойчивой полузаполненной конфигурации.
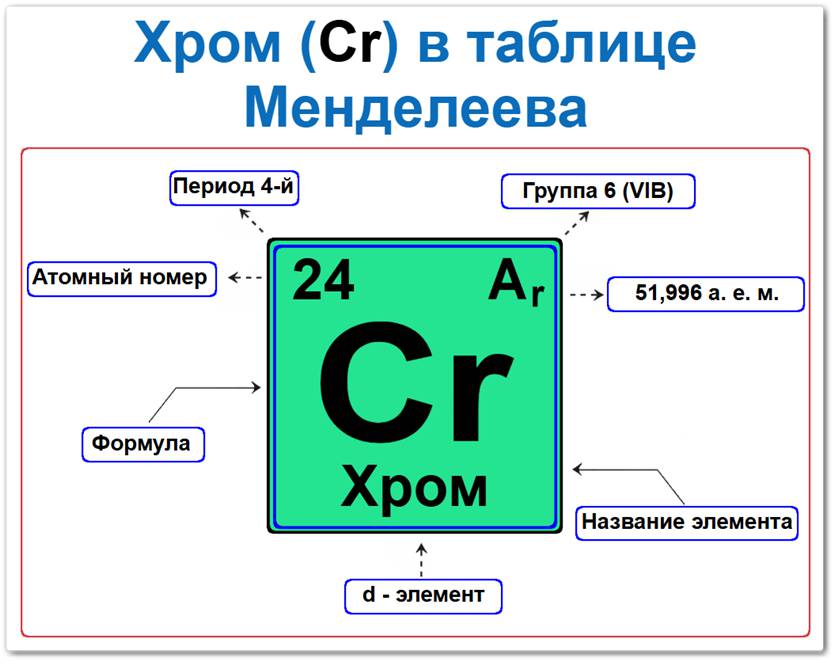
Хром элемент таблицы Менделеева который можно определить на основании закона периодичности: положение в ряду переходных металлов период 4, группа 6, а также по его порядковому номеру (Z = 24).
Содержание страницы
- 1. Как определить положение Хрома в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 24)
- 3. Название и символ
- 4. Группа (6 / VI B)
- 5. Период (4-й)
- 6. Относительная атомная масса (Ar)
- 7. d-Элемент (электронное семейство)
- 8. Определение энергетических уровней Хрома по Таблице Менделеева
- 9. Проверка знаний: Как определить хром по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Хрома в Таблице Менделеева
Локация хрома в таблице описывается характеристиками его атомного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (6-я группа, подгруппа хрома).
- Период (горизонтальный ряд).
- Электронное семейство (хром — d-элемент).
Порядковый номер / атомный номер (Z = 24)
- Служит уникальным кодом элемента в системе.
- В ядре — 24 протона; в нейтральной оболочке — 24 электрона.
- Электронное строение: [Ar] 3d5 4s1.
Важно: Особенность строения (3d5) делает хром самым твердым из чистых металлов, способным царапать стекло.
Название и символ
- Название: «хром» (от греч. «chroma» — цвет, из-за разнообразия окраски его соединений).
- Символ: Cr.
- Примечание: Открыт Луи-Николя Вокленом в 1797 году. В чистом виде — голубовато-белый, очень твердый металл.
Группа (6 / VI B)
Расположен в 6-й группе. В периодической системе хром находится в одной вертикальной колонке с молибденом (снизу), вольфрамом и сиборгий, поэтому они все входят в подгруппу хрома.
Химический потенциал:
- Валентность хрома: переменная, наиболее устойчивые состояния в степенях окисления +3 (амфотерность) и +6 (кислотные свойства).
- Степень окисления: от +1 до +6. Соединения хрома (VI) токсичны и являются сильными окислителями.
Период (4-й)
Находится в 4-м периоде — его электроны распределены по четырем энергетическим уровням.
Влияние на свойства:
- Химическая активность: Хром пассивируется на воздухе, образуя тончайшую защитную пленку оксида Cr2O3, что делает его неуязвимым для коррозии.
- Техническое значение: Основа нихромовых нагревателей и незаменимый компонент инструментальных сталей.
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
Относительная атомная масса (Ar)
- Ar(Cr) ≈ 51,996 а.е.м.
- Определение: среднее значение массы природных изотопов, наиболее распространенным из которых является хром-52.
Все значения для всех элементов можно узнать в таблице атомных масс.
d-Элемент (электронное семейство)
Активно заполняющимся является 3d-подуровень (3d5).
Специфика блока: Как d-элемент, хром проявляет свойства переходного металла, образуя ярко окрашенные комплексные соединения, что широко используется в аналитической химии и производстве красок.
Определение энергетических уровней Хрома по Таблице Менделеева
Положение Хрома (Cr) в системе Менделеева — это готовый «паспорт» его внутреннего устройства.
1. 4-й период (Количество этажей)
Номер периода определяет число электронных слоев.
- Итог: У Хрома 4 энергетических уровня.
2. Список «жильцов» (Распределение электронов)
Атомный номер Хрома — 24. Его 24 электрона распределены по уровням следующим образом:
Cr ) 2 ) 8 ) 13 ) 1
(Обратите внимание на 1 электрон на внешнем слое из-за эффекта «провала»)
3. 6-я группа (Химический характер)
Хром — элемент побочной подгруппы VI группы (или 6-й группы).
- d-элемент: Относится к переходным металлам.
- Металлические свойства: Тугоплавок, обладает исключительной твердостью и характерным металлическим блеском.
Проверка знаний: Как определить хром по таблице Менделеева
Выберите три верных тезиса, которые однозначно характеризуют Хром (Cr) в структуре таблицы.
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3
- 1) Номер 24. Указывает на количество протонов в ядре.
- 2) 4-й период, 6-я группа. Географические координаты элемента в системе.
- 3) d-элемент. Подтверждает его свойства как переходного металла.
- 4) Ошибка. Хром — активный металл (в безвоздушной среде), а не газ.
- 5) Ошибка. Хром — один из самых тугоплавких металлов ($1907^\circ C$).
- 6) Ошибка. Хром находится в группе металлов, а не типичных неметаллов.
Часто задаваемые вопросы:
Хром расположен в 4-м периоде, 6-й группе. Его порядковый номер — 24.
У хрома 4 энергетических уровня.
Электронная схема: 2, 8, 13, 1.
Хром является d-элементом семейства переходных металлов.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.