Теория:
Галлий (Ga) в периодической системе: 4‑й период, 13‑я группа (по устаревшей классификации — III A), атомная масса 69,723 а.е.м.
Занимает положение в 4‑м периоде, что определяет его принадлежность к главным подгруппам (p-элементам).
Галлий — уникальный металл, существование которого было предсказано Д. И. Менделеевым под названием «экаалюминий» еще до его официального открытия.
Будучи химическим аналогом алюминия и индия, он располагается в правой части таблицы Менделеева, сразу после переходных металлов.
Нахождение Галлия в 13‑й группе и наличие трех электронов на внешнем слое обуславливают его ключевые параметры:
Характерную степень окисления +3.
А также уникальное физическое свойство — аномально низкую температуру плавления (29,76°C), что позволяет ему становиться жидким от тепла человеческих рук.
Структура атома подтверждается его электронной формулой (конфигурацией):
[Ar] 3d10 4s2 4p1.
На которой наглядно можно определить его положение как p-блочного элемента, у которого начинает заполняться 4p-подуровень.
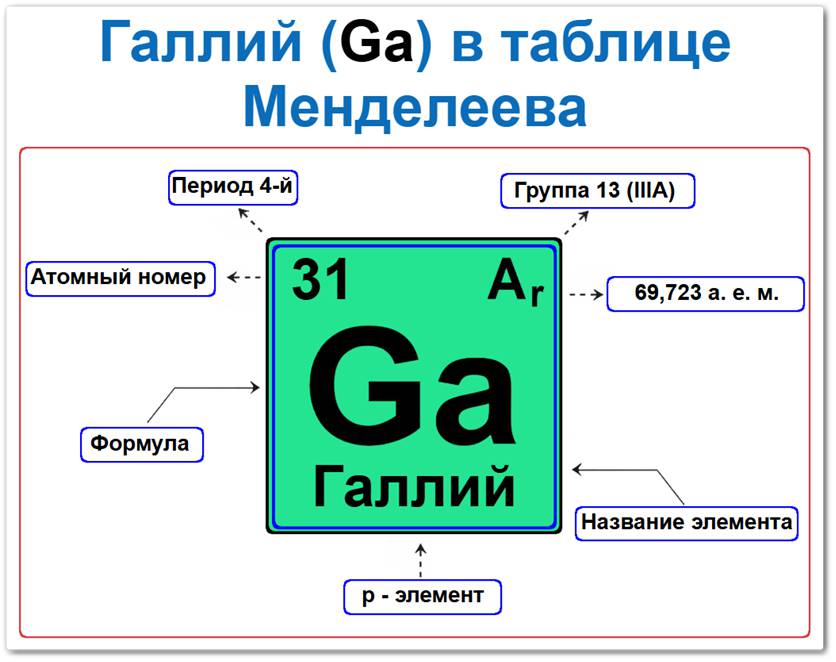
Галлий элемент таблицы Менделеева который можно определить на основании закона периодичности: положение в ряду металлов период 4, группа 13, а также по его порядковому номеру (Z = 31).
Содержание страницы
- 1. Как определить положение Галлия в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 31)
- 3. Название и символ
- 4. Группа (13 / III A)
- 5. Период (4‑й)
- 6. Относительная атомная масса (Ar)
- 7. p‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Галлия по Таблице Менделеева
- 9. Проверка знаний: Как определить галлий по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Галлия в Таблице Менделеева
Локация галлия в таблице описывается характеристиками его атомного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (13-я группа, подгруппа алюминия).
- Период (горизонтальный ряд).
- Электронное семейство (галлий — p‑элемент).
Порядковый номер / атомный номер (Z = 31)
- Служит уникальным кодом элемента в системе.
- В ядре — 31 протон; в нейтральной оболочке — 31 электрон.
- Электронное строение: [Ar] 3d10 4s2 4p1.
Важно: Галлий обладает одной из самых широких температурных областей существования в жидком состоянии. Он закипает только при 2204°C, что делает его незаменимым для высокотемпературных термометров.
Название и символ
- Название: «галлий» (от лат. «Gallia» — Франция, в честь родины первооткрывателя Поля Эмиля Лекока де Буабодрана).
- Символ: Ga.
- Примечание: Открыт в 1875 году. В чистом виде — мягкий серебристо-белый металл, способный смачивать поверхность стекла.
Группа (13 / III A)
Расположен в 13‑й группе. В периодической системе галлий находится в одной вертикальной колонке с алюминием (сверху) и индием (снизу) и входит в подгруппа бора.
Химический потенциал:
- Валентность галлия: постоянная валентность III (иногда проявляет I).
- Степень окисления: +3. Соединения галлия (арсенид галлия) являются ключевыми материалами современной полупроводниковой электроники.
Период (4‑й)
Находится в 4‑м периоде — его электроны распределены по четырем энергетическим уровням.
Влияние на свойства:
- Химическая активность: Галлий — амфотерный элемент, он способен реагировать как с кислотами, так и со щелочами.
- Техническое значение: Используется в лазерах, светодиодах (LED) и солнечных батареях.
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
Относительная атомная масса (Ar)
- Ar(Ga) ≈ 69,723 а.е.м.
- Определение: среднее значение массы природных изотопов, которых у галлия два (стабильные 69 и 71).
Все значения для всех элементов можно узнать в таблице атомных масс.
p‑Элемент (электронное семейство)
Валентные электроны располагаются на 4s и 4p подуровнях (4s2 4p1).
Специфика блока: Как p-элемент, галлий проявляет выраженные металлические свойства, но с элементами амфотерности, сближающими его с неметаллами по характеру некоторых оксидов.
Определение энергетических уровней Галлия по Таблице Менделеева
Положение Галлия (Ga) в системе Менделеева — это готовый «паспорт» его внутреннего устройства.
1. 4-й период (Количество этажей)
Номер периода определяет число электронных слоев.
- Итог: У Галлия 4 энергетических уровня.
2. Список «жильцов» (Распределение электронов)
Атомный номер Галлия — 31. Его 31 электрон распределен по уровням следующим образом:
Ga ) 2 ) 8 ) 18 ) 3
3. 13-я группа (Химический характер)
Галлий — элемент главной подгруппы III группы (или 13-й группы).
- p-элемент: Относится к типичным металлам главных подгрупп.
- Физические свойства: Легкоплавкий металл, склонен к сильному переохлаждению (может оставаться жидким при 0°C).
Проверка знаний: Как определить галлий по таблице Менделеева
Выберите три верных тезиса, которые однозначно характеризуют Галлий (Ga) в структуре таблицы.
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3
- 1) Номер 31. Соответствует количеству протонов в ядре.
- 2) 4-й период, 13-я группа. Его адрес в периодической системе.
- 3) p-элемент. Характеризуется наличием 1 электрона на p-подуровне.
- 4) Ошибка. Галлий очень мягкий и плавится даже в руках.
- 5) Ошибка. Галлий в группе алюминия (13), кислород — в 16-й.
- 6) Ошибка. Галлий — это металл, а не газ.
Часто задаваемые вопросы:
Галлий расположен в 4-м периоде, 13-й группе. Его порядковый номер — 31.
Это связано с его кристаллической структурой и низкой температурой плавления (всего 29,76°C), что ниже температуры человеческого тела.
У галлия 4 энергетических уровня. Схема распределения: 2, 8, 18, 3.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.