Кристаллическая решетка представляет собой вспомогательный геометрический образ, который используется для анализа структуры кристалла.
Решетка напоминает сетку или канву, что позволяет называть точки решетки узлами. Вся решетка состоит из точек, которые образуются из произвольно выбранной точки кристалла при применении группы трансляции.
Важно то, что все остальные точки находятся относительно каждой точки совершенно одинаково.
Применение любой трансляции к решетке приводит к ее параллельному перемещению и совпадению.
Для удобства анализа обычно точки решетки совмещают с центрами атомов, входящих в кристалл, или с элементами симметрии.
Содержание страницы
Кристаллические решетки: структура и классификация
Кристаллические решетки классифицируют по типу частиц, образующих правильную структуру твердого тела.
Если в узлах решетки находятся ионы, связанные между собой прочными кулоновскими силами, ее называют ионной.
Атомы, соединенные при помощи ковалентных связей, образуют атомную кристаллическую решетку.
Молекулярная решетка состоит из отдельных молекул, связанных между собой слабыми силами Ван-дер-Ваальса.
И наконец, если в узлах кристаллической решетки расположены нейтральные атомы и катионы металлов, окруженные «свободными» электронами, то говорят о металлической решетке.
Ионные кристаллические решетки

Энергетически наиболее выгодно, чтобы каждый ион был окружен наибольшим числом ионов противоположного знака.
Рис. кристаллическая решетка хлорида натрия
Но одноименно заряженные ионы отталкиваются, поэтому устойчивыми будут только такие кристаллические решетки, для которых выполняются следующие два условия:
- Разноименные ионы максимально сближены.
- Одинаково заряженные ионы максимально удалены друг от друга.
Радиусы ионов играют основную роль при образовании тех или иных кристаллических форм.
Так, если отношение радиуса катиона (rк) к радиусу аниона (rа) превышает 0,73, геометрически легко показать, что каждый ион может быть окружен восемью ионами противоположного знака.
При чк : ча = 0,41 ÷ 0,73 наблюдается октаэдрическая координация: вокруг каждого иона располагаются шесть противоположно заряженных ионов.
И наконец, при чк : ча < 0,41 окружение составляют только четыре иона. В таблице 1 приведены численные значения радиусов ионов некоторых щелочных металлов и галогенов.
В случае хлорида натрия отношение чк : ча равно 0,52, поэтому катион Na+ в кристалле NaCl окружен шестью ионами хлора, а каждый анион Сl—— шестью ионами натрия.
За счет равномерного распределения электронной плотности в пространстве все шесть связей оказываются совершенно равноценными.
В кристалле хлорида натрия нельзя выделить отдельных ионных молекул Na+Cl—; его необходимо рассматривать как гигантскую макромолекулу, построенную из равного числа катионов Na+ и анионов Сl— (рис.).
Таблица ионных радиусов галогенов и щелочных металлов
| Катион | Радиус, нм | Анион | Радиус, нм |
| Li+ | 0,078 | F— | 0,133 |
| Na+ | 0,095 | Сl— | 0,181 |
| К+ | 0,133 | Вr— | 0,196 |
| Cs+ | 0,165 | I— | 0,220 |
Для хлорида цезия отношение чк : ча равно 0,91. Восемь катионов Cs+ занимают вершины куба, в центре которого находится ион хлора.

Рис.2. Структура алмаза
Ионные кристаллы, как правило, легко растворяются в жидкостях, состоящих из полярных молекул, например, в воде.
Расположенные на поверхности ионы окружаются молекулами растворителя, отрываются от кристалла и переходят в раствор.
Для одного и того же ионного соединения растворимость возрастает с увеличением взаимодействия между молекулами растворителя и соответствующими ионами кристалла, т. е. с увеличением полярности растворителя (таблице 2).
Таблица 2 растворимости кристаллических ионных соединений в различных полярных растворителях
(температура 25°С; растворимость выражена в граммах растворенного вещества на 100 г растворителя; е — диэлектрическая проницаемость)
| Соединение | Растворимость в спиртах | ||
| метиловом (ε = 33) | этиловом (ε= 24) | пропиловом (ε= 20) | |
| KI | 90 | 46 | 28 |
| NaCl | 0,53 | 0,02 | 0,00 |
| Sr(NO3)2 | 1,26 | 0,02 | — |
Атомные кристаллические решетки
Атомные кристаллические решетки сформированы за счет ковалентных связей. Взаимная ориентация атомов определяется пространственным строением их электронных подуровней.
Например, каждый атом углерода может образовать четыре ковалентные связи, направленные из центра правильного тетраэдра к его вершинам.
С этим центральным атомом соединяются четыре атома углерода, находящихся в том же валентном состоянии.
У каждого из этих атомов остается по три неспаренных электрона, занимающих три гибридных sр3-подуровня, поэтому они образуют связи с тремя другими атомами углерода.
Так строится трехмерная кристаллическая решетка алмаза (рис. 2). Чтобы такой кристалл расплавился, необходимо разорвать большую часть ковалентных углерод-углеродных связей, обладающих высокой энергией.
Поэтому алмаз плавится при очень высокой температуре (>3500°С) и его невозможно растворить в какой либо жидкости.
Атомные кристаллы с ковалентными связями являются в большинстве случаев изоляторами, поскольку в них отсутствует как ионная , так и электронная проводимость.
Молекулярные кристаллические решетки
В узлах молекулярной кристаллической решетки находятся молекулы, связанные между собой силами Ван-дер-Ваальса. Такие решетки образуют водород, хлор, азот, оксид углерода (IV) и многие органические соедини.
Вследствие небольшой энергии взаимодействия частиц молекулярные кристаллы плавятся при низких температурах и легко растворяются в различных жидкостях.
Молекулы, имеющие разветвленное строение, образует более компактную кристаллическую структуру.
Силы взаимодействия между ними оказываются при этом гораздо выше, чем для не разветвленных молекул.
Поэтому соединения с близкой молекулярной массой, но неодинаковым строением имеют различные температуры плавления (например, гептан и 2, 2, 3-триметилбутан).
Взаимодействие между молекулами усиливается также с усложнением строения их электронных оболочек и увеличением полярности.
Температуры плавления полярных веществ существенно выше температур плавления неполярных соединений.
От полярности молекул сильно зависит растворимость молекулярных кристаллов.
Большое значение при этом играет соотношение между размерами полярной и неполярной части молекул.
Например, уксусная кислота Н3С—СООН смешивается с водой в любых отношениях, в то время как растворимость стеариновой кислоты составляет при 25°С всего лишь 0,03 г на 100 г Н2О.
Кристаллическая решетка льда
Для соединений, молекулы которых имеют полярные группы О—Н, N—Н, S—Н, структура кристаллов определяется в основном энергией водородных связей и характером их расположения в пространстве.
Наличием большого числа водородных связей:
объясняется, в частности, своеобразная структура льда.
Поскольку каждая молекула воды имеет два атома водорода и две не поделенные пары электронов, она может образовать четыре водородные связи:

В изолированной молекуле воды расстояние между ядрами атомов водорода и кислорода составляет примерно 0, 096 нм, а угол между направлениями связей О — Н равен 105°.
В твердом и жидком состояниях параметры молекул Н2О незначительно изменяются.
В кристаллической решетке льда вследствие образования водородных связей угол НОН приближается к тетраэдрическому (109,5°), а расстояние между ядрами атомов водорода и кислорода увеличивается до 0,099 нм.
Кристаллы льда принадлежат к гексагональной системе.
Каждая молекула воды связана водородными связями с четырьмя другими молекулами.
Вследствие относительно большой длины этих связей упаковка молекул Н2О оказывается очень неплотной, в структуре льда на каждые 46 молекул воды приходится шесть пустот диаметром 0,59 нм и две пустоты диаметром 0,52 нм.
Клатратные соединения
За счет включения в полости кристалла молекул хлора, аргона, ксенона и некоторых других газов возникают так называемые клатратные соединения или соединения включения.
Их образование с последующим разрушением применяется для разделения углеводородов и некоторых других веществ.
Клатраты используют также как удобную форму хранения газов.
Если внедряющиеся молекулы газа сравнительно невелики (Аr, Хе, СН4, СO2), то они занимают все восемь пустот.
Образующиеся при этом клатраты имеют состав:
X • 5,75 Н2О (8 : 46 = 1 : 5,75).
Более крупные частицы занимает только шесть пустот.
Предельное отношение числа внедренных молекул к числу молекул воды составляет в этом случае:
6 : 46 = 1 : 7,67.
Например, при охлаждении хлорной воды выпадают кристаллы гидрата хлора, имеющие состав Сl2 • 8Н2O.
При атмосферном давлении лед плавится при 0°С.
С точки зрения молекулярно-кинетической теории плавление льда происходит при такой температуре, когда энергия теплового движения молекул оказывается достаточной для разрыва большинства водородных связей.
Тетраэдрическая структура льда разрушается, и вода переходит в жидкое состояние.
В жидкой воде существует подвижное равновесие: действие водородных связей воссоздает в каждый момент времени в каждом элементе объема тетраэдрическую структуру льда, а тепловое движение молекул эту структуру разрушает.
Плавление льда сопровождается поглощением тепловой энергии в количестве 6,01 кдж/моль. Большая часть ее расходуется на разрыв водородных связей.
Решетка металлов
Следовательно, связь атомов металла в кристаллической решетке имеет иную природу, чем ионная или ковалентная.
С точки зрения современных представлений металл — это сложная система, состоящая из нейтральных атомов и положительно заряженных ионов, занимающих узлы кристаллической решетки, и «электронного газа», заполняющего межатомное пространство.
В одних местах кристалла катионы захватывают электроны из окружающего пространства, превращаясь в нейтральные атомы, в других — атомы металла отдают свои валентные электроны и превращаются в катионы.
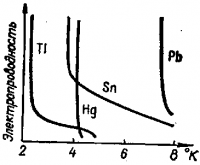
Рис. 5 . Изменение электропроводности металлов вблизи абсолютного нуля
Наличие «свободных» электронов в кристаллической решетке металла было подтверждено экспериментально опытами советских ученых Л. И. Мандельштама и Н. Д. Папалекси.
Которые наблюдали появление электрического тока при резком торможении вращающегося с большой скоростью куска металла.
Ток возникает также при резком ускорении движения металлического тела (эффект Толмена).
В последнем случае свободные электроны отбрасываются по инерции к противоположному по движению концу металла.
Электропроводность металлов
Одним из важнейших свойств металлов является их электропроводность. При одной и той же температуре одни металлы проводят электрический ток очень хорошо, другие — плохо.
Величина электропроводности зависит от общего числа валентных электронов в атоме, степени заполнения отдельных энергетических подуровней и от типа кристаллической решетки:
Таблица относительное значение электропроводности некоторых металлов
| Ag 59,0 | Na 20,8 | К 13,6 | Pt 9,7 | Be 5,2 | V 3,7 |
| Cu 56,9 | Ir 20,6 | Cd 12,6 | Pd 8,7 | Cr 5,1 | Hf 3,2 |
| Au 39,6 | Mo 20,0 | Ru 12,4 | Sn 8,3 | Cs 4,8 | Zr 2,3 |
| Al 36,1 | W 17,5 | Li 11,2 | Rb 7,7 | Nb 4,8 | Ti 2,2 |
| Ca 1,9 | Zn 16,0 | In 10,6 | Tl 6,3 | Pb 4,6 | Ba 1,9 |
| Rh 21,9 | Co 15,3 | Os 10,1 | Та 6,2 | Re 4,5 | Ce 1,2 |
| Mg 21,8 | Ni 13,9 | Fe 9,8 | Th 5,3 | Sr 4,2 | Hg 1,0 |
Для всех металлов характерно более или менее быстрое понижение электропроводности с увеличением температуры.
Это объясняется усилением колебательного движения катионов и нейтральных атомов в узлах кристаллической решетки, что приводит к замедлению направленного перемещения свободных электронов под действием внешнего электрического поля.
Очень интересным оказывается поведение металлов при низких температурах — вблизи абсолютного нуля (-273,16°С).
Последовательно увеличиваясь с понижением температуры, электропроводность некоторых металлов, например свинца, олова, ртути, неожиданно возрастает практически до бесконечности (рис. 5).
Это явление получило название сверхпроводимости. Оно характерно также для ряда сплавов и соединений металлов: карбидов, нитридов и т. д.
Быстрые ответы?
В зависимости от природы частиц, расположенных в узлах, и характера связи между ними различают четыре типа кристаллических решёток:
1. Ионную.
2. Металлическую.
3. Атомную.
4. Молекулярную.
1. Молекулярная — молекулы.
2. Атомная — атомы.
3. Ионная — ионы.
4. Металлическая — атом-ионы.
Вспомогательный геометрический образ, похожий на сетку, в узлах которой могут находиться атомы, молекулы или ионы.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.