Содержание страницы
Производство алюминия в промышленных масштабах
[toc wrapping=»right»]

Получение происходит в несколько этапов: добыча, обогащение минералов, в зависимости от метода получения алюминия используют разные методы переработки.
В лабораторных условиях алюминий получают восстановлением хлорид алюминия металлическим калием.
Алюминий — самый распространенный металл в природе. Он входит в состав глин, полевых шпатов, слюд и многих других минералов. Общее содержание алюминия в земной коре составляет 8,8 вес.% (по данным А. П. Виноградова).
Впервые он был получен Веллером в 1827 г. действием металлического калия на хлорид алюминия. Затем до конца 80 годов XIX в. алюминий получали путем вытеснения металлическим натрием из расплавленной соли АlСl3 • NaCl. Себестоимость алюминия была высокой. С открытием электролитического способа получения алюминия (1886 г.) Эру (Франция) и Холлом (США) производство его стало быстро возрастать, а стоимость уменьшаться. В настоящее время алюминий получают в миллионах тонн в год электролизом раствора окиси алюминия в расплавленном криолите.
Электролитический способ получения алюминия принципиально сохранился до настоящего времени. Однако его техническое оформление значительно изменилось, как и производство чистой окиси алюминия, криолита и угольных материалов. Развитие техники производства алюминия сопровождалось обширным изучением теории процессов.
Термические методы получения алюминия, утратившие значение в конце XIX в., вновь возродились за последние годы, главным образом для производства сплавов алюминия с кремнием.
Большое значение в развитии производства алюминия имели работы русских и советских ученых. В 90 годах XIX в., русский химик К. И. Байер впервые разработал щелочной способ производства чистой окиси алюминия из бокситов, получивший мировое признание. Затем А. А. Яковкиным, И. С. Лилеевым и другими были разработаны способы переработки высококремнистых бокситов на глинозем спеканием боксита с содой и известняком. В 1915 г. А. Н. Кузнецов и Е. И. Жуковский предложили электротермический способ извлечения глинозема из низкосортных алюминиевых руд через алюминаты щелочноземельных металлов.
Значительные успехи в последние годы были достигнуты по разработке комплексного передела нефелинов на окись алюминия, поташ, соду и цемент.
Теория электролитического способа получения алюминия впервые была разработана в начале XX в. П. П. Федотьевым.
В 1929 г. на ленинградском заводе «Красный выборжец» руководством П. П. Федотьева Н. П. Федотьевым были впервые в бывшем СССР проведены полузаводские опыты по получению алюминия из отечественного сырья.
В 1930 г. был пущен Ленинградский опытный алюминиевый завод, в 1932 г. — Волховский, в 1933 г. — Днепровский, а в последующие годы — еще ряд новых алюминиевых заводов. В создании их крупную роль сыграли П. П. Федотьев, П. Ф. Антипин, Ю. В. Баймаков, В. П. Машовец, В. М. Гуськов, Г. А. Абрамов, А. И. Беляев и сотрудники различных институтов, главным образом ВАМИ и Гипроалюминия.
Свойства применение алюминия
Алюминий представляет собой легкий металл плотностью 2,7 г/см3, плавящийся при 659° С, с температурой кипения около 2500° С. При обычной температуре алюминий не изменяется на воздухе, так как быстро покрывается тонким плотным слоем окиси, предохраняющей металл от дальнейшего окисления. Разбавленные соляная и серная кислоты легко растворяют алюминий, особенно при нагревании. Легко растворяется алюминий в щелочах, образуя алюминаты. Холодная азотная кислота пассивирует алюминий.
В виде порошка или тонкой алюминиевой фольги алюминий может при сильном нагревании воспламеняться и сгорает ярким пламенем с большим выделением тепла. Последнее свойство алюминия используется для приготовления некоторых взрывчатых смесей и при термитной сварке рельсов и балок.
Металлический алюминий легко вытягивается в проволоку и прокатывается в тонкие листы.
Алюминий используют в авиа- и автопромышленности, где его применяют в виде сплавов, имеющих высокие механические свойства. Например, прочность на разрыв литого алюминия 9— 12 кгс/мм2, прокатанного 18—28 кгс/мм2, а некоторых сплавов алюминия после термической обработки доходит до 45 кгс/мм2, т. е. достигает прочности углеродистой стали, при небольшой плотности — около 3 г/см3.
Количество легких сплавов на основе алюминия весьма обширно. Как правило, в них содержится до 95% Аl и остальное — присадки Сu, Mn, Mg, Ni, Ti и других металлов. Это прокатные сплавы. К литейным сплавам на основе алюминия относятся силумин (87% Аl и 13% Si), а также сплавы Аl с Zn, Сu и др. Кроме того, многие сплавы на магниевой или медной основе также содержат добавки алюминия.
Одним из ценных свойств алюминия является его высокая электропроводность, равная 60% проводимости чистой меди. А так как алюминий в 3 с лишним раза легче меди, то одинаковую с медью электропроводность будут иметь алюминиевые шины и провода, будучи в 2 раза легче медных.
Широкое применение получил алюминий в химической промышленности для изготовления различных сосудов и аппаратуры для хранения и производства органических кислот, спиртов, жиров, масел и других веществ, в пищевой промышленности — для изготовления аппаратуры и фольги. Из алюминия изготовляют также мебель, посуду, краску и т. д. Алюминий используют в строительстве, при изготовлении различных приборов, а также в качестве восстановителя и модификатора в металлургии.
Получение сырья для производства алюминия
Исходное сырье. Из многочисленных минералов, содержащих алюминий, исходным сырьем для получения алюминия или его сплавов с кремнием являются бокситы, нефелины, алуниты и каолины. Основной промышленной рудой для получения окиси алюминия служит боксит. В последнее время начали перерабатывать на глинозем также нефелины и алуниты.
Бокситы содержат в основном 50—60% Аl2O3, 1 —15% SiO2, 2—25% Fe2O3, 2—4% TiO2,10—30% Н2O. Возможны примеси окислов других элементов.
Нефелин отвечает формуле 3Na2O • К2O • Аl2O3 • 9SiO2. Богатейшие запасы нефелина имеются на Кольском полуострове в виде апатито-нефелиновых пород. Последние, после флотационного обогащения для выделения апатитовой фракции, дают хвосты, содержащие до 95% нефелина, идущего для комплексной переработки на глинозем, поташ, соду и цемент.
Алунитам отвечает формула K2SO4• Al2(SO4)3• 4Аl(ОН)3. Они встречаются в СНГ, а также в США, Италии, Австралии и Корее.
Каолины, которые содержат до 40% Аl2O3, могут быть использованы для получения глинозема. Однако вследствие высокого содержания SiO2 из каолинов выгоднее получать сплавы алюминия с кремнием.
Производство глинозема
К одной из наиболее ответственных стадий получения алюминия электролитическим путем относится производство чистой окиси алюминия. Основные компоненты, сопутствующие алюминию в рудах: Fe, Si, Ti — более электроположительны, чем алюминий, и при электролизе будут переходить в последний, загрязняя и ухудшая его физико-химические и механические свойства.
Из различных предложенных в свое время способов получения чистой окиси алюминия можно выделить три группы: щелочные, кислотные и электротермические. Последние два способа практически не применяются.
Применительно к переработке бокситов наиболее широкое распространение получили способы первой группы; при обработке щелочью получают водорастворимый алюминат натрия NаАlO2, отделяемый нерастворимого остатка.
Разложением растворов алюмината выделяют гидроокись алюминия, которая при последующем прокаливании превращается в окись алюминия, а раствор возвращают на выщелачивание новых порций боксита. Впервые этот способ, как уже указывалось, предложил Байер. Сущность способа заключается в непосредственном выщелачивании глинозема щелочными растворами при 160—170° С и давлении 3—4 (и больше) ат с получением алюминатного раствора. Последний самопроизвольно разлагается в присутствии Аl(ОН)3 с выделением гидроокиси алюминия.
Боксит дробят и измельчают в растворе щелочи, пульпу подают в автоклавы и обрабатывают 40% раствором NaOH в течение 2—3 ч.
При этом, например, гидроокись алюминия, находящаяся в боксите, растворяется:
Al(OH)3 + NaOH → NaAlO2+2H2O
Кремнезем, имеющийся в боксите, также растворяется с образованием силиката натрия:
SiO2 + 2NaOH→ Na2SiO3 + H2O
Далее силикат натрия реагирует с алюминатом, образуя нерастворимый натриевый алюмосиликат, выпадающий в осадок:
2NaAlO2 + 2Na2SiO3 + 4Н2O → Na2O • Аl2O3 • 2SiO2 • 2Н2O + 4NaOH
Присутствие в боксите кремнезема неизбежно связано с потерей щелочи и понижением извлечения в раствор глинозема при выщелачивании. Поэтому способ Байера для бокситов с большим содержанием кремнезема (свыше 5—6% SiO2) применять нецелесообразно.
Пульпу после выщелачивания направляют в самоиспаритель, затем раствор разбавляют промывными водами и направляют в сгустители для отделения красного шлама, идущего после отмывки в отвал. Слив из сгустителей, представляющий собой раствор алюмината натрия и содержащий 120 г/л Аl2O3 и 135 г/л Na2O, подвергают гидролизу. Эта операция, называемая выкручиванием или декомпозицией, осуществляется при разбавлении растворов в специальных аппаратах-декомпозерах. Для ускорения процесса декомпозиции в раствор вводят в качестве затравки часть ранее полученной гидроокиси алюминия для создания первичных центров кристаллизации. Продолжительность процесса выкручивания составляет 75—90 ч. Полученная гидратная пульпа сгущается и разделяется в классификаторах на мелкую и крупную фракции. Первую используют в процессе выкручивания в качестве затравки, а крупные частицы гидроокиси алюминия тщательно промывают, фильтруют и подвергают кальцинации до полного обезвоживания во вращающихся трубчатых печах, нагреваемых до 1200° С. После этого охлажденный глинозем поступает на электролиз.
Раствор после отделения Аl(ОН)3 содержит до 140 г/л NaOH; его выпаривают и возвращают в автоклавы на выщелачивание.
При этом из раствора выпадают кристаллы соды, получившейся при взаимодействии едкого натра с карбонатами шихты и СО2 воздуха. Едкий натр регенерируют действием гашеной извести Са(ОН)2 и направляют на выщелачивание боксита.
Для получения 1 т Аl2O3 расходуют около 2,5 т боксита, до 200 кг NaOH и до 120 кг извести (на регенерацию щелочи).
При большом содержании в бокситах SiO2 для получения глинозема пользуются способом спекания или комбинированным щелочным способом.
Способ спекания, применительно к отечественному сырью, разработан в ГИПХ А. А. Яковкиным и И. С. Лилеевым.
Размолотый боксит тщательно смешивают с содой и известью и обжигают в трубчатых вращающихся печах при 1000—1200°С. Спекание приводит к образованию алюмината и феррита натрия и силиката кальция. При температуре около 700° С окислы алюминия и железа, находящиеся в боксите, реагируют с содой:
Al2O3 + Na2CO3 → Na2O + Аl2O3 + СO2 Fe2O3 + Na2CO3 → Na2O • Fe2O3 + CO2
при 900°С:
Na2O • Fe2O3 + Al2O3 → Na2O • Al2O3 + Fe2O3
Получается также алюмосиликат натрия Na2O • Аl2O3 • 2SiO2, но в присутствии извести большая часть его образует вновь алюминат натрия и двукальциевый силикат:
Na2O • Аl2O3 • 2SiO2 + 4СаО → Na2O • Аl2O3 +2 (2СаО • SiO2)
Таким образом, основными составляющими спека являются Na2O • Аl2O3, Na2O • Fe2O3 и 2СаО • SiO2. Для получения спека такого состава необходимо вводить в шихту 1 моль Na2CO3 на 1 моль Аl2O3, 1 моль соды на 1 моль Fe2O3 и 2 моль СаСО3 на 1 моль SiO2.
Двуокись титана и, частично, SiO2, образуют нерастворимые титанат и силикат кальция, а часть SiO2 дает растворимый силикат натрия. Полученный спек охлаждают, размалывают и выщелачивают водой. В раствор переходят алюминат и силикат натрия; феррит натрия разлагается и дает в осадке гидроокись железа. В воде не растворяются титанат и силикат кальция; с Fe(OH)3 они образуют красный шлам, идущий в отвал.
Отфильтрованный алюминатный раствор идет на обескремнивание с помощью известкового молока и нагревания в автоклавах под давлением 1,5—2,5 ат. Большая часть SiО2 переходит в осадок в виде алюмосиликата кальция и натрия. Этот осадок — белый шлам — отделяют и фильтрат алюмината натрия разлагают, в отличие от способа Байера, карбонизацией. В карбонизаторы, содержащие подогретый раствор алюмината, пропускают при перемешивании отходящие печные газы, содержащие СО2. Карбонизацию не доводят до конца, чтобы вместе с осаждающейся гидроокисью алюминия не выпадала SiО2 из имеющегося раствора силиката натрия.
Раствор соды фильтруют от Аl(ОН)3, выпаривают, и соду возвращают на спекание с новыми порциями боксита. Промытую Аl(ОН)3 прокаливают для получения Al2O3.
Описанный способ может быть применен к большому числу материалов, в частности к нефелинам. После отделения от апатита нефелиновые «хвосты» содержат до 45% SiO2, около 30% Аl2O3 и до 20% суммы окислов натрия и калия. Последнее обстоятельство позволяет отказаться от добавления соды в шихту для спекания. В этом случае шихта состоит только из нефелина и известняка. Измельченный известняк смешивают с нефелином и спекают в трубчатых печах так же, как поступали с бокситовыми рудами. Дальнейшая схема переработки спека мало отличается от схемы переработки бокситового спека.
Высокое содержание в нефелине окислов калия и натрия позволяет извлекать из растворов после осаждения глинозема поташ и соду, а известково-кремнистые шламы использовать как сырье для изготовления цемента.
Производство криолита
Для получения алюминия электролизом необходим криолит Na3AlF6. Криолит в природе встречается редко (Гренландия), поэтому для нужд алюминиевой промышленности его получают искусственно. Он должен быть свободен от примесей кремнезема и окиси железа, а также влаги и сульфатов. Общее содержание примесей не должно быть выше 4%. Основным сырьем для получения его является плавиковый шпат CaF2. Последний, обогащенный до содержания 95—96% CaF2 и размолотый, нагревают во вращающихся трубчатых печах с серной кислотой до 200° С, получая при этом гипс и фтористый водород:
CaF2 + H2SO4 → CaSO4+2HF
Содержащийся в плавиковом шпате кремнезем реагирует с HF с образованием газообразного SiF4:
SiO2+4HF → SiF4 + 2H2O; SiF4 + 2HF → H2SiF6
Поэтому наряду с плавиковой кислотой образуется кремнефтористоводородная кислота, для удаления которой в раствор вводят соду. При этом образуется труднорастворимый кремнефторид натрия Na2SiF6, выпадающий в осадок.
В очищенную таким образом плавиковую кислоту вводят гидроокись алюминия в количестве, необходимом для протекания реакции:
12HF + 2Al(OH)3 → 2H3AlF6 + 6H2O
Полученную «H3AlF6 нейтрализуют содой с получением криолита:
2H3AlF6 + 3Na2CO3 → 2Na3AlF6+3Н2O + 3СO2
Осадок криолита после фильтрации и сушки при температуре около 150° С является окончательным продуктом.
Для производства других солей, содержащих фтор, необходимых для корректировки электролита, плавиковую кислоту нейтрализуют либо гидроокисью алюминия (для получения AlF3), либо содой (для получения NaF).
Производство угольных материалов. На электролизерах с непрерывно самообжигающимся анодом в алюминиевый кожух анода загружают сырую анодную массу, которая за счет тепла, выделенного в ванне, спекается в монолитный угольный блок. Анодную массу готовят смешением размолотого нефтяного или пекового кокса с расплавленным пеком при температуре около 100° С. Количество пека, играющего роль связующего материала, составляет 28—32% общего веса массы. Хорошо перемешанную массу охлаждают в железных формах и передают в виде брикетов к электролизерам.
Анодная масса должна быть высокой чистоты; в ней может находиться только минимальное количество золь, содержащей окислы железа и кремния. Анодная масса делится на четыре сорта: нулевой сорт с содержанием золы не более 0,45%, первый — до 0,65%, второй — до 0,85% и третий, где золы не более 1,25%. Кроме чистоты, обожженная анодная масса должна быть достаточно механически прочной, малопористой (плотной), обладать высокой электропроводностью и стойкостью против окисления на воздухе.
Существенную роль играет также режим обжига, регулировать который можно главным образом за счет общей высоты анода при данной технологии подготовки брикетов и частоты загрузки их в алюминиевый кожух.
Угольную массу с меньшим содержанием связующего (около 25%) применяют для забивки швов между блоками при монтаже угольной подины ванны. Угольные блоки для пода и боковой футеровки электролизеров изготовляют на специальных электродных заводах. Шихту для блоков готовят из смеси прокаленного и размолотого антрацита с нефтяным коксом и 16—18% от веса массы пека, выполняющего роль связующего материала. Массу тщательно перемешивают на специальных смесительных машинах с подогревом до 100—110° С и прессуют либо на прошивных прессах, либо в глухую матрицу под давлением до 1000 кг/см2. Полученные блоки высушивают на воздухе и подвергают обжигу в кольцевых камерных печах, обогреваемых генераторным газом. Необходимо при этом строго выдерживать определенный режим обжига, который продолжается 18—20 суток без доступа воздуха при постепенном подъеме температуры до 1300—1400° С и медленном пониже металла. Здесь же указаны расходные коэффициенты сырья и электроэнергии и относительный удельный вес элементов затрат, составляющих себестоимость.
Переплавка и рафинирование алюминия
Из металлических примесей основную часть, в отдельных ваннах до 1,8%, составляют железо и кремний и много других металлов с общим количеством 0,01 —0,05 % .
К неметаллическим примесям относятся глинозем, фториды, углерод, карбид и нитрид алюминия. Основной газовой примесью является водород, который растворяется в расплавленном алюминии от 0,05 до 0,25 см3 на 100 г алюминия.
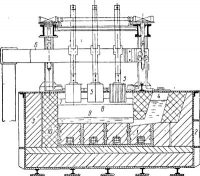
Рис. 2. Ванна для электролитического рафинирования алюминия:
1 — подина ванны; 2 —кожух; 3 — футеровка; 4 — загрузочный карман; 5—катод; 6 — катодная шина; 7 — рафинированный алюминий; 8 — электролит; 9 —анодный сплав; 10 — магнезитовая футеровка.
Для очистки алюминия от неметаллических примесей и газовых включений через расплавленный алюминий в ковше пропускают в течение 10—15 мин газообразный хлор из баллонов в специальной хлорной камере. Хлор взаимодействует с частью алюминия, образуя АlСl3, который выделяется из металла в виде паров. Пары АlСl3 адсорбируются взвешенными в металле частицами глинозема, фторидов и угля. Эти частицы всплывают вместе с АlСl3 на поверхность расплавленного металла в виде серого порошка и удаляются дырчатыми ложками. Водород удаляется из алюминия при этом с отходящими газами.
Очистить алюминий можно и при переплавке металла, которую производят в отражательных электрических печах сопротивления. Цель такой переплавки, кроме очистки от неметаллических примесей и газовых включений, получить путем смешения различных по качеству партий алюминия металл нужной марки и отлить в слитки нужной формы и размеров.
Нередко после хлорирования металлу дают отстояться и в жидком виде направляют для смешения и некоторой дополнительной рафинировки в отражательную печь сопротивления. Алюминий получается с содержанием его 99,5—99,7%. Для получения алюминия высокой чистоты (99,99%) Аl) металл подвергается дополнительному электролитическому рафинированию (рис. 2).
Промышленное применение получил трехслойный метод, в котором анодом служит загрязненный сплав, катодом — чистый рафинированный алюминий, а электролит, состоящий из расплавленной смеси 60% ВаСl2, 23% lIF3 и 17% NaF, расположен между ними. Для утяжеления анодного сплава к нему добавляют до 30% меди. При температуре электролиза, равной около 740—760°С, с отношение плотностей таково (в г/см3):анодный сплав около 3, электролит 2,7, а катодный алюминий 2,3.
Конструкция электролизера напоминает обычную многоанодную ванну для получения алюминия. Устройство подины аналогично устройству ее в алюминиевых ваннах с той разницей, что внутренняя боковая футеровка составлена не из угольных плит, а из магнезитового кирпича, что позволяет устранить утечку тока через футеровку. Для отвода тока от слоя рафинированного алюминия в него на 5—6 см погружены графитированные электроды, защищенные от окисления алюминиевыми кожухами.
Для загрузки алюминия, подлежащего рафинированию, в боковой футеровке сделан карман, футерованный магнезитовым кирпичом и сообщающийся с рабочим пространством ванны на уровне анодного сплава. Процесс рафинирования сводится к растворению из анодного сплава алюминия и более электроотрицательных примесей— натрия, кальция, магния и др. Более электроположительные примеси — кремний, медь, железо и другие — не растворяются и накапливаются до некоторой концентрации в анодном сплаве.
На катоде идет разряд практически только ионов алюминия. Другие электроотрицательные примеси накапливаются в электролите. Анодный сплав и электролит периодически заменяют новыми.
Выход по току достигает до 98%, а напряжение на ванне 6—7 в при электродной плотности тока около 0,5 а/см2.
Одним из возможных способов получения алюминия весьма высокой чистоты может быть дистилляция технического алюминия через его субсоединения (одновалентный алюминий), а также зонная перекристаллизация.
Статья на тему Производство алюминия

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.