Теория:
Степень окисления цезия во всех стабильных соединениях принимает значение +1. В свободном состоянии как простое вещество она равна 0.
Более высокие состояния (+2, +3 и +5) возможны лишь в теории при сверхвысоком давлении и в обычной химии не встречаются.
Например для высшей СО +1: в соединении CsCl (хлорид цезия) степень окисления металла равна +1.
Это происходит потому, что цезий находится в 1-й группе и обладает крайне низкой энергией ионизации.
При взаимодействии с любым неметаллом он мгновенно отдает свой единственный валентный электрон (6s1), достигая максимально устойчивой оболочки инертного газа ксенона.
Для сравнения, отрицательная СО -1: встречается в таких редких соединениях, как цезиды (например, в растворах с краун-эфирами).
Здесь ситуация специфическая: за счет мощного структурирования среды и использования лигандов, удерживающих катионы, свободный атом цезия может «принять» электрон на свою 6s-орбиталь, образуя анион Cs⁻.
Такие состояния крайне неустойчивы и существуют только в отсутствие малейших следов окислителей или воды, так как металл стремится вернуться к положительному заряду, который для него энергетически наиболее выгоден.
Промежуточные или более высокие степени окисления, такие как +2, являются «невозможными» в обычных условиях.
Обладая конфигурацией [Xe] 6s1, цезию предельно просто остановиться на форме +1.
Чтобы оторвать второй электрон, потребовалось бы разрушить заполненный и очень стабильный слой [Xe], что требует колоссальной энергии.
Именно поэтому химия цезия считается одной из самых предсказуемых — он практически всегда выступает как однозарядный катион.
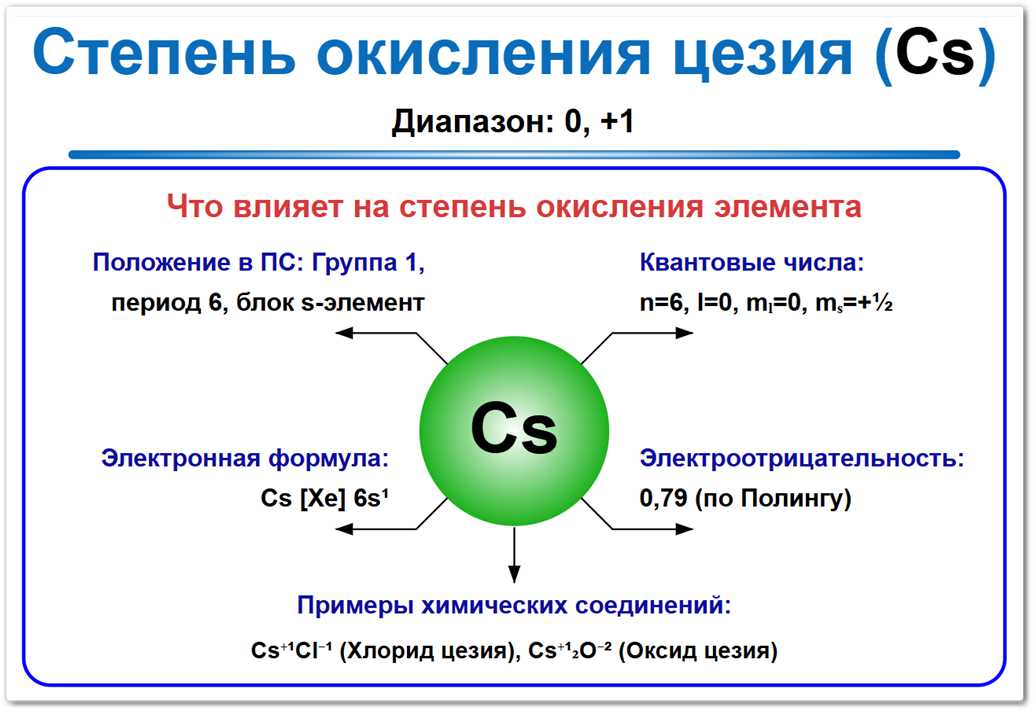
Рис. 1. Возможные степени окисления цезия: от -1 до +1. Самая устойчивая и единственно распространенная форма — +1 (соли, оксиды).
Обратите внимание, что химия цезия во многом схожа с химией франция (Fr), своего соседа по группе, однако цезий является самым активным из стабильных металлов. Его электроотрицательность составляет всего 0,79 по шкале Полинга.
На формирование его свойств влияют электронное строение (6s1), положение в 1-й группе и огромный атомный радиус.
Содержание страницы
- 1. Почему у цезия стабильная степень окисления?
- 2. Степень окисления цезия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления цезия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления цезия
- 6. Шпаргалка для цезия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у цезия стабильная степень окисления?
Причина стабильности состояния +1 заключается в достижении электронной конфигурации инертного газа ксенона при потере всего одного электрона. Эта структура энергетически совершенна и не склонна к дальнейшим изменениям.
- В простом веществе (Cs⁰): Заряд равен 0. Конфигурация:
6s [↑]. - В ионе (Cs+1): Цезий отдает 1 валентный электрон. Конфигурация:
[Xe].

Рис. 2. Процесс окисления цезия: от мягкого золотистого металла до стабильного катиона в составе солей.
Степень окисления цезия в соединениях
В подавляющем большинстве случаев цезий в соединениях проявляет степень окисления +1, однако вид соединения может быть разным:
- Сульфат цезия (Cs2SO4): Cs +1, S +6, O -2.
- Оксид цезия (Cs2O): Cs +1, O -2.
- Надперекись цезия (CsO2): Cs +1, O -0.5 (среднее).
- Гидрид цезия (CsH): Cs +1, H -1.
- Фторид цезия (CsF): Cs +1, F -1.
Высшая степень окисления
Высшая степень окисления цезия равна +1. Это значение полностью соответствует номеру группы (I) в периодической системе.
Хотя под сверхвысоким давлением ученым удалось зафиксировать признаки более высоких СО, в стандартной химии +1 — это предел.
Низшая степень окисления
Для цезия возможна степень окисления -1 в составе экзотических алкалидов, однако степень окисления цезия равна 0 в металлическом виде — это стандартное состояние для элемента как простого вещества.
Промежуточные степени окисления
Для цезия промежуточные степени окисления отсутствуют. Атом либо находится в нейтральном состоянии (0), либо полностью отдает свой валентный электрон (+1).
Важно: Цезий — самый химически активный металл. Он настолько стремится к степени окисления +1, что воспламеняется на воздухе и реагирует со льдом даже при температуре -116°C.
Почему степень окисления чаще положительная?
Знак заряда определяется природой щелочного металла:
- Положительная СО (+): Цезий имеет самый большой радиус и легче всех металлов отдает электрон.
- Нулевая СО (0): Характерна для чистого металла, который хранится в вакууме или аргоне.
- Отрицательная СО (-): Встречается в уникальных лабораторных условиях при «насильственном» добавлении электрона в пустую 6s-ячейку.
Как определить степень окисления цезия
По таблице Менделеева
- Семейство: s-элемент (щелочной металл).
- Валентные электроны: 1 (на 6s-подуровне).
- Атомная масса цезия: 133 а.е.м.
По валентности (Число связей)
В отличие от переходных металлов, валентность цезия постоянна и равна I.
- В хлориде (CsCl): Атом цезия связан с одним атомом хлора. Его валентность — I, а степень окисления равна +1.
- В гидроксиде (CsOH): Цезий связан с одной OH-группой. Валентность — I, СО цезия — +1.
По электронной конфигурации
- Электронная формула цезия: [Xe] 6s1.
- Атому цезия степени окисления +1 достичь максимально выгодно, так как это превращает его в структуру инертного газа.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для Cs2CO3 (карбонат цезия):
Сумма СО равна 0. Углерод +4, Кислород -2. Обозначим Cs как x.
2x + (+4) + 3 · (-2) = 0
2x + 4 — 6 = 0 ⇒ 2x = 2 ⇒ x = +1
Примеры степеней окисления цезия
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +1 | Единственная стабильная. Характерна для всех солей и щелочей. | CsCl, CsOH, CsNO3 |
| 0 | Металл. Химически крайне активное вещество. | Cs (жидкий или твердый металл) |
| -1 | Отрицательная. Обнаружена в криптат-комплексах. | [Cs(18-crown-6)]+Cs— |
Шпаргалка для цезия
- +1 — единственная степень, которую нужно запомнить для школьных и вузовских задач.
- Активность — в СО +1 цезий образует самую сильную щелочь среди всех нерадиоактивных элементов (CsOH).
- Изотопы — цезий-137 в СО +1 является опасным продуктом деления в ядерных реакторах.
Пример решения задачи:
▶️ Дано:
Соединение: Cs2O (оксид цезия).
⌕ Найти:
Определите СО цезия.
✨ Решение:
Кислород (O) обычно равен -2. Уравнение для двух атомов цезия: 2x + (-2) = 0 → 2x = 2 → x = +1.
✅ Ответ:
Cs(+1).
Проверка знаний
Показать ответы
Правильные ответы: 1, 3, 4, 5.
Разбор ошибок:
2 — неверно: цезий проявляет только +1. Состояния +2 и +3 не существуют в устойчивых химических соединениях.
Часто задаваемые вопросы
В обычной химии — нет. Только под экстремальным давлением в лабораториях были получены признаки участия внутренних электронов в связях.
Всегда +1. В таких веществах, как CsO2, меняется степень окисления кислорода, но не самого цезия.
Из-за огромного расстояния от ядра до единственного внешнего электрона, который удерживается очень слабо.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.