Теория:
Степень окисления стронция (Sr) в сложных соединениях всегда равна +2, это состояние является единственно устойчивым для элементов его группы.
Значения, отличные от 0 и +2, для стронция в обычных условиях не характерны.
Состояние +2 обусловлено легкой отдачей двух валентных электронов с внешнего s-слоя, после чего атом приобретает стабильную электронную конфигурацию благородного газа криптона.
Стронций находится во 2-й группе (главная подгруппа II группы) и является s-элементом 5-го периода.
Как s-элемент, он обладает электронной конфигурацией [Kr] 5s2. На внешнем уровне у стронция находятся два электрона, которые он легко теряет при химическом взаимодействии.
Стронций проявляет постоянную степень окисления +2 в соединениях.
Это связано с низкой энергией ионизации: атому энергетически выгодно полностью освободить 5s-подуровень. Предвнешний слой стронция при этом остается стабильным.
В отличие от магния или кальция, стронций химически более активен, что объясняется увеличением атомного радиуса и более слабым удержанием внешних электронов ядром.
Чтобы определить возможные значения, используют электронную формулу.
Например:
- Для стронция (1s22s22p63s23p63d104s24p65s2) — потеря двух внешних 5s-электронов дает устойчивую СО +2.
- Для рубидия (сосед слева, 5s1) — наличие только одного s-электрона ограничивает максимальную СО значением +1.
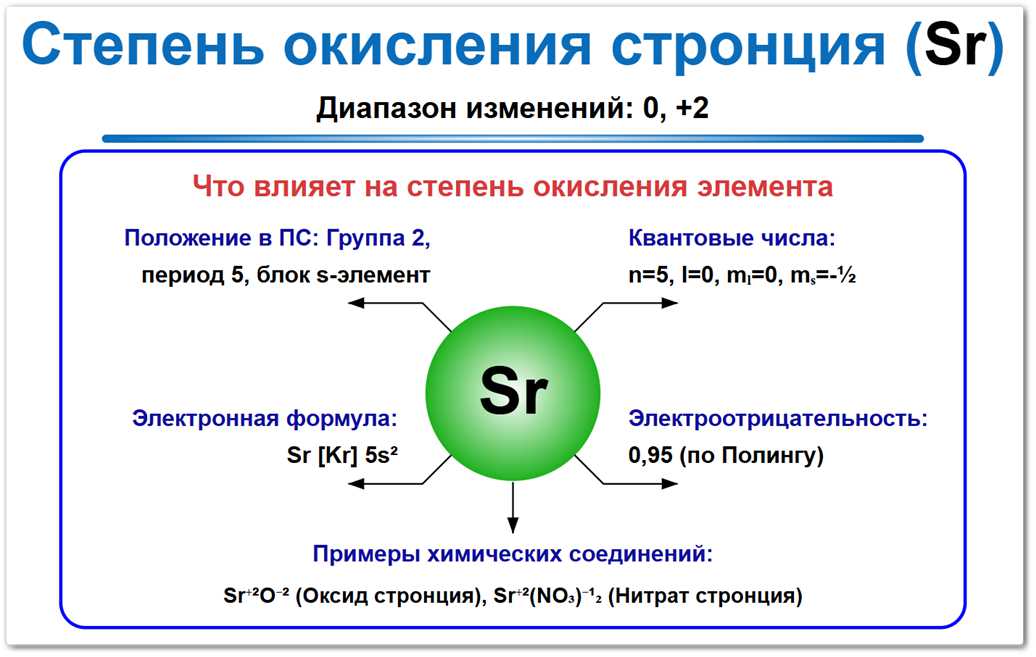
Рис. 1. Возможные степени окисления стронция: 0, +2. В отличие от переходных металлов, стронций не проявляет переменной валентности в водных растворах.
На их формирование влияют электронное строение (два 5s-электрона), положение во 2-й группе (щелочноземельные металлы) и низкое значение электроотрицательности 0,95 по шкале Полинга.
Содержание страницы
- 1. Почему у стронция стабильная степень окисления?
- 2. Степень окисления стронция в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 3. Почему степень окисления стронция всегда положительная?
- 4. Как определить степень окисления стронция
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления стронция
- 6. Шпаргалка для стронция
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у стронция стабильная степень окисления?
Причина стабильности стронция — завершенность электронной оболочки, которая образуется сразу после отдачи двух внешних электронов.
- В простом веществе (Sr⁰): Заряд равен 0. Конфигурация:
5s [↑↓]. - В ионе (Sr+2): Стронций отдает 2 электрона с 5s-уровня. Конфигурация:
5s [ ].

Рис. 2. Процесс окисления стронция: атом Sr ([Kr] 5s2) легко расстается с валентными электронами, превращаясь в стабильный двухзарядный катион.
Степень окисления стронция в соединениях
Соединения стронция типичны для сильных оснований и солей активных металлов:
- Оксид стронция (SrO): Sr +2, O -2.
- Гидроксид стронция (Sr(OH)2): Sr +2.
- Хлорид стронция (SrCl2): Sr +2, Cl -1.
- Карбонат стронция (SrCO3): Sr +2 (используется в пиротехнике для красного огня).
- Нитрат стронция (Sr(NO3)2): Sr +2.
Высшая степень окисления
Высшая степень окисления стронция равна +2. Она соответствует номеру его группы (IIА) в таблице Менделеева.
Низшая степень окисления
Низшая для металлов в свободном состоянии равна 0. Отрицательных степеней окисления стронций не проявляет из-за выраженных металлических свойств.
Важно: Стронций настолько активен, что в степени окисления 0 (чистый металл) он мгновенно окисляется на воздухе, покрываясь желтоватой оксидной пленкой.
Почему степень окисления стронция всегда положительная?
Знак заряда определяется крайне низкой электроотрицательностью (ЭО).
- Положительная СО (+): Стронций всегда выступает донором электронов, так как почти все элементы (кроме щелочных металлов) имеют более высокую ЭО.
- Отсутствие отрицательной СО: Атому стронция энергетически невозможно притянуть чужие электроны, так как его собственное ядро слабо удерживает даже свои внешние частицы.
- Нулевая СО (0): Встречается только в чистом металлическом стронции, который хранят под слоем керосина.
Как определить степень окисления стронция
По таблице Менделеева
- Семейство: s-элемент (щелочноземельные металлы).
- Валентные электроны: 2 (на 5s-уровне).
- Атомная масса стронция: 87,62 а.е.м. Для сравнения масс используй таблицу атомных масс.
- Типичная СО: +2.
По валентности (Число связей)
Валентность стронция всегда равна II.
- Валентность II: Соответствует СО +2.
- Пример: SrO. Здесь стронций образует две связи с кислородом.
По электронной конфигурации
- Электронная формула стронция: [Kr] 5s2. Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
- Наличие пары s-электронов на пятом энергетическом уровне предопределяет химическую стабильность иона Sr2+.
По химическому соединению (Алгебраический расчет)
Так как Стронций — активный металл 2-й группы, его степень окисления во всех солях и оксидах всегда +2.
Это упрощает расчет других элементов в сложных солях.
Пример для SrBr2 (бромид стронция):
Сумма всех СО в молекуле равна 0.
Обозначим СО стронция за x, а у брома (галоген) она равна -1.
1 · x + 2 · (-1) = 0
x — 2 = 0 ⇒ x = +2
Примеры степеней окисления стронция
| СО | Цвет пламени / Соединений | Примеры соединений (с индексами) |
|---|---|---|
| +2 | Белый (соли), карминово-красный (в пламени) | SrO, SrSO4, Sr(NO3)2 |
| 0 | Серебристо-белый металл | Sr (Стронций) |
Шпаргалка для стронция
- +2 — единственная степень окисления в любых химических реакциях.
- Красный огонь — ионы Sr2+ окрашивают пламя в характерный ярко-красный цвет.
- Аналог кальция — из-за одинаковой СО (+2) и схожего радиуса стронций может замещать кальций в костях.
- 0 — нестабильное состояние, металл быстро реагирует даже с водой.
Пример решения задачи:
▶️ Дано:
Соединение: Sr(OH)2.
⌕ Найти:
Определите СО стронция.
✨ Решение:
Группа OH всегда имеет суммарный заряд −1. Уравнение: x + 2 · (−1) = 0 → x = +2.
✅ Ответ:
Sr(+2).
Проверка знаний
Отметьте правильные утверждения для Стронция (Sr):
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: металлы 2-й группы не проявляют отрицательных степеней окисления.
Часто задаваемые вопросы
В стабильных химических соединениях — нет. Стронций всегда отдает оба валентных электрона, образуя устойчивый катион Sr2+.
Крайне нестабильные частицы с СО +1 могут существовать лишь доли секунды в газовой фазе при экстремальных температурах.
Химически ион стронция Sr2+ очень похож на ион кальция Ca2+. Организм «путает» их и встраивает радиоактивный изотоп стронция в костную ткань вместо кальция, что приводит к облучению изнутри.
Именно переход электронов в возбужденное состояние в ионе Sr2+ (СО +2) при нагревании заставляет пламя окрашиваться в карминово-красный цвет.
Это свойство широко используется в производстве фейерверков.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.