Теория:
Степень окисления иттрия (Y) в подавляющем большинстве устойчивых соединений равна +3, а также +2, +1 неустойчивые.
Значение 0 встречается только в простом веществе. В отличие от d-элементов середины таблицы, иттрий не проявляет переменной валентности в обычных условиях, что сближает его свойства с лантаноидами.
Иттрий находится в 3-й группе (побочная подгруппа III группы) и является d-элементом 5-го периода.
Как d-элемент, он обладает электронной конфигурацией [Kr] 4d15s2. На внешнем и предвнешнем уровнях у него всего три валентных электрона.
Иттрий проявляет постоянную степень окисления +3. Это связано с тем, что атом легко отдает все три валентных электрона (один 4d и два 5s) для достижения стабильной электронной конфигурации благородного газа криптона.
В отличие от скандия, иттрий имеет больший атомный радиус, что делает его более активным металлом, способным быстро окисляться на воздухе при нагревании.
Чтобы определить возможные значения, используют электронную формулу.
Например:
- Для иттрия (1s2…4p64d15s2) — потеря всех трех электронов (одного d и двух s) дает максимально устойчивую СО +3.
- Для германия (1s2…4s24p2) — наличие четырех электронов на внешнем p-слое позволяет варьировать степень окисления от -4 до +4.
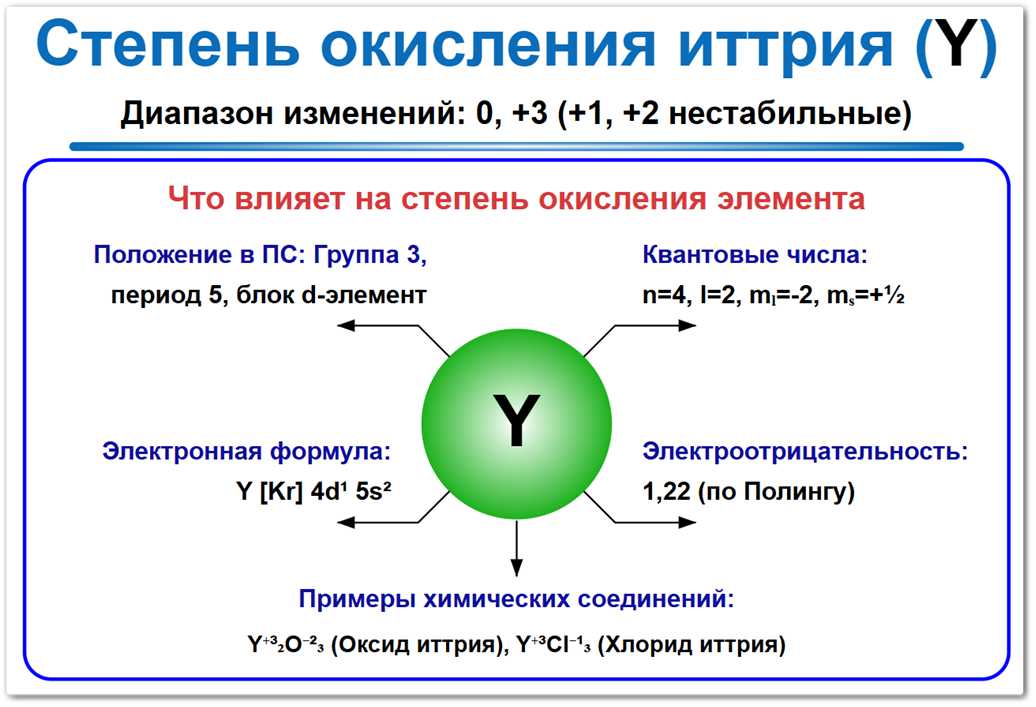
Рис. 1. Возможные степени окисления иттрия: 0, +3, а также +1, +2 нестабильные.
Обратите внимание, что в отличие от соседей по периоду, у иттрия практически не зафиксированы другие устойчивые заряды.
На их формирование влияют электронное строение (4d1 5s2), положение в начале d-блока и низкое значение электроотрицательности 1,22 по шкале Полинга.
Содержание страницы
- 1. Почему у иттрия стабильная степень окисления?
- 2. Степень окисления иттрия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления почти всегда положительная?
- 4. Как определить степень окисления иттрия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления иттрия
- 6. Шпаргалка для иттрия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у иттрия стабильная степень окисления?
Причина стабильности иттрия — энергетическая выгодность полной отдачи трех электронов. Удаление последующих электронов с глубоко лежащего 4p-слоя требует огромных затрат энергии.
- В простом веществе (Y⁰): Заряд равен 0. Конфигурация:
5s [↑↓] 4d [↑][ ][ ][ ][ ]. - В ионе (Y+3): Иттрий отдает 1 электрон с 4d и 2 электрона с 5s-уровня. Конфигурация:
5s [ ] 4d [ ][ ][ ][ ][ ].

Рис. 2. Процесс окисления иттрия: атом Y ([Kr] 4d1 5s2) теряет три электрона, приобретая конфигурацию инертного газа.
Степень окисления иттрия в соединениях
Все значимые соединения иттрия содержат его в форме катиона Y3+. Он проявляет типичные свойства активного металла:
- Оксид иттрия (Y2O3): Y +3, O -2.
- Хлорид иттрия (YCl3): Y +3, Cl -1.
- Нитрат иттрия (Y(NO3)3): Y +3.
- Фторид иттрия (YF3): Y +3, F -1.
- Гидрид иттрия (YH3): Y +3, H -1.
Высшая степень окисления
Высшая степень окисления иттрия равна +3. Она соответствует номеру его группы (III) в таблице Менделеева.
Низшая степень окисления
Понятие «низшая степень окисления» для металлов 3-й группы обычно ограничивается 0 (металлическое состояние), так как они не склонны принимать электроны.
Промежуточные степени окисления
Хотя для иттрия наиболее характерно состояние +3, в особых условиях (например, в кластерных соединениях или при сверхвысоких температурах) он может проявлять промежуточные степени окисления +1 и +2.
Эти состояния крайне неустойчивы и существуют преимущественно в виде твердых галогенидов (например, YI2 или YCl) или комплексных соединений.
Они являются сильнейшими восстановителями и легко окисляются до стабильного состояния +3 при малейшем контакте с окислителем или влагой.
Важно: Из-за стабильности СО +3 иттрий часто называют «редкоземельным элементом», хотя он не входит в семейство лантаноидов, но всегда сопутствует им в рудах.
Почему степень окисления почти всегда положительная?
Знак заряда зависит от низкой электроотрицательности (1,22).
- Положительная СО (+): Иттрий является сильным восстановителем. Он легко отдает электроны практически всем неметаллам.
- Отрицательная СО (-): Для иттрия не характерна, так как он не обладает сродством к электрону.
- Нулевая СО (0): Характерна для чистого металлического иттрия (светло-серый металл).
Как определить степень окисления иттрия
По таблице Менделеева
- Семейство: d-элемент (переходные металлы).
- Валентные электроны: 3 (2 на s-уровне и 1 на d-уровне).
- Атомная масса иттрия: 88,90 а.е.м. Для сравнения масс других элементов используй таблицу атомных масс.
По валентности (Число связей)
Валентность иттрия практически всегда равна III.
- Пример: В оксиде Y2O3 каждый атом иттрия образует три химические связи с кислородом.
По электронной конфигурации
- Электронная формула иттрия: [Kr] 4d1 5s2. Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
- Наличие трех внешних электронов за пределами заполненного слоя криптона предопределяет СО +3.
По химическому соединению (Алгебраический расчет)
Так как Иттрий — активный металл 3-й группы, его степень окисления в сложных веществах практически всегда +3.
Пример для YCl3 (хлорид иттрия):
Сумма всех СО в молекуле равна 0.
Обозначим СО иттрия за x, а у хлора она равна -1.
1 · x + 3 · (-1) = 0
x — 3 = 0 ⇒ x = +3
Примеры степеней окисления иттрия
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +3 | Высшая / Типичная. Максимально устойчивая форма. | Y2O3, YCl3, Y(NO3)3 |
| +2, +1 | Промежуточные. Нестабильны, встречаются в субгалогенидах. | YI2, YCl, Y2Cl3 |
| 0 | Низшая. Металлическое состояние иттрия. | Y (кристаллический металл) |
Шпаргалка для иттрия
- +3 — единственно важная степень окисления в химии.
- Сходство — по химическому поведению почти идентичен лантаноидам (особенно гадолинию).
- Оксид Y2O3 — используется в производстве люминофоров для экранов и сверхпроводников.
Пример решения задачи:
▶️ Дано:
Соединение: Y2(SO4)3.
⌕ Найти:
Определите СО иттрия.
✨ Решение:
Сульфат-ион (SO₄) имеет заряд −2. Уравнение: 2x + 3 · (−2) = 0 → 2x = 6 → x = +3.
✅ Ответ:
Y(+3).
Проверка знаний
Отметьте правильные утверждения для Иттрия (Y):
Показать ответы
Правильные ответы: 1, 2, 4.
Разбор ошибок:
3 — неверно: иттрий находится в 5-м периоде.
5 — неверно: иттрий проявляет преимущественно основные свойства.
Часто задаваемые вопросы
В обычных водных растворах и солях — нет. Однако в некоторых экзотических твердых соединениях (например, галогенидах типа YI2) могут наблюдаться нестабильные низшие состояния, но они не характерны для химии этого элемента.
Высшая степень окисления для Иттрия (Y) +3.Иттрий находится в 3-й группе, и его электронная конфигурация [Kr] 4d1 5s2 позволяет ему отдавать все 3 валентных электрона.
Нет отрицательной степени окисления по двум причинам:
Низкая электроотрицательность: Иттрий — типичный металл. Его электроотрицательность (1.22 по Полингу) слишком мала, чтобы притягивать чужие электроны. Ему гораздо «выгоднее» отдавать свои.
Электронная структура: Чтобы достроить внешний уровень до стабильного состояния (как у инертного газа Криптона), иттрию проще избавиться от 3 электронов (4d1 5s2), чем пытаться набрать огромное количество новых.
