Теория:
Степень окисления празеодима в большинстве соединений принимает значение +3, однако для этого элемента также характерно состояние +4, а в редких случаях и +2, +5.
Празеодим является одним из немногих лантаноидов, способных проявлять высокую степень окисления +4 в оксидах и фторидах, что отличает его от большинства «соседей» по семейству.
Например для высшей СО +5: в специфических условиях, таких как матричная изоляция при сверхнизких температурах, обнаружены следы соединений типа PrO2+, где степень окисления металла формально достигает +5.
Это происходит потому, что празеодим имеет конфигурацию (4f3 6s2) и при экстремальном воздействии сильных окислителей он способен задействовать не только внешние s-электроны, но и электроны с f-подуровня, стремясь достичь конфигурации инертного газа ксенона.
Для сравнения, редкая СО +2: встречается в таких галогенидах, как PrI2.
Здесь ситуация обратная: празеодим не отдает все валентные электроны, а сохраняет часть из них на d- или f-орбиталях.
Такие состояния крайне нестабильны и проявляют сильные восстановительные свойства, стремясь вернуться к заряду +3.
Такие состояния крайне нестабильны на воздухе и в воде, так как металл мгновенно окисляется до более стабильных положительных зарядов.
Промежуточные же степени окисления, такие как в оксиде Pr6O11, являются результатом сосуществования атомов в разных состояниях.
Обладая конфигурацией [Xe] 4f3 6s2, празеодиму наиболее энергетически выгодно находиться в форме +3, которая характерна для всей группы лантаноидов.
Именно поэтому соединения празеодима(IV) являются сильными окислителями — они стремятся захватить недостающий электрон, чтобы перейти в устойчивое состояние +3.
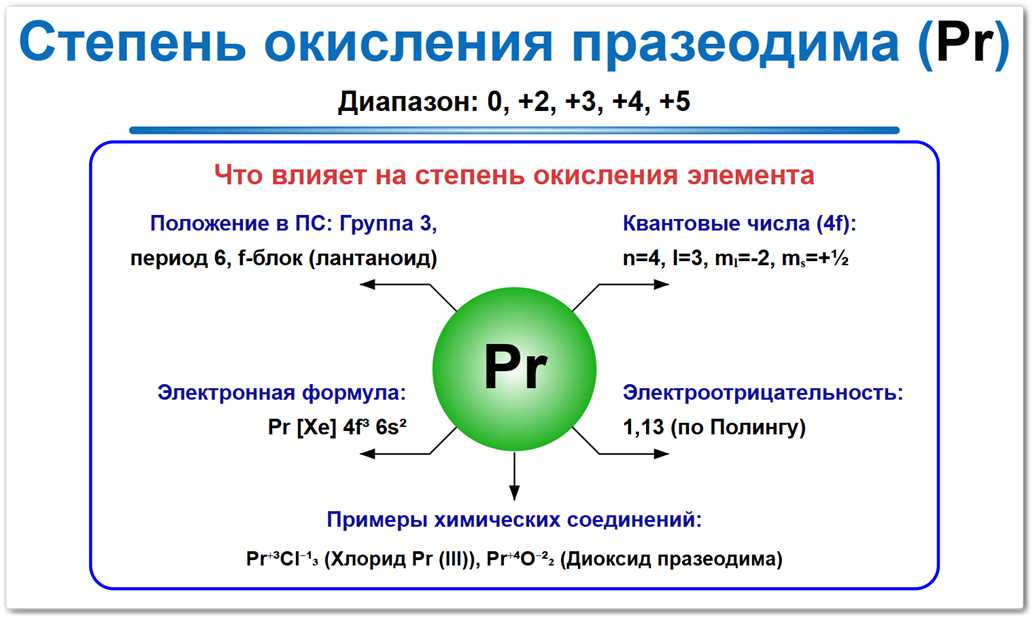
Рис. 1. Возможные степени окисления празеодима: 0 — сам химический элемент, +2, +3, +4 и +5 крайне не стабильная.
Самая устойчивая форма — +3 (зеленые соли), а наиболее известная высокозарядная форма — +4 (в составе темных оксидов).
Обратите внимание, что химия празеодима имеет сходство с химией тербия (Tb), который также способен образовывать диоксиды состава MeO2, что нетипично для большинства других редкоземельных металлов.
На их формирование влияют электронное строение (4f3 6s2), положение в семействе лантаноидов и значение электроотрицательности 1,13 по шкале Полинга.
Содержание страницы
- 1. Почему у празеодима стабильная степень окисления?
- 2. Степень окисления празеодима в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления празеодима
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления празеодима
- 6. Шпаргалка для празеодима
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у празеодима стабильная степень окисления?
Причина преобладания состояния +3 заключается в особенностях экранирования f-электронов, однако близость энергий 4f и 5d орбиталей позволяет празеодиму иногда проявлять валентность IV.
- В простом веществе (Pr⁰): Заряд равен 0. Конфигурация:
[Xe] 4f3 6s2. - В ионе (Pr+3): Празеодим отдает 2 электрона с 6s и 1 электрон с 4f подуровня. Конфигурация:
[Xe] 4f2.

Рис. 2. Процесс окисления празеодима: от серебристо-белого металла до окрашенных ионов +3 в составе различных соединений.
Степень окисления празеодима в соединениях
В зависимости от реагентов, празеодим в соединениях проявляет степень окисления, которая определяет цвет и химические свойства вещества:
- Оксид празеодима(III) (Pr2O3): Pr +3, O -2.
- Диоксид празеодима (PrO2): Pr +4, O -2.
- Хлорид празеодима(III) (PrCl3): Pr +3.
- Фторид празеодима(IV) (PrF4): Pr +4.
- Смешанный оксид (Pr6O11): содержит Pr +3 и Pr +4.
Высшая степень окисления
Высшая степень окисления празеодима в устойчивых твердых телах равна +4. В исключительных лабораторных условиях (газовая фаза) возможно достижение СО +5, что является пределом для данного элемента.
Низшая степень окисления
Для празеодима возможна редкая степень окисления +2 в некоторых иодидах, однако степень окисления празеодима равна 0 в металлическом виде — это наиболее типичное состояние чистого вещества.
Промежуточные степени окисления
Степень окисления празеодима в веществах часто выглядит как «дробная» (например, в Pr6O11), но на самом деле это кристаллическая решетка, где соседствуют ионы +3 и +4 в определенном соотношении.
Важно: Состояние +3 является «визитной карточкой» элемента: большинство его растворимых солей имеют характерный луково-зеленый цвет, где степень окисления празеодима формула соединения всегда подразумевает заряд +3.
Почему степень окисления чаще положительная?
Знак заряда определяется типично металлическим характером лантаноида:
- Положительная СО (+): Празеодим легко отдает электроны неметаллам из-за низкой энергии ионизации.
- Нулевая СО (0): Характерна для чистого металла, который медленно окисляется на воздухе.
- Отрицательная СО (-): Для лантаноидов, включая празеодим, отрицательные степени окисления невозможны.
Как определить степень окисления празеодима
По таблице Менделеева
- Семейство: f-элемент (редкоземельный металл).
- Валентные электроны: 5 (4f3 6s2).
- Атомная масса празеодима: 140,9 а.е.м.
По валентности (Число связей)
Как и у других лантаноидов, валентность празеодима преимущественно равна III, но может проявляться и IV.
- В оксиде (Pr2O3): Каждый атом празеодима образует три связи. Его валентность — III, а степень окисления — +3.
- В диоксиде (PrO2): Атом образует четыре связи с кислородом. Валентность — IV, СО празеодима — +4.
По электронной конфигурации
- Электронная формула празеодима: [Xe] 4f3 6s2.
- Атому празеодима степени окисления +3 достичь легче всего, так как это создает устойчивый энергетический баланс для f-подуровня.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для Pr(NO3)3 (нитрат празеодима III):
Сумма СО равна 0. Нитрат-группа (NO3) всегда -1. Обозначим Pr как x.
x + 3 · (-1) = 0
x — 3 = 0 ⇒ x = +3
Примеры степеней окисления празеодима
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +4, +5 | Высшие. Состояние +4 стабильно в оксидах, +5 крайне нестабильно. | PrO2, PrF4, Na2PrF6 |
| +3 | Наиболее стабильная. Основная форма существования элемента. | PrCl3, Pr2O3, Pr2(SO4)3 |
| +2 | Низкая. Встречается в редких безводных галогенидах. | PrI2, PrSe |
| 0 | Металл. Чистый элемент. | Pr (металлическая мишень) |
Шпаргалка для празеодима
- +3 — стабильная степень, дающая солям красивый зеленый цвет.
- Оксид Pr6O11 — самая распространенная коммерческая форма празеодима, черный порошок.
- Магнитные свойства — празеодим в СО +3 используется в мощных магнитах вместе с неодимом.
Пример решения задачи:
▶️ Дано:
Соединение: PrF4 (тетрафторид празеодима).
⌕ Найти:
Определите СО празеодима.
✨ Решение:
Фтор (F) всегда имеет СО -1. Уравнение: x + 4 · (-1) = 0 → x — 4 = 0 → x = +4.
✅ Ответ:
Pr(+4).
Проверка знаний
Показать ответы
Правильные ответы: 1, 3, 4.
Разбор ошибок:
2 — неверно: высшая СО празеодима в твердых телах +4, а +8 физически невозможна для него.
5 — неверно: празеодим является f-элементом и относится к редкоземельным металлам.
Часто задаваемые вопросы
Наиболее стабильной и распространенной в химии является степень окисления +3.
Да, это возможно в диоксиде (PrO2) и некоторых фторидах, где он проявляет свойства сильного окислителя.
Это связано с электронными переходами на 4f-подуровне, которые поглощают свет в видимой части спектра.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.