Теория:
Степень окисления палладия в большинстве соединений принимает значения +2, +4, реже встречаются состояния 0, +1, +3, +6.
Также существуют крайне нестабильные -1 и -2, которые проявляются только в специфических условиях (например, в сложных металлоорганических комплексах с особыми лигандами).
Например для высшей СО +6: в соединении Cs2PdF6 (гексафторпалладат цезия) степень окисления металла достигает +6.
Это происходит крайне редко и только при взаимодействии с мощнейшими окислителями (фтором).
В отличие от рутения, палладий находится в 10-й группе, но никогда не задействует все 10 электронов, так как его 4d-оболочка очень устойчива.
Для сравнения, отрицательная СО -2: встречается в таких комплексах, как [Pd(CO)3]2-.
Здесь ситуация обратная: палладий не отдает электроны, а за счет взаимодействия с молекулами угарного газа «принимает» избыточную электронную плотность на свободные орбитали.
Такие состояния крайне нестабильны на воздухе, так как металл стремится вернуться к положительному заряду, который для него энергетически естественнее.
Промежуточные же степени окисления, такие как +1 или +3, являются «неудобными» для атома.
Обладая уникальной конфигурацией [Kr] 4d10 5s0, палладию проще всего остановиться на стабильной форме +2.
Именно поэтому промежуточные соединения часто склонны к диспропорционированию — они самопроизвольно распадаются на более устойчивых соседей (например, +3 распадается на +2 и +4).
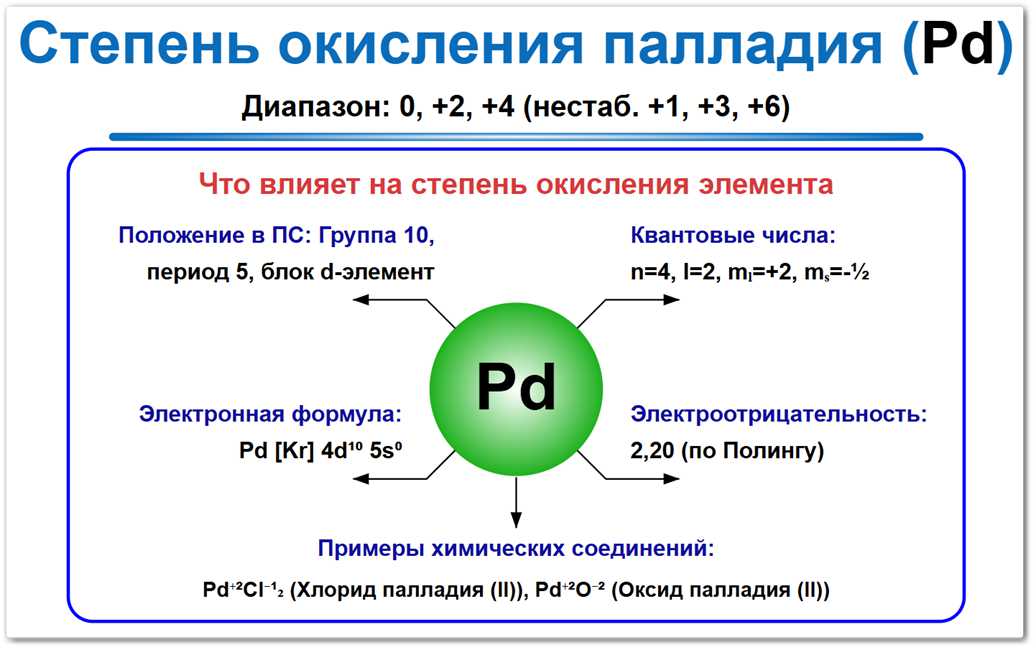
Рис. 1. Возможные степени окисления палладия: от 0 до +6. Наиболее устойчивые формы — +2 (хлориды) и +4 (комплексные соли), а высшая форма +6 возможна только в экстремальных условиях.
Обратите внимание, что химия палладия во многом схожа с химией платины (Pt), однако палладий чаще предпочитает состояние +2, в то время как платина одинаково стабильна и в +2, и в +4.
На их формирование влияют электронное строение (4d10 5s0), положение в 10-й группе и значение электроотрицательности 2,2 по шкале Полинга.
Содержание страницы
- 1. Почему у палладия стабильная степень окисления?
- 2. Степень окисления палладия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления палладия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления палладия
- 6. Шпаргалка для палладия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у палладия стабильная степень окисления?
Причина стабильности состояний палладия заключается в особенностях его d-оболочки. Палладий — единственный элемент, у которого на внешнем уровне (5s) ноль электронов в основном состоянии.
- В простом веществе (Pd⁰): Заряд равен 0. Конфигурация:
5s [ ] 4d [↑↓][↑↓][↑↓][↑↓][↑↓]. - В ионе (Pd+2): Палладий отдает 2 электрона с 4d-подуровня. Конфигурация:
[Kr] 4d8.

Рис. 2. Процесс окисления палладия: от металлического состояния до наиболее стабильного катиона +2 в составе солей.
Степень окисления палладия в соединениях
В зависимости от реагентов, палладий в соединениях проявляет степень окисления, определяющую его каталитические способности:
- Хлорид палладия(II) (PdCl2): Pd +2, Cl -1.
- Диоксид палладия (PdO2): Pd +4, O -2.
- Гексафторпалладат(IV) калия (K2PdF6): Pd +4.
- Оксид палладия(II) (PdO): Pd +2.
- Тетракарбонилпалладий (Pd(CO)4): Pd 0.
Высшая степень окисления
Высшая степень окисления палладия равна +6. Это значение крайне неустойчиво и встречается только в редких фторсодержащих комплексах. В отличие от других металлов 10-й группы, палладий очень неохотно отдает электроны выше состояния +4.
Низшая степень окисления
Для палладия возможны степени окисления -1 и -2 в металлоорганических соединениях, однако степень окисления палладия равна 0 в чистом металле — это наиболее важное состояние для его работы в качестве катализатора.
Промежуточные степени окисления
Степень окисления палладия в веществах иногда принимает значения +1 и +3 (например, в смешанном оксиде или сложных кластерах), но они быстро переходят в устойчивую форму +2.
Важно: Состояние +2 — основа всей химии этого элемента. Почти все растворимые соли и катализаторы содержат степень окисления палладия +2.
Почему степень окисления чаще положительная?
Знак заряда обусловлен тем, что палладий является благородным металлом:
- Положительная СО (+): Металл отдает d-электроны более активным неметаллам.
- Нулевая СО (0): Палладий способен поглощать огромные объемы водорода, оставаясь в нулевом заряде.
- Отрицательная СО (-): Требует присутствия специфических донорных лигандов.
Как определить степень окисления палладия
По таблице Менделеева
- Семейство: d-элемент (платиновый металл).
- Валентные электроны: 10 (все на d-подуровне, 5s — пустой).
- Атомная масса палладия: 106,4 а.е.м.
По валентности (Число связей)
В отличие от более активных металлов, валентность палладия чаще всего равна II.
- В хлориде (PdCl2): Атом палладия образует две связи с хлором. Его валентность — II, а СО равна +2.
- В диоксиде (PdO2): Палладий образует четыре связи с кислородом. Валентность — IV, СО палладия — +4.
По электронной конфигурации
- Электронная формула палладия: [Kr] 4d10 5s0.
- Атому палладия степени окисления +2 достичь наиболее выгодно, так как это требует минимальных затрат энергии на разрушение d-подуровня.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для K2PdCl6 (гексахлорпалладат калия):
Сумма СО равна 0. Калий +1, Хлор -1. Обозначим Pd как x.
2 · (+1) + x + 6 · (-1) = 0
2 + x — 6 = 0 ⇒ x = +4
Примеры степеней окисления палладия
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +6 | Высшая. Исключительно редкая и нестабильная. | Cs2PdF6 |
| +4 | Высокая. Характерна для комплексных фторидов и хлоридов. | PdO2, K2PdCl6 |
| +2 | Наиболее стабильная. Основная форма палладия. | PdCl2, PdO, Pd(NO3)2 |
| 0 | Металл. Состояние в катализаторах и ювелирных сплавах. | Pd (компактный), Pd/C (на угле) |
| -2 | Отрицательная. Крайне редкая в карбонилах. | [Pd(CO)3]2- |
Шпаргалка для палладия
- +2 — самая важная СО, образует большинство солей и комплексов.
- Водород — палладий (СО 0) может впитать до 900 объемов водорода на 1 объем металла.
- Катализатор — незаменим в реакциях кросс-сочетания (Нобелевская премия 2010 года).
Пример решения задачи:
▶️ Дано:
Соединение: K2PdCl4 (тетрахлорпалладат калия).
⌕ Найти:
Определите СО палладия.
✨ Решение:
Калий (K) равен +1, Хлор (Cl) равен -1. Уравнение: 2 · (+1) + x + 4 · (-1) = 0 → 2 + x — 4 = 0 → x = +2.
✅ Ответ:
Pd (+2).
Проверка знаний
Показать ответы
Правильные ответы: 1, 3, 4, 5.
Разбор ошибок:
2 — неверно: в отличие от рутения, палладий не отдает все электроны. Его высшая СО — +6, и та встречается крайне редко.
Часто задаваемые вопросы
Самой устойчивой является степень окисления +2. Большинство известных соединений палладия относятся именно к этой форме.
Да, это физически возможно, но такие соединения (например, соли гексафторпалладата) крайне агрессивны и разлагаются при контакте с большинством веществ.
Это результат «провала» электронов на 4d-подуровень для создания более симметричной и энергетически выгодной полностью заполненной оболочки (d10)

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.