Теория:
Степень окисления гафния (Hf) в подавляющем большинстве химических соединений принимает значение +4.
Это состояние является единственным по-настоящему стабильным для данного металла.
Но есть и +2 и +3 но редки и очень неустойчивы.
Кроме того, выделяют значение 0, которое характерно для свободного химического элемента в металлическом состоянии.
Например для наиболее стабильной СО +4: в таком веществе, как HfO2 (диоксид гафния), заряд иона металла составляет +4.
Для сравнения, низшие СО +2 и +3: крайне редко встречаются в некоторых галогенидах, например HfCl2 (хлорид гафния II), однако они крайне неустойчивы и легко окисляются.
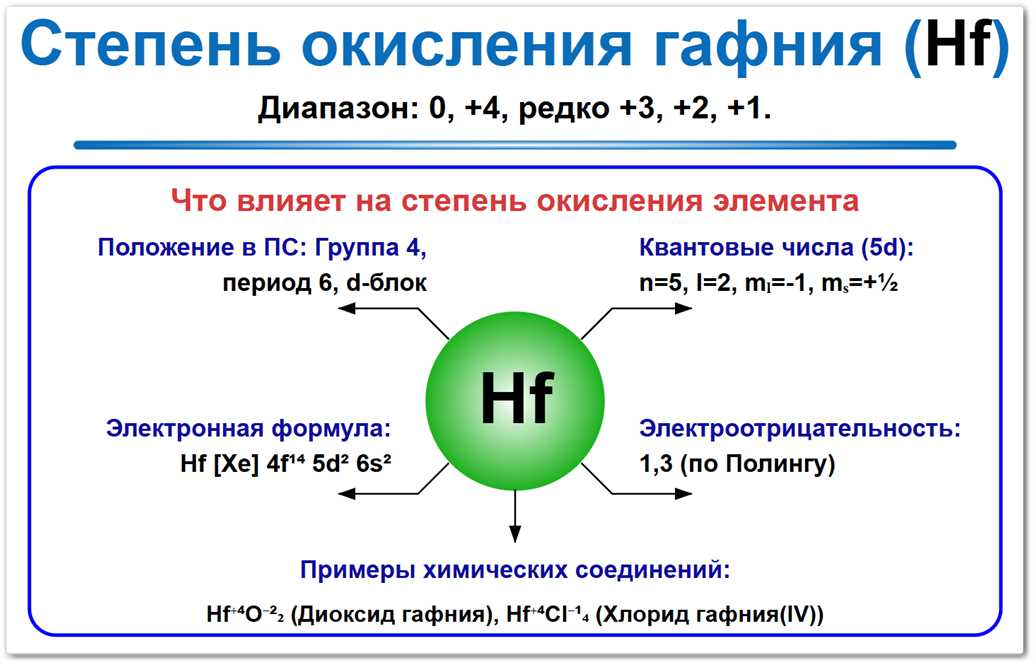
- Почему +4? Гафний относится к 4-й группе и имеет электронную конфигурацию [Xe] 4f14 5d2 6s2. Отдача всех четырех внешних электронов (двух с 6s и двух с 5d-подуровней) приводит к формированию наиболее устойчивой электронной оболочки.
- Почему +4 так доминирует? Энергия ионизации первых четырех электронов сравнительно невелика для переходного металла этого периода, а образующийся катион Hf4+ обладает высокой плотностью заряда, что способствует созданию прочных ковалентно-ионных связей.
- Почему нет более высоких СО? После потери четырех электронов гафний достигает конфигурации инертного газа (с заполненным 4f14 слоем). Изъятие следующего электрона из глубоких слоев потребовало бы запредельных энергетических затрат.
Стоит заметить, что химия гафния в его основном состоянии +4 проявляет поразительное сходство с химией циркония (Zr).
Из-за лантаноидного сжатия их ионные радиусы почти идентичны, что делает эти элементы «химическими близнецами».
На спецификацию его параметров влияют электронная структура (4f14 5d2 6s2), нахождение в 4-й группе системы элементов и величина электроотрицательности 1,3 по шкале Полинга.
Содержание страницы
- 1. Почему +4 — самая стабильная степень окисления у гафния
- 2. Степень окисления гафния в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему гафний выступает донором электронов (степень +4), а не акцептором?
- 4. 4 способа определить степень окисления гафния
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления гафния
- 6. Шпаргалка для гафния
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему +4 — самая стабильная степень окисления у гафния
Причина устойчивости состояний гафния кроется в возможности полной деформации внешних энергетических уровней, что при потере электронов обеспечивает переход к инертной конфигурации.
- В простом веществе (Hf⁰): Заряд равен 0. Конфигурация:
[Xe] 4f14 5d2 6s2. - В катионе (Hf+4): Гафний лишается 4 электронов. Конфигурация:
[Xe] 4f14(стабильный остов).
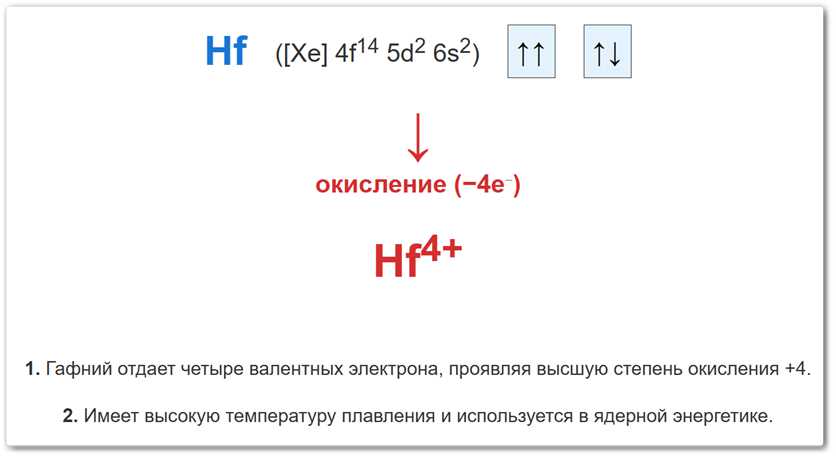
Рис. 2. Механизм окисления гафния: переход от нейтрального атома к наиболее надежному катиону +4 через отдачу всех валентных электронов.
Степень окисления гафния в соединениях
В зависимости от реагентов, гафний в соединениях проявляет степень окисления, которая обуславливает его применение в качестве высокотемпературной керамики или компонентов ядерных реакторов:
- Диоксид гафния (HfO2): Hf +4, O -2.
- Тетрахлорид гафния (HfCl4): Hf +4, Cl -1.
- Карбид гафния (HfC): Hf +4, C -4 (условно в тугоплавких фазах).
- Нитрат гафния (Hf(NO3)4): Hf +4.
- Тетрафторид гафния (HfF4): Hf +4.
Высшая степень окисления
Высшая степень окисления Hf составляет +4. Данный показатель строго соответствует номеру группы элемента в периодической таблице.
Низшая степень окисления
Для гафния упоминаются степени окисления +1, +2 и +3 в искусственно созданных кластерах, однако металл гафний имеет степень окисления 0 в чистом виде — это базис для металлургических расчетов.
Промежуточные степени окисления
Степень окисления гафния в веществах почти никогда не отклоняется от четверки.
В отличие от элементов начала d-блока, гафний не склонен к образованию стабильного ряда разнообразных валентных форм.
Важно: Благодаря стабильности состояния +4, диоксид гафния используется как диэлектрик в микропроцессорах, где степень окисления гафния формула соединения гарантирует неизменность свойств прибора.
Почему гафний выступает донором электронов (степень +4), а не акцептором?
Направление заряда диктуется металлическим характером элемента и его координационным числом:
- Положительная СО (+): Гафний легко отдает электроны электроотрицательным неметаллам, образуя прочные катионы.
- Нулевая СО (0): Свойственна для блестящего, тугоплавкого переходного металла.
- Отрицательная СО (-): У гафния не обнаружена, так как его сродство к электрону крайне низкое.
4 способа определить степень окисления гафния
По таблице Менделеева
- Семейство: d-элемент.
- Валентные электроны: 4 (2 на 6s-орбитали и 2 на 5d-орбитали).
- Атомная масса гафния: 178,5 а.е.м.
По валентности (Число связей)
В подавляющем большинстве случаев валентность гафния неизменно равна IV.
- В диоксиде (HfO2): Гафний формирует связи, эквивалентные валентности IV, СО — +4.
- В тетрахлориде (HfCl4): Металл проявляет валентность IV, СО — +4.
По электронной конфигурации
- Электронная формула гафния: [Xe] 4f14 5d2 6s2.
- Атому гафния степени окисления +4 достичь энергетически выгодно, так как это полностью очищает 6s и 5d уровни.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для HfF4 (фторид гафния IV):
Сумма СО равна 0. Фтор всегда -1. Обозначим Hf как x.
x + 4 · (-1) = 0 ⇒ x = +4
Примеры степеней окисления гафния
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +4 | Единственно стабильная. Типичная форма для всех природных и синтетических фаз. | HfO2, HfCl4, HfF4 |
| +2, +3 | Крайне неустойчивые. Существуют только в специальных лабораторных условиях. | HfCl2, HfBr3 |
| 0 | Металл. Состояние чистого простого вещества. | Hf (слиток) |
Шпаргалка для гафния
- +4 — доминирующая степень окисления, обеспечивающая химическую инертность.
- Близнец циркония — из-за СО +4 и схожих размеров их практически невозможно разделить химически.
- Тугоплавкость — соединения гафния(+4), такие как карбиды, имеют одни из самых высоких температур плавления.
Пример решения задачи:
▶️ Дано:
Соединение: HfCl4 (хлорид гафния IV).
⌕ Найти:
Определите СО гафния.
✨ Решение:
Хлор (Cl) как типичный галоген равен -1. Уравнение: x + 4 · (-1) = 0 → x — 4 = 0 → x = +4.
✅ Ответ:
Hf(+4).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: у гафния нет стабильных состояний выше +4, так как его валентная оболочка ограничена 4 электронами.
Часто задаваемые вопросы
Безусловно, это состояние +4.
В обычных условиях — нет. Низшие СО (+2, +3) можно получить лишь в жестких лабораторных условиях, и они моментально разрушаются.
Потому что у атома всего 4 валентных электрона. Для достижения СО +5 пришлось бы разрушать глубокий и очень стабильный f-подуровень.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.