Теория:
Степень окисления гадолиния (Gd) в подавляющем большинстве стабильных соединений принимает значение +3.
В редких случаях зафиксированы низшие состояния +1 и +2.
Гадолиний — это типичный представитель семейства лантаноидов, чья химия определяется стремлением достичь энергетически выгодной конфигурации с наполовину заполненным f-подуровнем.
Например для высшей СО +3: в соединении Gd2O3 (оксид гадолиния) степень окисления металла равна +3.
Это происходит потому, что гадолиний находится в ряду лантаноидов и при химическом взаимодействии с кислородом он задействует свои валентные электроны (5d1 6s2), достигая стабильного состояния.
При этом его 4f-подуровень остается наполовину заполненным (4f7), что придает атому особую устойчивость.
Для сравнения, редкая СО +2: встречается в специфических галогенидах, таких как GdI2.
Здесь ситуация иная: гадолиний не полностью отдает валентные электроны, что делает такие соединения сильными восстановителями.
Подобные состояния крайне нестабильны и стремятся перейти в классическую форму +3, которая для него энергетически естественнее.
Такие промежуточные формы легко окисляются, так как конфигурация с «лишним» электроном на d-подуровне менее выгодна, чем чистая полузаполненная f-оболочка.
В отличие от соседей по группе (например, церия или тербия), гадолиний практически не проявляет степень окисления +4.
Обладая конфигурацией [Xe] 4f7 5d1 6s2, гадолинию крайне «невыгодно» трогать наполовину заполненный 4f-слой, который защищен правилом Хунда.
Атому проще остановиться на стабильной форме +3, отдав только внешние электроны.
Именно поэтому гадолиний считается одним из самых «предсказуемых» лантаноидов в плане валентности — он практически всегда выступает в роли трехзарядного катиона.
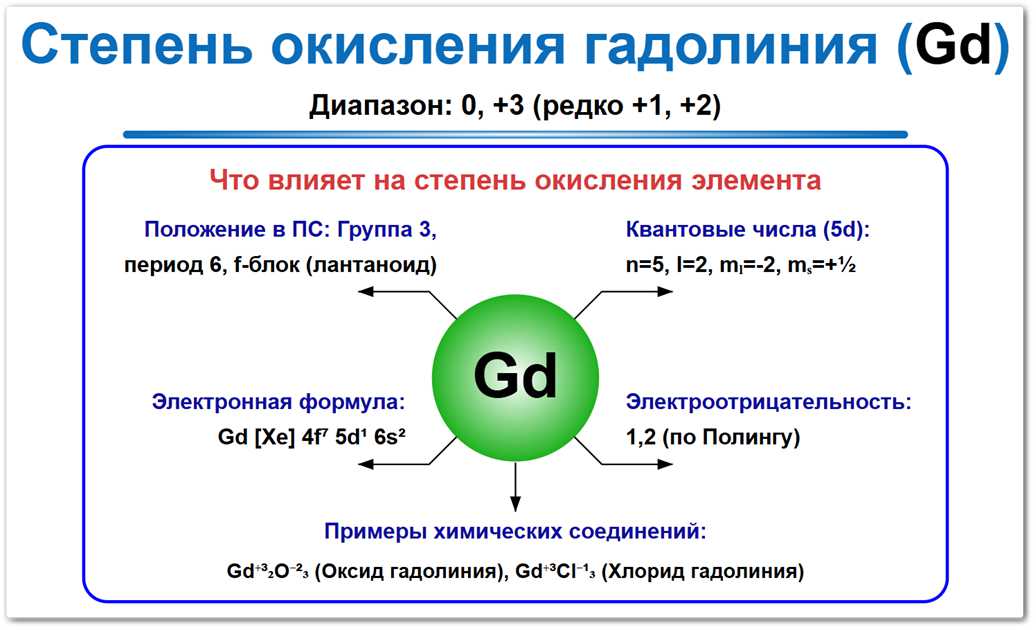
Рис. 1. Возможные степени окисления гадолиния: наиболее устойчивая форма — +3.
Состояния +1 и +2 встречаются крайне редко в составе твердотельных кластерных соединений.
Обратите внимание, что химия гадолиния демонстрирует так называемый «гадолиниевый излом» в графиках свойств лантаноидов, что связано именно с особой устойчивостью конфигурации 4f7.
На формирование его свойств влияют электронное строение (4f7 5d1 6s2), положение в середине ряда лантаноидов и значение электроотрицательности 1,2 по шкале Полинга.
Содержание страницы
- 1. Почему у гадолиния стабильная степень окисления?
- 2. Степень окисления гадолиния в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления гадолиния
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления гадолиния
- 6. Шпаргалка для гадолиния
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у гадолиния стабильная степень окисления?
Причина стабильности состояния +3 заключается в достижении наполовину заполненного 4f-подуровня, что является одной из самых устойчивых электронных конфигураций в химии f-элементов.
- В простом веществе (Gd⁰): Заряд равен 0. Конфигурация:
[Xe] 4f7 5d1 6s2. - В ионе (Gd+3): Гадолиний отдает 3 валентных электрона (5d и 6s). Конфигурация:
[Xe] 4f7.

Рис. 2. Процесс окисления гадолиния: потеря трех электронов приводит к образованию катиона с идеально симметричной f-оболочкой.
Степень окисления гадолиния в соединениях
В большинстве реакций гадолиний в соединениях проявляет степень окисления, которая делает его важным материалом для МРТ-контрастирования и ядерной энергетики:
- Оксид гадолиния (Gd2O3): Gd +3, O -2.
- Хлорид гадолиния (GdCl3): Gd +3, Cl -1.
- Нитрат гадолиния (Gd(NO3)3): Gd +3.
- Фторид гадолиния (GdF3): Gd +3.
- Сульфат гадолиния (Gd2(SO4)3): Gd +3.
Высшая степень окисления
Высшая степень окисления гадолиния равна +3. Это значение является пределом для элемента в обычных условиях, так как для дальнейшего окисления потребовалось бы разрушить очень стабильный 4f7 слой.
Низшая степень окисления
В специфических кластерных соединениях и дигалогенидах возможна степень окисления +2.
Однако степень окисления гадолиния равна 0 в металлическом виде — это стандарт для расчетов параметров чистого вещества.
Промежуточные степени окисления
Степень окисления гадолиния в веществах крайне редко принимает значения ниже +3.
Такие формы неустойчивы и при контакте с водой или кислородом моментально переходят в +3.
Важно: Именно стабильность состояния +3 и наличие семи неспаренных электронов делают гадолиний уникальным парамагнетиком, что используется в медицине для улучшения качества снимков МРТ.
Почему степень окисления чаще положительная?
Знак заряда определяется металлической природой лантаноида:
- Положительная СО (+): Гадолиний легко отдает электроны неметаллам, достигая симметричной электронной оболочки.
- Нулевая СО (0): Характерна для чистого серебристо-белого металла.
- Отрицательная СО (-): Физически невозможна для гадолиния из-за его низкой электроотрицательности и типично металлических свойств.
Как определить степень окисления гадолиния
По таблице Менделеева
- Семейство: f-элемент (лантаноид).
- Валентные электроны: 3 электрона участвуют в образовании связей (с подуровней 5d и 6s).
- Атомная масса гадолиния: 157 а.е.м.
По валентности (Число связей)
В отличие от переходных металлов, валентность гадолиния постоянна. В стабильных соединениях она всегда равна III.
- В оксиде (Gd2O3): Атом гадолиния образует три связи с кислородом. Его валентность — III, а степень окисления равна +3.
- В фториде (GdF3): Гадолиний образует три связи с фтором. Валентность — III, СО — +3.
По электронной конфигурации
- Электронная формула гадолиния: [Xe] 4f7 5d1 6s2.
- Атому гадолиния степени окисления +3 достичь выгоднее всего, так как конфигурация f7 обладает повышенной энергией стабилизации.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для Gd(NO3)3 (нитрат гадолиния):
Сумма СО равна 0. Нитрат-ион (NO₃) всегда -1. Обозначим Gd как x.
x + 3 · (-1) = 0 ⇒ x = +3
Примеры степеней окисления гадолиния
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +3 | Наиболее стабильная. Единственная типичная СО. | Gd2O3, GdCl3, Gd2(SO4)3 |
| +2 | Низкая. Встречается в редких кластерах. | GdI2, GdCl2 |
| 0 | Металл. Состояние простого вещества. | Gd (слиток или порошок) |
Шпаргалка для гадолиния
- +3 — универсальная и самая устойчивая степень окисления.
- Медицина — ионы Gd³⁺ используются как контрастное вещество в МРТ.
- Магнетизм — гадолиний обладает самым высоким сечением захвата тепловых нейтронов среди всех элементов.
Пример решения задачи:
▶️ Дано:
Соединение: Gd2(SO4)3 (сульфат гадолиния).
⌕ Найти:
Определите СО гадолиния.
✨ Решение:
Сульфат-ион (SO₄) равен -2. Уравнение: 2x + 3 · (-2) = 0 → 2x — 6 = 0 → x = +3.
✅ Ответ:
Gd(+3).
Проверка знаний
Показать ответы
Правильные ответы: 2, 4, 5.
Разбор ошибок:
1 — неверно: гадолиний является f-элементом (лантаноидом).
3 — неверно: высшая степень окисления гадолиния ограничена +3, состояние +8 для него невозможно.
Часто задаваемые вопросы
Безусловно, это +3. В этом состоянии атом достигает идеальной симметрии 4f-подуровня.
Потому что для перехода в +4 нужно забрать электрон из устойчивой конфигурации 4f7, что требует колоссальных затрат энергии.
Энергетически атому Gd намного дешевле стать положительным ионом Gd3+, чем тратить колоссальную энергию на удержание лишних отрицательных зарядов.
