Теория:
Степень окисления флеровия (Fl) в химических соединениях чаще всего проявляет стабильную степень окисления +2, что отличает его от легких аналогов по группе.
Это обусловлено положением элемента в 14-й группе Периодической системы.
В отличие от углерода или кремния, у сверхтяжелого флеровия из-за релятивистских эффектов 7s-электроны становятся очень инертными («эффект инертной пары»), что делает состояние +2 более выгодным, чем +4.
Кроме того, выделяют показатель 0, который относится к флеровию в виде простого вещества (предположительно, очень летучий металл или даже инертный газ по поведению).
Например для наиболее стабильной СО +2: в гипотетическом соединении FlCl2 (хлорид флеровия II) заряд иона равен +2.
В этом состоянии флеровий проявляет сходство со свинцом (Pb), но с еще более выраженной стабильностью низшей степени окисления.
Для сравнения, другие СО: высшая степень окисления +4 (например, в FlF4) предсказывается теоретически, но экспериментально ее достичь крайне сложно, так как флеровий крайне неохотно отдает свои 7s-электроны.
- Почему +2? Электронная формула флеровия [Rn] 5f14 6d10 7s2 7p2. Энергия связи 7s-электронов настолько велика, что в реакциях участвуют преимущественно только два 7p-электрона.
- Почему +4 менее вероятна? Релятивистское сжатие 7s-орбитали делает эти электроны «закрытыми» для химического взаимодействия, что резко снижает стабильность четыреххлористых и других четырехзарядных соединений.
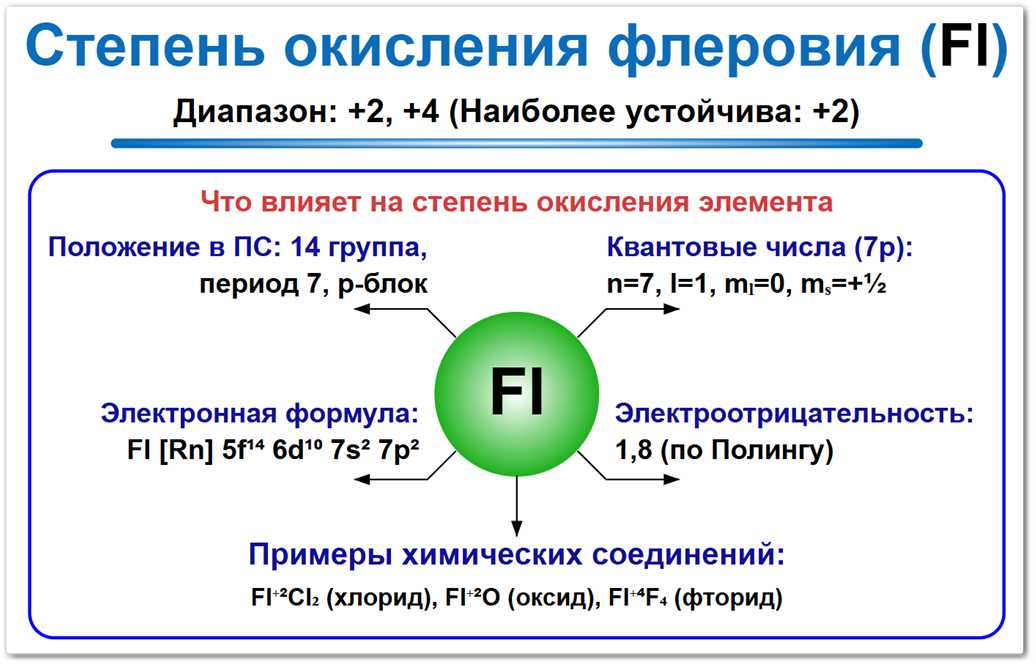
Рис. 1. Основная степень окисления флеровия: 0 и +2.
Состояние +2 считается наиболее характерным для химии флеровия в растворах и газовой фазе, согласно последним теоретическим моделям и экспериментам.
Важно заметить, что флеровий — радиоактивный элемент, открытый в Дубне (ОИЯИ). Его время жизни измеряется секундами (наиболее стабильный изотоп 289Fl живет около 2 секунд).
Химия флеровия исследуется методами адсорбции отдельных атомов на золотых поверхностях.
Первые опыты показали, что он химически менее активен, чем свинец, и проявляет свойства, промежуточные между металлом и благородным газом.
Содержание страницы
- 1. Почему +2 — самая характерная степень окисления у флеровия
- 2. Степень окисления флеровия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему флеровий «предпочитает» заряд +2, а не +4?
- 4. 4 способа определить степень окисления флеровия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления флеровия
- 6. Шпаргалка
- 7. Флеровий вне учебника: что скрывает наука?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +2 — самая характерная степень окисления у флеровия
Стабильность определяется балансом между энергией разрыва электронной пары и энергией образования химических связей.
- В простом веществе (Fl0): Заряд равен 0. Конфигурация:
[Rn] 5f14 6d10 7s2 7p2. - В двухвалентном ионе (Fl+2): Флеровий теряет два 7p-электрона. Конфигурация:
[Rn] 5f14 6d10 7s2.

Рис. 2. Схема образования степени окисления +2: удаление только 7p-электронов.
Степень окисления флеровия в соединениях
- Хлорид флеровия(II) (FlCl2): Fl +2.
- Фторид флеровия(IV) (FlF4): Fl +4 (крайне нестабилен).
Высшая степень окисления
Высшая степень окисления Fl теоретически равна +4, но она не является типичной.
Низшая степень окисления
Характерна степень окисления 0, причем из-за релятивистских эффектов атом флеровия в состоянии 0 очень инертен.
Промежуточные степени окисления
Данные о существовании СО +1 или других промежуточных состояний отсутствуют.
Важно: Флеровий находится на границе «острова стабильности» — области сверхтяжелых ядер, которые живут дольше своих соседей.
Почему флеровий «предпочитает» заряд +2, а не +4?
- Релятивистский эффект: Скорость электронов у тяжелого ядра заставляет 7s-орбиталь «сжиматься» и становиться очень стабильной.
- Энергия ионизации: Энергия, необходимая для отрыва третьего и четвертого электрона (с 7s-подуровня), слишком высока, чтобы компенсироваться энергией образования химических связей.
4 способа определить степень окисления флеровия
По таблице Менделеева
- Семейство: Постпереходные металлы (формально).
- Валентные электроны: 4.
- Атомная масса: ~289 а.е.м.
По валентности (Число связей)
Валентность флеровия (Fl) чаще всего равна II.
Несмотря на наличие 4 валентных электронов, флеровий ведет себя как «двухвалентный свинец на стероидах», ограничиваясь образованием двух связей.
По электронной конфигурации
Электронная формула флеровия: [Rn] 5f14 6d10 7s2 7p2.
Как происходит ионизация:
- Валентные электроны: Четыре (7s² 7p²).
- Механизм потери: Легко уходят только два p-электрона.
- Результат: Ион Fl2+ с устойчивой конфигурацией
7s2.
По химическому соединению (Алгебраический расчет)
Пример для FlBr2:
- 1. Бром (Br) имеет СО -1.
- 2. Два атома брома: 2 · (-1) = -2.
- 3. Уравнение: x + (-2) = 0.
- 4. Решение: x = +2.
✅ Вывод: Степень окисления флеровия здесь равна +2.
Примеры степеней окисления флеровия
| СО | Характеристика | Примеры |
|---|---|---|
| +2 | Наиболее характерная. | FlCl2, FlO |
| +4 | Высшая (теоретическая). | FlF4 |
Шпаргалка
- +2 — главная рабочая СО.
- Эффект инертной пары — причина стабильности +2.
Флеровий вне учебника: что скрывает наука?
«Благородный» металл?
Первоначальные эксперименты по адсорбции флеровия на золоте удивили ученых: он показал очень слабую связь с поверхностью.
Это породило гипотезу, что флеровий может быть химически почти таким же пассивным, как инертные газы (радон), оставаясь при этом металлом по структуре.
Остров стабильности:
Флеровий — «звезда» теории об острове стабильности. Ученые надеются найти изотопы флеровия с еще большим количеством нейтронов, которые могли бы жить дни или даже годы.
Интересный факт: Элемент назван в честь Лаборатории ядерных реакций имени Г. Н. Флерова, где он и был впервые получен. Сам Флеров был ключевой фигурой в советском атомном проекте.
Пример решения задачи:
▶️ Дано:
Соединение: FlO (оксид флеровия II).
⌕ Найти:
Определите степень окисления (СО) флеровия.
✨ Решение:
1. Степень окисления кислорода в оксидах равна -2.
2. Молекула нейтральна, значит сумма зарядов равна 0.
3. Обозначим СО флеровия за x: x + (-2) = 0.
4. Отсюда x = +2.
✅ Ответ:
СО флеровия (Fl) в оксиде равна +2.
Проверка знаний
Показать ответы
Правильные ответы: 1, 3, 4.
Разбор ошибок:
2 — неверно: +2 намного стабильнее из-за инертной пары электронов.
5 — неверно: синтезируется только искусственно.
Часто задаваемые вопросы
Обусловлена следующими факторами:
1. Эффект инертной пары.
2. Доступность p-электронов.
3. Сближение уровней.
Самая стабильная для флеровия (Fl) +2.
Флеровий — металл, а его внешняя электронная оболочка (7s27p2) слишком далека от завершения (p6), чтобы принимать лишние электроны. Ему энергетически невыгодно образовывать отрицательные ионы.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.